Part Ⅰ Antioxidants catalítics al ronyó
Apr 19, 2023
Resum
L'oxigen reactiu i el nitrogen reactiu estan estretament associats amb la lesió renal, inclosa la lesió renal aguda, la malaltia renal crònica, la nefropatia hipertensiva i la nefropatia diabètica. Per tant, els antioxidants són importants en el tractament de les malalties renals. Els antioxidants catalítics es defineixen com a petites molècules que imitan enzims antioxidants com la superòxid dismutasa, la catalasa i la glutatió peroxidasa, alguns dels quals són potents desintoxicants de peròxids lipídics i peroxinitrit. S'ha demostrat que diversos antioxidants catalítics són efectius en diversos models de malaltia in vitro i in vivo associats a l'estrès oxidatiu, inclosa la malaltia renal. Aquest article revisa el paper dels enzims antioxidants en la malaltia renal, la classificació dels antioxidants catalítics i el seu ús actual en la malaltia renal.
Paraules clau
catalasa; glutatió peroxidasa; superòxid dismutasa; antioxidants catalítics; ronyó;Beneficis de Cistanche.

Feu clic aquí per obtenirEfectes de cistanche sobre el ronyó
Introducció
L'estrès oxidatiu descriu el desequilibri entre la formació de substàncies reactives i la defensa dels antioxidants quan es pertorba la senyalització redox o el dany molecular. Les espècies reactives d'oxigen (ROS) i les espècies reactives de nitrogen (RNS) són subproductes tòxics del metabolisme essencial de l'oxigen en els organismes vius. Aquests radicals lliures inclouen el superòxid (O2-), peròxid d'hidrogen (H2O2), òxid nítric (NO-), radicals hidroxil (OH-), peroxinitrit (ONOO-) i radicals peroxil lipídic (LOO-). Durant la respiració, O2- es produeix de manera endògena als mitocondris, i les ROS són produïdes per complexos de la cadena de transport d'electrons i per metabòlits parcialment reduïts de l'oxigen molecular formats en sistemes biològics. La producció excessiva de ROS es produeix mitjançant l'activació d'enzims oxidatius específics, com ara la nicotinamida adenina dinucleòtid fosfat (NADPH) oxidasa (NOX), la xantina oxidasa, l'òxid nítric sintasa desacoblat (NOS) i els enzims metabolitzadors de l'àcid araquidònic. ROS indueix danys a les proteïnes cel·lulars i els lípids , hidrats de carboni i ADN, que finalment condueixen a una disfunció cel·lular. Per tant, s'han considerat reguladors importants en moltes vies de senyalització cel·lular des dels primers temps (figura 1). Els mecanismes de defensa antioxidant són complexos i compartimentats i poden regular de manera independent els nivells de ROS al citoplasma, els mitocondris i el nucli. En els sistemes vius, els nivells de ROS estan regulats per una varietat d'enzims antioxidants, incloent la superòxid dismutasa (SOD), la catalasa (CAT), la glutatió peroxidasa (GPx), la peroxiredoxina (Prx), la tioredoxina (Trx) i la citocrom c oxidasa.
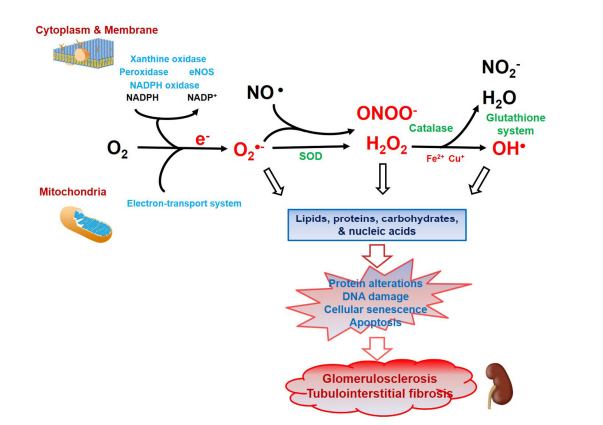
Figura 1. Visió esquemàtica de les fonts endògenes d'estrès oxidatiu i reaccions antioxidants en dany renal. Les fonts d'estrès oxidatiu exògenes (factors ambientals com la contaminació de l'aire i l'aigua, el tabaquisme, les drogues i la radiació) i endògenes (processos metabòlics normals en els organismes vius) produeixen espècies reactives d'oxigen (ROS). De manera endògena, les ROS es generen com a productes de reaccions bioquímiques als mitocondris (sistema de transport d'electrons; ETS), la membrana plasmàtica, el citoplasma (inclosos peroxisomes i lisozimes) i la membrana del reticle endoplasmàtic. L'ETS mitocondrial, l'adenina dinucleòtid fosfat (NADPH) oxidasa, la xantina oxidasa, la mieloperoxidasa i l'òxid nítric sintasa endotelial (eNOS) són les principals fonts de formació de ROS cel·lular. Una reacció important en la formació de radicals lliures són les reaccions semblants a Fenton i Fenton per produir ROS en les quals Fe2 més i Cu més reaccionen amb H2O2 per formar OH , respectivament. Per protegir i reparar la lesió molecular causada per ROS, les cèl·lules utilitzen un sistema de defensa compost d'antioxidants enzimàtics, incloent la superòxid dismutasa (SOD), catalasa, peroxidasa i antioxidants no enzimàtics fets pel sistema de glutatió. El lloc principal de generació d'O2•− és la membrana mitocondrial interna durant els processos ETS. La descomposició de H2O2 en aigua i oxigen es fa per SOD, el sistema de glutatió i catalasa, en aquest ordre. L'excés de ROS provoca peroxidació lipídica, nitrooxidació, oxidació del glicol i dany oxidatiu a l'ADN, que conjuntament poden causar alteracions de proteïnes, danys a l'ADN, senescència cel·lular i apoptosi. Tots aquests canvis eventualment condueixen a glomeruloesclerosi i fibrosi tubulointersticial.
L'estrès oxidatiu està implicat en la patogènesi de diverses malalties renals, com ara la lesió renal aguda (IRA), la malaltia renal crònica (ERC), la nefropatia hipertensiva i la nefropatia diabètica. Per tant, els antioxidants són eines efectives per al tractament de les malalties renals. Els antioxidants catalítics són imitacions de molècules petites d'enzims antioxidants similars a SOD, CAT i GPx, alguns dels quals poden actuar com a agents desintoxicants de peròxids de lípids i ONOO-. Com que aquests compostos són catalítics i no només eliminadors de radicals lliures, mostren una activitat antioxidant més forta que altres suplements dietètics. Aquest article repassa el paper dels enzims antioxidants en les malalties renals, la classificació dels antioxidants catalítics i l'estat actual de la seva aplicació en les malalties renals.
Enzims antioxidants i malaltia renal
Les cèl·lules tenen importants mecanismes de defensa antioxidant per protegir-se del dany tòxic dels radicals lliures. Els antioxidants poden tenir fonts endògenes o exògenes, amb la síntesi endògena produint enzims i petites molècules o dieta que proporcionen importants defenses exògenes. Segons la seva activitat, els antioxidants es poden classificar en enzimàtics o no enzimàtics. Els principals antioxidants enzimàtics són SOD, CAT i GPx. Els antioxidants endògens no enzimàtics inclouen l-arginina, àcid lipoic, coenzim Q10, melatonina, albúmina i àcid úric. Els antioxidants no enzimàtics exògens inclouen fàrmacs com l'àcid ascòrbic (vitamina C), l'alfa-tocoferol (vitamina E), els antioxidants fenòlics, l'oli de lecitina i l'acetilcisteïna. També hi ha diversos sistemes antioxidants al ronyó per protegir els teixits renals i les cèl·lules associades de l'estrès oxidatiu.

Suplements de cistanche
1. Superòxid Dismutasa i Malaltia Renal
L'anió radical superòxid és una substància potencialment nociva produïda per la reducció d'un sol electró de l'oxigen molecular durant la respiració. La SOD és el sistema enzimàtic antioxidant clau i la majoria dels organismes que viuen en presència d'oxigen expressen almenys un SOD. El metall lligand del lloc actiu permet la classificació de SOD: SOD coure-zinc (Cu/Zn-SOD), SOD de manganès (Mn-SOD), SOD de ferro (Fe-SOD) i SOD de níquel (NiSOD). SOD és un grup de metaloenzims que catalitzen la reacció de clivage per desintoxicar ROS, que catalitza la ruptura de dos O2- per generar H2O2i molecular O2, que es descomponen en aigua i oxigen pel CAT.
![]()
La SOD també es divideix en tres isoformes principals segons la seva localització en compartiments subcel·lulars: SOD1 (Cu/Zn-SOD), SOD2 (Mn-SOD) i SOD3 (SOD extracel·lular, EC-SOD), que solen trobar-se al ronyó. .SOD1 està constitutivament present al citoplasma i al buit de membrana dels mitocondris, mentre que SOD2 està present als mitocondris de les cèl·lules eucariotes. SOD3 és un Cu/Zn-SOD que es secreta a l'espai extracel·lular. D'aquests tres SOD, SOD1 és abundant a la majoria dels teixits, i representa el 60-80 per cent de l'activitat de la SOD a la vasculatura renal i aproximadament el 30 per cent de l'activitat de la SOD a la vasculatura renal. SOD2 també s'expressa a la majoria de cèl·lules dels teixits, com ara l'estómac, el pulmó, el múscul esquelètic, la melsa, el cor, el fetge, el ronyó i el cervell. La SOD3 s'expressa molt en la vasculatura, el ronyó, el pulmó i el cor. Tot i que SOD1 representa el percentatge més alt d'activitat de SOD renal, els canvis patològics associats amb la deficiència de SOD2 i la deficiència de SOD1 són més greus perquè ROS i RNS es formen principalment als mitocondris.
Les tres isoformes SOD tenen un paper crucial en la progressió i la remissió de diverses malalties renals. Diversos estudis experimentals proporcionen evidència que l'eliminació o la sobreexpressió de gespa mitjançant manipulació genètica o fàrmacs poden alterar l'estrès oxidatiu i la gravetat de la malaltia en AKI o CKD. L'esgotament de SOD1 condueix a un augment significatiu de la senyalització renal mediada pel factor nuclear potenciador de la cadena lleugera (NF-κB) i el dany oxidatiu de l'ADN a les cèl·lules B activades. De fet, la funció renal es va reduir greument després d'una lesió per isquèmia-reperfusió renal (I/R) en ratolins eliminatoris de SOD1, i el tractament amb SOD1 humà recombinant va reduir significativament el ROS i va millorar la funció renal disminuint el factor de necrosi tumoral (TNF) i la interleucina (IL) { {7}} nivells en teixits lesions renals I/R. En els ratolins d'obstrucció ureteral unilateral (UUO), la deficiència de SOD1 va millorar la hipertensió sensible a la sal i la fibrosi tubulointersticial, mentre que, en els ratolins d'obstrucció ureteral unilateral b, la sobreexpressió SOD1 o el tractament crònic del lòbul temporal van abrogar aquestes troballes. SOD1 també modula la remodelació microvascular renal, la reactivitat de les artèries petites i la sensibilitat a l'angiotensina II (Ang II). Els ratolins eliminatoris de sOD1 van mostrar una pressió arterial elevada i van reduir el diàmetre de l'artèria petita aferent durant la infusió d'Ang II, mentre que aquests canvis es van atenuar en els ratolins transgènics SOD1. En la nefropatia diabètica, els productes finals de glicosilació avançada (AGE) milloren l'estrès oxidatiu mitjançant la generació de NOX de ROS als mitocondris, i les interaccions entre AGE i receptors per a AGE (RAGE) milloren l'inici de la senyalització relacionada. Els enzims antioxidants, com SOD i CAT, inhibeixen la producció de ROS mediada per l'edat. En comparació amb el control dels ratolins diabètics, els ratolins transgènics db/db SOD1 i els ratolins transgènics SOD1 tractats amb estreptozotocina STZ van mostrar una proteïnúria reduïda, expressions de factor de creixement transformant (TGF)- 1 i col·lagen IV, així com l'expansió de la matriu tilacoïdal i els marcadors reduïts de estrès oxidatiu.
S'ha informat que la disfunció SOD2 agreuja la disfunció renal, la fibrosi tubulointersticial, la inflamació i l'apoptosi renal. Parajuli et al. va trobar que els ratolins amb deficiència de SOD2-específics de ronyó tenien ronyons més lleugers i més petits que els ratolins de tipus salvatge amb un estrès oxidatiu millorat i lesions tubulars, inclosa la dilatació tubular distal, la formació de motlles de proteïnes i la inflamació de les cèl·lules epitelials tubulars distals. En la lesió renal I/R, l'expressió SOD2 es va reduir a la unitat renal distal i la funció renal es va deteriorar en els ratolins eliminadors de SOD2 en comparació amb els ratolins control. En un model de rata d'AKI induïda per radiocontrast, el pretractament SOD2 recombinant va augmentar significativament l'activitat de la SOD i va millorar la disminució de la funció renal i la necrosi tubular. A més, una dieta alta en sal en ratolins amb deficiència de sod2- va provocar un augment significatiu de la pressió arterial i l'excreció d'albúmina urinària mitjançant la regulació de NOX i l'activació de NF-κB. Un altre estudi també va demostrar que la deficiència de SOD2 agreuja la inflamació intersticial i accelera la glomeruloesclerosi, la lesió tubulointersticial i la hipertensió sensible a la sal, especialment en ratolins d'edat avançada. El mecanisme proposat per aquests autors per a la funció microvascular deteriorada és que la deficiència de SOD2 augmenta O2--nivella i altera el flux i la vasodilatació induïda per agonistes a les artèries mesentèriques aïllades.
Excés d'O mitocondrial2- la producció i la disfunció mitocondrial associada s'associen a la patogènesi de la nefropatia diabètica. Diversos experiments han reportat una activitat reduïda de SOD2 en models animals de nefropatia diabètica tipus 1 i tipus 2. En canvi, altres estudis no van informar de cap diferència significativa en l'expressió de SOD2 entre ratolins diabètics i control. Dugan et al. van trobar un augment de la ROS renal en ratolins diabètics amb deficiència de SOD2-, però no van trobar cap evidència d'augment de la proteinúria o l'expansió de l'estroma tilacoide. Per tant, el paper de SOD2 en la nefropatia diabètica és controvertit i es necessiten estudis addicionals per determinar el mecanisme de l'activitat de SOD2 en la nefropatia diabètica.
Igual que amb SOD1 i SOD2, diversos estudis han utilitzat models animals eliminadors de SOD3 per demostrar el paper de SOD3 en la protecció o acceleració de la lesió renal en resposta a l'estrès oxidatiu. després del tall de l'artèria renal en ratolins eliminadors de SOD3, el tractament amb Ang II condueix a un augment de la pressió arterial i indueix una disfunció endotelial, i el tractament recombinant de SOD3 redueix selectivament els ratolins eliminadors de SOD3 hipertensos [44 pressió arterial]. Un altre estudi va informar que SOD3 es localitza predominantment al túbul proximal i es co-localitza amb l'eritropoietina (EPO). En comparació amb els animals de control, els ratolins eliminadors de SOD3 exposats a la hipòxia van mostrar un augment menor dels nivells d'EPO i una menor acumulació de factor induïble per la hipòxia de translocació nuclear (HIF)-1. D'acord amb aquesta troballa, la supressió de SOD3 va retardar la recuperació del flux sanguini renal després d'una isquèmia renal i va augmentar significativament la necrosi tubular i la formació de motlles tubulars després de la reperfusió. la glomerulosclerosi segmentària (FSGS), una troballa associada a la via de senyalització de NOX2 i -catenina es va associar amb la regulació de les vies de senyalització de NOX2 i -catenina. Així, SOD3 té un paper crucial en la protecció renal en una varietat de malalties renals.

Herba Cistanche
Per avaluar el paper de les isoformes SOD en la nefropatia diabètica, Fijuta et al. va avaluar l'activitat de SOD i l'expressió de la isoforme de SOD al ronyó d'un model de ratolí diabètic i va trobar que SOD1 i SOD3 estaven regulats a la baixa en els ronyons diabètics, però SOD2 no. El mateix grup va informar d'utilitzar ratolins diabètics SOD1- i sod3-knockout per confirmar el paper únic de les isoformes SOD en la nefropatia diabètica. Van concloure que en els ratolins diabètics C57BL/6-Akita, la deficiència de SOD1, però no la deficiència de SOD3, augmenta l'O2 - renal i causa una lesió renal significativa, i que la SOD1 té un paper més destacat que la SOD3 en la patogènesi dels diabètics. nefropatia. Tanmateix, estudis recents han informat d'un paper independent de SOD3 en la protecció contra la nefropatia diabètica. El nostre estudi va demostrar que l'expressió de SOD3 a les regions glomerulars i tubulars de ratolins db/db va augmentar significativament després de la suplementació de SOD3 humana recombinant. En models animals de nefropatia diabètica tipus 1 i tipus 2, la suplementació de SOD3 humana recombinant va millorar l'expressió de SOD3 mitjançant la inhibició de la fosforilació de ROS i la cinasa regulada per senyal extracel·lular (ERK) 1/2 o el proliferador de proteïna quinasa-peroxisome activat amb 5' intrarrenal. -activació del coactivador del receptor (PGC)-1 -factor nuclear eritroide 2-activació del factor relacionat (Nrf)2 de les vies de senyalització per millorar la nefropatia diabètica. Per tant, es necessiten més experiments per dilucidar el paper independent de SOD3 en la protecció de la nefropatia diabètica.
2. Catalasa i Malaltia Renal
La CAT és una proteïna homotetramèrica que conté hem de 240 kDa situada principalment al peroxisoma i abundantment present al fetge, pulmó i ronyó. Al ronyó, la CAT es distribueix principalment al citoplasma dels túbuls proximals de l'escorça paramediana i s'expressa menys en els túbuls proximals de l'escorça superficial. D'altra banda, la CAT no està present als glomèruls, túbuls distals, col·laterals de Hench o conductes col·lectors. La deficiència de CAT condueix a la sobreexpressió de ROS mitocondrial i dany mitocondrial funcional. CAT redueix l'H2O2 produït per SOD a oxigen i aigua. Tot i que la CAT és eficient per reduir l'H2O2, el seu paper en la regulació de l'H2O2 pot no ser central, ja que es troba principalment al peroxisoma.
![]()
S'ha informat que la deficiència de CAT augmenta la fibrosi tubulointersticial i els productes de peroxidació lipídica de lesions tubulointersticials en ratolins UUO. Kobayashi et al. va demostrar que la CAT redueix la funció renal i accelera la fibrosi renal progressiva regulant la transició epitelial-mesenquimal dels ronyons restants en 5/6 ratolins nefrectomitzats. A més, en comparació amb els ratolins de tipus salvatge, els ratolins tractats amb adriamicina amb pèrdua de sang van produir proteinúria severa, glomeruloesclerosi accelerada i fibrosi tubulointersticial i augment de l'acumulació de peroxidació lipídica.
En la nefropatia diabètica, la sobreexpressió de CAT específica del túbul proximal en ratolins diabètics tractats amb STZ i ratolins db/db va inhibir la generació de ROS renal i la fibrosi intersticial tubular i va atenuar l'angiotensinogen, p53 i la proteïna x associada a Bcl-2-pro-apoptòtica (BAX). ) Expressió gènica. D'acord amb aquests estudis, la sobreexpressió de CAT en ratolins Akita va reduir significativament la pressió arterial sistòlica regulant el sistema renina-angiotensina intrarenal (RAS), millorant l'enzim convertidor d'angiotensina (ACE) 2, inhibint l'expressió de l'ACE i angiotensinogen o activant el factor nuclear eritroide. 2-via de senyalització relacionada amb el factor 2 (Nrf2)-hemoxigenasa (HO)-1. Godin et al. van utilitzar ratolins transgènics CAT i/o angiotensinogen específics per als túbuls proximals per confirmar l'associació de l'acció de CAT i RAS intrarenal en el desenvolupament d'hipertensió i lesió renal. Un altre investigador també va informar que la deficiència de CAT accelera la nefropatia diabètica perjudicant la biogènesi del peroxisome/mitocondrial i l'oxidació d'àcids grassos. Així, la CAT endògena té un paper protector important en la nefropatia diabètica mitjançant la regulació del metabolisme del RAS intrarenal i dels peroxisomes i reduint l'estrès oxidatiu.
3. Glutatió Peroxidasa i Malalties Renals
Un altre H2O2 carronyador, GPx, converteix peròxids i OH- en substàncies no tòxiques oxidant el glutatió reduït (GSH) a disulfur de glutatió (GSSG), que després es redueix a glutatió per la glutatió reductasa mitjançant NADPH. GPx fa sinergia amb CAT per descompondre H2O2a H2O i oxida el glutatió, que després es redueix per la glutatió reductasa. GPx requereix GSH com a donant d'hidrogen per catabolitzar H2O2a l'aigua i l'oxigen i requereix seleni (Se) com a cofactor per participar en la reacció amb peròxids.
El GPx és una proteïna tetramèrica en la qual cada monòmer conté un àtom de Se al lloc catalític. Cada monòmer conté selenocisteïna, on el sofre de la cisteïna ha estat substituït per seleni (R-SeH). Al llarg del cicle catalític, el selenol (proteïna Se-) reacciona amb peròxid d'hidrogen (H2O2o peròxid d'hidrogen lipídic, LOOH) per produir selenita (proteïna-SeOH). L'àcid seleniós regenera el selenol mitjançant dos GSH, que finalment s'oxiden a GSSG i LOOH. LOOH es redueix a l'alcohol lipídic corresponent (LOH).

Fins ara, s'han identificat vuit GPx diferents en mamífers; tanmateix, només cinc isoformes contenen selenocisteïna i requereixen l'ús de glutatió com a cofactor reductor per catalitzar la reducció de H2O2 i LOOH (GPx 1-4 i 6). Al ronyó, es troben grans quantitats de GPx als túbuls proximals i distals i a les cèl·lules musculars llises de les artèries renals. entre les isoformes GPx, GPx1 i GPx4 s'expressen principalment en podòcits i cèl·lules tilacoides; GPx3 es produeix a la membrana basal dels túbuls proximal i distal de l'escorça renal; GPx2 i GPx5 no es detecten al ronyó. GPx1, el gen identificat més primerenc, és l'alta expressió, i el seu paper en la reducció de l'estrès oxidatiu s'ha demostrat àmpliament. GPx1 es troba principalment als ronyons normals i representa el 96 per cent de l'activitat renal de GPx. Esposito et al. va demostrar que GPx1 s'expressa abundantment als mitocondris de l'escorça renal i que la deficiència de GPx1 redueix el pes corporal i agreuja una disminució endògena i depenent de l'edat de la funció cel·lular global. Així, es creu que la regulació de la GPx1 renal té un paper important en la protecció del ronyó de l'estrès oxidatiu.

Extracte de Cistanche
Diversos estudis anteriors han avaluat els efectes nefroprotectors de GPx1 en la malaltia renal. La inhibició del gen GPx1 exacerba l'AKI induïda per la cocaïna mitjançant la inhibició de la via de senyalització de la fosfoinosítid cinasa (PI3K)-Akt per activar el receptor de l'angiotensina II tipus 1 (AT1R). A més, GPx1 La sobreexpressió millora l'estrès oxidatiu i les ROS mitocondrials en ratolins envellits atenuant la glomerulosclerosi [74]. En la nefropatia diabètica, Chiu et al. va informar que els nivells plasmàtics i urinaris de GPx eren significativament més baixos en pacients amb glomeruloesclerosi diabètica que en pacients sense glomerulosclerosi i que l'expressió de GPx glomerular era menor en rates diabétiques que en rates control normal. Tanmateix, els ratolins diabètics amb deficiència de GPx1-exhibeixen nivells similars de dany oxidatiu, dany glomerular i fibrosi renal com els ratolins diabètics control, i la deficiència de GPx1 no es va compensar de manera endògena per augments de CAT o altres isoformes de GPx durant les primeres etapes de la diabetis. nefropatia. L'activitat de GPx millorada i la carboxilació de GPx no van anar acompanyades d'una expressió augmentada de GPx als ronyons de ratolins diabètics joves. L'expressió i l'activitat de GPx1 i GPx4 tampoc es van diferenciar en els ronyons de ratolins diabètics i no diabètics. En canvi, Chew et al. va demostrar que la deficiència de GPx1 augmentava la proteinúria en ratolins diabètics ApoE/GPx1 doble knockout, que es va associar amb l'augment de l'expansió de la matriu tilacoide glomerular i la regulació positiva dels mediadors de la inflamació i la fibrosi. Per tant, l'efecte nefroprotector de GPx1 en la nefropatia diabètica segueix sent incert.
GPx3 és una selenoproteïna antioxidant extracel·lular, també coneguda com a GPx de plasma. GPx3 es sintetitza principalment a la llum externa de la base renal i s'uneix a la membrana basal de les cèl·lules epitelials corticals renals. GPx3 també s'uneix a la membrana basal de les cèl·lules epitelials extrarenals del tracte gastrointestinal, el pulmó i l'epidídim a través del torrent sanguini. Aquestes troballes suggereixen que la deficiència de GPx3 causada per una lesió renal pot afectar els òrgans distals. En un model d'ERC induïda quirúrgicament, la deficiència de GPx3 redueix significativament la supervivència i promou la disfunció ventricular esquerre, ja que l'acumulació de ROS agreuja la senyalització inflamatòria i l'activació plaquetària. Així, GPx3 pot tenir un paper important en la diafonia entre el ronyó i altres òrgans.
Recentment, s'ha informat que la ferroptosi, una mort cel·lular programada depenent del ferro caracteritzada per l'acumulació d'hidroperòxids lipídics a nivells letals, està implicada en la fisiopatologia de diverses malalties renals. La GPx4 és l'enzim principal que bloqueja la ferroptosi i els inhibidors de GPx4 indueixen ferroptosi. la mort cel·lular mitjançant la unió i la inactivació de GPx4. La deficiència de GPx4 també agreuja l'AKI augmentant el LOOH intracel·lular i la promoció de la mort cel·lular que causa ferro agreuja l'AKI; la lipoestatina-1 prevé la lesió renal induïda per l'esgotament de GPx4. Un estudi recent va mostrar nivells significativament elevats d'acil-coenzim A sintasa membre de la família de cadena llarga 4 (ACSL4) i nivells significativament reduïts de GPx4 en ratolins diabètics, i aquestes troballes suggereixen que la flacidesa del ferro està implicada en la patogènesi de la nefropatia diabètica [85] . Fins ara, no hi ha hagut cap associació entre GPx2 i GPx5 i la malaltia renal.
Referències
1. Sies, H. L'estrès oxidatiu: un concepte en biologia i medicina redox. Redox Biol. 2015, 4, 180–183.
2. Murphy, MP Com els mitocondris produeixen espècies reactives d'oxigen. Bioquímica. J. 2009, 417, 1–13.
3. Xu, N.; Jiang, S.; Persson, PB; Persson, EAG; Lai, EY; Patzak, A. Espècies reactives d'oxigen en la funció vascular renal. Acta Physiol. 2020, 229, e13477.
4. Wang, Y.; Branicky, R.; Noë, A.; Hekimi, S. Superoxide Dismutases: Dual Roles in Controlling ROS Dany and Regulating ROS Signaling. J. Cell Biol. 2018, 217, 1915–1928.
5. Vés, YM; Jones, DP Compartimentació redox en cèl·lules eucariotes. Biochim. Biofísica. Acta 2008, 1780, 1273–1290.
6. Matés, JM; Pérez-Gómez, C.; Núñez de Castro, I. Enzims antioxidants i malalties humanes. Clin. Bioquímica. 1999, 32, 595–603.
7. Espinosa-Diez, C.; Miguel, V.; Mennerich, D.; Kietzmann, T.; Sánchez-Pérez, P.; Cadenas, S.; Lamas, S. Respostes antioxidants i ajustos cel·lulars a l'estrès oxidatiu. Redox Biol. 2015, 6, 183–197.
8. Sharma, K. Obesitat i malaltia renal diabètica: paper de l'estrès oxidant i equilibri redox. Antiòxid. Senyal redox. 2016, 25, 208–216.
9. Dennis, JM; Witting, PK paper protector dels antioxidants en la malaltia renal aguda. Nutrients 2017, 9, 718.
10. Irazabal, MV; Torres, VE Espècies reactives d'oxigen i senyalització redox en la malaltia renal crònica. Cel·les 2020, 9, 1342.
11. Ratliff, BB; Abdulmahdi, W.; Pawar, R.; Wolin, MS Mecanismes oxidants en lesions i malalties renals. Antiòxid. Senyal redox. 2016, 25, 119–146.
12. Dia, BJ Catalytic Antioxidants: A Radical Approach to New Therapeutics. Drogues Discov. Avui 2004, 9, 557–566.
13. Mirończuk-Chodakowska, I.; Witkowska, AM; Zujko, ME Antioxidants endògens no enzimàtics en el cos humà. Adv. Med. Ciència. 2018, 63, 68–78.
14. Pisoschi, AM; Pop, A. El paper dels antioxidants en la química de l'estrès oxidatiu: una revisió. Eur. J. Med. Chem. 2015, 97, 55–74.
15. Rouco, L.; González-Noya, AM; Pedrido, R.; Maneiro, M. Perseguint l'elixir de la vida: efectes antioxidants in vivo dels complexos de manganosalen. Antioxidants 2020, 9, 727.
16. Zelko, IN; Mariani, TJ; Folz, RJ Família multigènica de la superòxid dismutasa: una comparació de les estructures, evolució i expressió dels gens CuZn-SOD (SOD1), Mn-SOD (SOD2) i EC-SOD (SOD3). Radic Lliure. Biol. Med. 2002, 33, 337–349.
17. Marklund, SL Superòxid dismutasa extracel·lular i altres isoenzims de superòxid dismutasa en teixits de nou espècies de mamífers. Bioquímica. J. 1984, 222, 649–655.
18. Van Remmen, H.; Salvador, C.; Yang, H.; Huang, TT; Epstein, CJ; Richardson, A. Caracterització de l'estat antioxidant del ratolí eliminatori de superòxid dismutasa de manganès heterozigot. Arc. Bioquímica. Biofísica. 1999, 363, 91–97.
19. Schieber, M.; Chandel, NS Funció ROS en senyalització redox i estrès oxidatiu. Curr. Biol. 2014, 24, R453–R462.
20. Brzoska, K.; Sochanowicz, B.; Siomek, A.; Olinski, R.; Kruszewski, M. Alteracions en l'expressió de gens relacionats amb la senyalització de NFkappaB en fetge i ronyó de ratolins amb deficiència de CuZnSOD. Mol. Cèl·lula. Bioquímica. 2011, 353, 151–157.
21. Siomek, A.; Brzoska, K.; Sochanowicz, B.; Gackowski, D.; Rozalski, R.; Foksinski, M.; Zarakowska, E.; Szpila, A.; Guz, J.; Bartlomiejczyk, T.; et al. La deficiència de Cu, Zn-superòxid Dismutasa en ratolins condueix a un augment específic d'òrgans de l'ADN danyat oxidativament i l'activitat de la proteïna NF-kappaB1. Acta Biochim. Pol. 2010, 57, 577–583.
22. Yamanobe, T.; Okada, F.; Iuchi, Y.; Onuma, K.; Tomita, Y.; Fujii, J. Deteriorament de la insuficiència renal aguda induïda per isquèmia/reperfusió en ratolins deficients SOD1-. Radic Lliure. Res. 2007, 41, 200–207.
23. Yin, M.; Wheeler, MD; Connor, HD; Zhong, Z.; Bunzendahl, H.; Dikalova, A.; Samulski, RJ; Schoonhoven, R.; Mason, RP; Swenberg, JA; et al. El gen Cu/Zn-Superòxid Dismutasa atenua la lesió d'isquèmia-reperfusió al ronyó de rata. Melmelada. Soc. Nefrol. 2001, 12, 2691–2700.
24. Carlström, M.; Brown, RD; Sällström, J.; Larsson, E.; Zilmer, M.; Zabihi, S.; Eriksson, UJ; Persson, AE La deficiència de SOD1 causa sensibilitat a la sal i agreuja la hipertensió en la hidronefrosi. Am. J. Physiol. Regul. Integr. Comp. Physiol. 2009, 297, R82–R92.
25. Carlström, M.; Lai, EY; Ma, Z.; Steege, A.; Patzak, A.; Eriksson, UJ; Lundberg, JO; Wilcox, CS; Persson, AE La superòxid dismutasa 1 limita la remodelació microvascular renal i atenua les respostes de l'arteriola i la pressió arterial a l'angiotensina II mitjançant la modulació de la biodisponibilitat de l'òxid nítric. Hipertensió 2010, 56, 907–913.
26. Cepas, V.; Collino, M.; Mayo, JC; Sainz, RM Senyalització Redox i productes finals de glicació avançada (AGE) en malalties relacionades amb la dieta. Antioxidants 2020, 9, 142.
27. DeRubertis, FR; Craven, PA; Melhem, MF; Salah, EM Atenuació de lesions renals en ratolins db/db que sobreexpressen la superòxid dismutasa: evidència de la reducció de la interacció superòxid-òxid nítric. Diabetis 2004, 53, 762–768.
28. Craven, PA; Melhem, MF; Phillips, SL; DeRubertis, FR La sobreexpressió de Cu2 plus /Zn2 més superòxid dismutasa protegeix contra la lesió glomerular diabètica precoç en ratolins transgènics. Diabetis 2001, 50, 2114–2125.
29. Kitada, M.; Xu, J.; Ogura, Y.; Monno, I.; Koya, D. Disfunció de la superòxid dismutasa de manganès i la patogènesi de la malaltia renal. Davant. Physiol. 2020, 11, 755.
30. Parajuli, N.; Marina, A.; Simmons, S.; Saba, H.; Mitchell, T.; Shimizu, T.; Shirasawa, T.; Macmillan-Crow, LA Generació i caracterització d'un nou ratolí Knockout de superòxid dismutasa de manganès específic del ronyó. Radic Lliure. Biol. Med. 2011, 51, 406–416.
31. Parajuli, N.; MacMillan-Crow, LA Paper de la reducció de la superòxid dismutasa de manganès en la lesió per isquèmia-reperfusió: un possible desencadenant per a l'autofàgia i la biogènesi mitocondrial? Am. J. Physiol. Physiol renal. 2013, 304, F257–F267.
32. Pisani, A.; Sabbatini, M.; Riccio, E.; Rossano, R.; Andreucci, M.; Capasso, C.; De Luca, V.; Carginale, V.; Bizzarri, M.; Borrelli, A.; et al. Efecte d'una superòxid dismutasa de manganès recombinant en la prevenció de la lesió renal aguda induïda pel contrast. Clin. Exp. Nefrol. 2014, 18, 424–431.
33. Jin, K.; Vaziri, ND La hipertensió sensible a la sal en la deficiència de superòxid dismutasa mitocondrial s'associa amb l'estrès oxidatiu intrarenal i la inflamació. Clin. Exp. Nefrol. 2014, 18, 445–452.
34. Rodríguez-Iturbe, B.; Sepassi, L.; Quiroz, Y.; Ni, Z.; Wallace, DC; Vaziri, ND Associació de deficiència de SOD mitocondrial amb hipertensió sensible a la sal i senescència renal accelerada. J. Appl. Physiol. 2007, 102, 255–260.
35. Yan, C.; Huang, A.; Wu, Z.; Kaminski, PM; Wolin, MS; Hintze, TH; Kaley, G.; Sun, D. L'augment del superòxid condueix a una disminució de la dilatació induïda pel flux en les artèries de resistència de ratolins amb deficiència de Mn-SOD. Am. J. Physiol. Circ del cor. Physiol. 2005, 288, H2225–H2231.
36. Forbes, JM; Thorburn, DR Disfunció mitocondrial en la malaltia renal diabètica. Nat. Reverent Nephrol. 2018, 14, 291–312.
37. Sharma, K. Mitocondrial Dysfunction in the Diabetic Kidney. Adv. Exp. Med. Biol. 2017, 982, 553–562.
38. Li, C.; Matavelli, LC; Akhtar, S.; Siragy, el receptor HM (pro)renina contribueix a la disfunció dels mitocondris renals, l'apoptosi i la fibrosi en ratolins diabètics. Ciència. Rep. 2019, 9, 11667.
39. Kim, MY; Lim, JH; Youn, HH; Hong, YA; Yang, KS; Park, HS; Chung, S.; Ko, SH; Shin, SJ; Choi, BS; et al. El resveratrol prevé la lipotoxicitat renal i inhibeix la glucotoxicitat de les cèl·lules mesangials d'una manera que depèn de l'eix AMPK-SIRT1-PGC1alpha en ratolins db/db. Diabetologia 2013, 56, 204–217.
40. De Cavanagh, EM; Ferder, L.; Toblli, JE; Piotrkowski, B.; Stella, I.; Fraga, CG; Inserra, F. La deterioració mitocondrial renal s'atenua pel bloqueig AT1 en la diabetis tipus I experimental. Am. J. Physiol. Circ del cor. Physiol. 2008, 294, H456–H465.
41. Hong, YA; Lim, JH; Kim, MY; Kim, TW; Kim, Y.; Yang, KS; Park, HS; Choi, SR; Chung, S.; Kim, HW; et al. El fenofibrat millora la lipotoxicitat renal mitjançant l'activació d'AMPK-PGC-1alfa en ratolins db/db. PLoS ONE 2014, 9, e96147.
42. Fujita, H.; Fujishima, H.; Chida, S.; Takahashi, K.; Qi, Z.; Kanetsuna, Y.; Breyer, MD; Harris, RC; Yamada, Y.; Takahashi, T. Reducció de la superòxid dismutasa renal en la nefropatia diabètica progressiva. Melmelada. Soc. Nefrol. 2009, 20, 1303–1313.
43. Dugan, LL; Tu, YH; Ali, SS; Diamond-Stanic, M.; Miyamoto, S.; DeCleves, AE; Andreiev, A.; Quach, T.; Ly, S.; Shekhtman, G.; et al. La desregulació de l'AMPK promou la reducció del superòxid i la funció mitocondrial relacionada amb la diabetis. J. Clin. Invertir. 2013, 123, 4888–4899.
44. Jung, O.; Marklund, SL; Geiger, H.; Pedrazzini, T.; Busse, R.; Brandes, RP La superòxid dismutasa extracel·lular és un determinant important de la biodisponibilitat de l'òxid nítric: evidència in vivo i ex vivo de ratolins amb deficiència d'ecSOD. Circ. Res. 2003, 93, 622–629.
45. Suliman, HB; Ali, M.; Piantadosi, CA La superòxid dismutasa-3 promou l'expressió completa de la resposta de l'EPO a la hipòxia. Sang 2004, 104, 43–50.
46. Schneider, diputat; Sullivan, JC; Wach, PF; Boesen, EI; Yamamoto, T.; Fukai, T.; Harrison, DG; Pollock, DM; Pollock, JS Funció protectora de la superòxid dismutasa extracel·lular en la lesió per isquèmia/reperfusió renal. Ronyó Int. 2010, 78, 374–381.
47. Tan, RJ; Zhou, D.; Xiao, L.; Zhou, L.; Li, Y.; Bastacky, SI; Oury, TD; Liu, Y. La superòxid dismutasa extracel·lular protegeix contra la malaltia renal proteïnúrica. Melmelada. Soc. Nefrol. 2015, 26, 2447–2459.
48. Fujita, H.; Fujishima, H.; Takahashi, K.; Sato, T.; Shimizu, T.; Morii, T.; Shimizu, T.; Shirasawa, T.; Qi, Z.; Breyer, MD; et al. SOD1, però no SOD3, la deficiència accelera la lesió renal diabètica en ratolins diabètics C57BL/6-Ins2(Akita). Metabolisme 2012, 61, 1714–1724.
49. Kuo, CW; Shen, CJ; Tung, YT; Chen, HL; Chen, YH; Chang, WH; Cheng, KC; Yang, SH; Chen, CM La superòxid dismutasa extracel·lular millora la nefropatia diabètica de rata induïda per estreptozotocina mitjançant la inhibició de la senyalització ROS/ERK1/2. Ciència de la vida. 2015, 135, 77–86.
50. Hong, YA; Lim, JH; Kim, MY; Kim, Y.; Park, HS; Kim, HW; Choi, BS; Chang, YS; Kim, HW; Kim, TY; et al. La superòxid dismutasa extracel·lular atenua l'estrès oxidatiu renal mitjançant l'activació de la proteïna cinasa activada per adenosina monofosfat en la nefropatia diabètica. Antiòxid. Senyal redox. 28, 2018, 1543–1561.
51. Ho, YS; Xiong, Y.; Ma, W.; Spector, A.; Els ratolins Ho, DS que no tenen catalasa es desenvolupen normalment, però mostren una sensibilitat diferencial a la lesió del teixit oxidant. J. Biol. Chem. 2004, 279, 32804–32812.
52. Zhou, Z.; Kang, YJ Localització cel·lular i subcel·lular de catalasa al cor de ratolins transgènics. J. Histochem. Citoquímica. 2000, 48, 585–594.
53. Hwang, I.; Lee, J.; Eh, JY; Park, J.; Lee, HB; Ho, YS; Ha, H. La deficiència de catalasa accelera la lesió renal diabètica mitjançant la disfunció peroxisòmica. Diabetis 2012, 61, 728–738.
54. Sunami, R.; Sugiyama, H.; Wang, DH; Kobayashi, M.; Maeshima, Y.; Yamasaki, Y.; Matsuoka, N.; Ogawa, N.; Kira, S.; Makino, H. L'acatalasèmia sensibilitza les cèl·lules epitelials tubulars renals a l'apoptosi i exacerba la fibrosi renal després de l'obstrucció ureteral unilateral. Am. J. Physiol. Physiol renal. 2004, 286, F1030–F1038.
55. Kobayashi, M.; Sugiyama, H.; Wang, DH; Toda, N.; Maeshima, Y.; Yamasaki, Y.; Matsuoka, N.; Yamada, M.; Kira, S.; Makino, H. La deficiència de catalasa fa que els ronyons restants siguin més susceptibles a la lesió del teixit oxidant i la fibrosi renal en ratolins. Ronyó Int. 2005, 68, 1018–1031.
56. Takiue, K.; Sugiyama, H.; Inoue, T.; Morinaga, H.; Kikumoto, Y.; Kitagawa, M.; Kitamura, S.; Maeshima, Y.; Wang, DH; Masuoka, N.; et al. Els ratolins acatalasèmics són lleugerament susceptibles a la nefropatia d'adriamicina i presenten un augment de l'albuminúria i la glomerulosclerosi. BMC Nephrol. 13 i 14 de 2012.
57. Brezniceanu, ML; Liu, F.; Wei, CC; Tran, S.; Sachetelli, S.; Zhang, SL; Guo, DF; Filep, JG; Ingelfinger, JR; Chan, JS La sobreexpressió de catalasa atenua l'expressió i l'apoptosi de l'angiotensinogen en ratolins diabètics. Ronyó Int. 2007, 71, 912–923.
58. Brezniceanu, ML; Liu, F.; Wei, CC; Chénier, I.; Godin, N.; Zhang, SL; Filep, JG; Ingelfinger, JR; Chan, JS Atenuació de la fibrosi intersticial i l'apoptosi tubular en ratolins transgènics db/db que sobreexpressen la catalasa en cèl·lules tubulars proximals renals. Diabetis 2008, 57, 451–459.
59. Shi, Y.; Lo, CS; Chenier, I.; Maachi, H.; Filep, JG; Ingelfinger, JR; Zhang, SL; Chan, JS La sobreexpressió de la catalasa prevé la hipertensió i la fibrosi tubulointersticial i la normalització de l'expressió de l'enzim convertidor d'angiotensina renal-2 en ratolins Akita. Am. J. Physiol. Physiol renal. 2013, 304, F1335–F1346.
60. Abdo, S.; Shi, Y.; Otoukesh, A.; Ghosh, A.; Lo, CS; Chenier, I.; Filep, JG; Ingelfinger, JR; Zhang, SL; Chan, JS La sobreexpressió de la catalasa impedeix el factor nuclear eritroide 2-Factor 2 relacionat amb l'estimulació de l'expressió gènica de l'angiotensinogen renal, la hipertensió i la lesió renal en ratolins diabètics. Diabetis 2014, 63, 3483–3496.
61. Godin, N.; Liu, F.; Lau, GJ; Brezniceanu, ML; Chénier, I.; Filep, JG; Ingelfinger, JR; Zhang, SL; Chan, JS La sobreexpressió de catalasa prevé la hipertensió i l'apoptosi tubular en ratolins transgènics d'angiotensinogen. Ronyó Int. 2010, 77, 1086–1097.
62. Flohe, L.; Günzler, WA; Schock, HH Glutatió peroxidasa: un selenoenzim. FEBS Lett. 1973, 32, 132–134.
63. Schafer, FQ; Buettner, GR Entorn redox de la cèl·lula vist a través de l'estat redox de la parella disulfur de glutatió/glutatió. Radic Lliure. Biol. Med. 2001, 30, 1191–1212.
64. Lei, XG; Cheng, WH Nous papers per a un vell selenoenzim: evidència de ratolins nuls i sobreexpressants de glutatió peroxidasa-1. J. Nutr. 2005, 135, 2295–2298.
65. Dia, BJ Catalasa i Glutatió Peroxidasa Mimics. Bioquímica. Pharmacol. 2009, 77, 285–296.
66. Behne, D.; Kyriakopoulos, A. Proteïnes que contenen seleni de mamífers. Ann. Rev. Nutr. 2001, 21, 453–473.
67. Musa, KE; Oberley, TD; Sempf, JM; Oberley, LW Immunolocalització d'enzims antioxidants en ronyó de hàmster adults. Histoquímica. J. 1994, 26, 734–753.
68. Wiedenmann, T.; Dietrich, N.; Fleming, T.; Altamura, S.; Deelman, LE; Henning, RH; Muckenthaler, MU; Nawroth, PP; Hammes, HP; Wagner, AH; et al. Modulació de l'activitat de la glutatió peroxidasa per carbonilació depenent de l'edat en glomèruls de ratolins diabètics. J. Diabetes Complicat. 2018, 32, 130–138.
69. Olson, GE; Whitin, JC; Hill, KE; Winfrey, VP; Motley, Alaska; Austin, LM; Deal, J.; Cohen, HJ; Burk, RF extracel·lular glutatió peroxidasa (Gpx3) s'uneix específicament a les membranes del soterrani de les cèl·lules del túbul de l'escorça renal del ratolí. Am. J. Physiol. Physiol renal. 2010, 298, F1244–F1253.
70. De Haan, JB; Bladier, C.; Griffiths, P.; Kelner, M.; O'Shea, RD; Cheung, NS; Bronson, RT; Silvestro, MJ; Salvatge, S.; Zheng, SS; et al. Els ratolins amb una mutació nul·la homozigota per a la glutatió peroxidasa més abundant, Gpx1, mostren una major susceptibilitat als agents que indueixen l'estrès oxidatiu paraquat i peròxid d'hidrogen. J. Biol. Chem. 1998, 273, 22528–22536.
71. De Haan, JB; Stefanovic, N.; Nikolic-Paterson, D.; Scurr, LL; Croft, KD; Mori, TA; Hertzog, P.; Kola, I.; Atkins, RC; Tesch, GH L'expressió renal de la glutatió peroxidasa-1 no és protectora contra la nefropatia diabètica induïda per estreptozotocina. Am. J. Physiol. Physiol renal. 2005, 289, F544–F551.
72. Esposito, LA; Kokoszka, JE; Waymire, KG; Cottrell, B.; MacGregor, GR; Wallace, DC Estrès oxidatiu mitocondrial en ratolins que no tenen el gen de la glutatió peroxidasa-1. Radic Lliure. Biol. Med. 2000, 28, 754–766.
73. Mai, HN; Chung, YH; Shin, EJ; Kim, DJ; Jeong, JH; Nguyen, TT; Nam, Y.; Lee, YJ; No, SY; Yu, DY; et al. L'esgotament genètic de la glutatió peroxidasa-1 potencia la nefrotoxicitat induïda per múltiples dosis de cocaïna mitjançant l'activació del receptor AT1 de l'angiotensina II. Radic Lliure. Res. 2016, 50, 467–483.
74. Chu, Y.; Lan, RS; Huang, R.; Feng, H.; Kumar, R.; Dayal, S.; Chan, KS; Dai, DF Glutatió Peroxidasa-1 La sobreexpressió redueix l'estrès oxidatiu i millora la patologia i la remodelació del proteoma als ronyons de ratolins vells. Aging Cell 2020, 19, e13154.
75. Chiu, YW; Kuo, MC; Kuo, HT; Chang, JM; Guh, JY; Lai, YH; Chen, HC Alteracions dels nivells glomerulars i extracel·lulars de la glutatió peroxidasa en pacients i rates experimentals amb nefropatia diabètica. J. Lab. Clin. Med. 2005, 145, 181–186.
76. Mastegar, P.; Yuen, DY; Stefanovic, N.; Pete, J.; Coughlan, MT; Jandeleit-Dahm, KA; Tomàs, MC; Rosenfeldt, F.; Cooper, ME; de Haan, JB Efectes antiateroscleròtics i renoprotectors d'Ebselen a l'apolipoproteïna diabètica E/GPx1-ratolí de doble eliminació. Diabetis 2010, 59, 3198–3207.
77. Ottaviano, FG; Tang, SS; Handy, DE; Loscalzo, J. Regulació de l'antioxidant extracel·lular de selenoproteïna plasmàtica glutatió peroxidasa (GPx-3) en cèl·lules de mamífers. Mol. Cèl·lula. Bioquímica. 2009, 327, 111–126.
78. Burk, RF; Olson, GE; Winfrey, VP; Hill, KE; Yin, D. La glutatió peroxidasa-3 produïda pel ronyó s'uneix a una població de membranes basals del tracte gastrointestinal i d'altres teixits. Am. J. Physiol. Test gastrointestinal. Physiol hepàtic. 2011, 301, G32–G38.
79. Pang, P.; Abbott, M.; Abdi, M.; Fucci, QA; Chauhan, N.; Mistri, M.; Proctor, B.; Chin, M.; Wang, B.; Yin, W.; et al. El model preclínic de la deficiència severa de glutatió peroxidasa-3 i la malaltia renal crònica dóna lloc a la trombosi de l'artèria coronària i la funció ventricular esquerra deprimida. Nefrol. Marqueu. Trasplantament. 2018, 33, 923–934.
80. Martín-Sanchez, D.; Fontecha-Barriuso, M.; Martínez-Moreno, JM; Ramos, AM; Sánchez-Niño, MD; Guerrero-Hue, M.; Moreno, JA; Ortiz, A.; Sanz, AB Ferroptosi i malaltia renal. Nefrologia 2020, 40, 384–394.
81. Hu, Z.; Zhang, H.; Yang, SK; Wu, X.; Ell, D.; Cao, K.; Zhang, W. Paper emergent de la ferroptosi en la lesió renal aguda. Òxid. Med. Cèl·lula. Longev. 2019, 2019, 8010614.
82. Belavgeni, A.; Meyer, C.; Stumpf, J.; Hugo, C.; Linkermann, A. Ferroptosi i necroptosi al ronyó. Cell Chem. Biol. 2020, 27, 448–462.
83. Yang, WS; SriRamaratnam, R.; Welsch, ME; Shimada, K.; Skouta, R.; Viswanathan, VS; Cheah, JH; Clemons, PA; Shamji, AF; Clish, CB; et al. Regulació de la mort de cèl·lules canceroses ferroptòtiques per GPX4. Cèl·lula 2014, 156, 317–331.
84. Friedmann Angeli, JP; Schneider, M.; Proneth, B.; Tyurina, YY; Tyurin, VA; Hammond, VJ; Herbach, N.; Aichler, M.; Walch, A.; Eggenhofer, E.; et al. La inactivació del regulador de ferroptosi Gpx4 desencadena insuficiència renal aguda en ratolins. Nat. Biol cel·lular. 2014, 16, 1180–1191.
85. Wang, Y.; Bi, R.; Quan, F.; Cao, Q.; Lin, Y.; Yue, C.; Cui, X.; Yang, H.; Gao, X.; Zhang, D. Ferroptosi implica la mort de cèl·lules tubulars renals en la nefropatia diabètica. Eur. J. Pharmacol. 2020, 888, 173574.
Yu Ah Hong1i Cheol Whee Park1,2,
1 Departament de Medicina Interna, Facultat de Medicina, Universitat Catòlica de Corea, Seül 06591, Corea; amorfati@catholic.ac.kr
2 Institut per a l'envelliment i les malalties metabòliques, Facultat de Medicina, Universitat Catòlica de Corea, Seül 06591, Corea





