Part 1: ceramida-1-fosfat com a regulador potencial de la segona bomba de sodi dels túbuls proximals del ronyó mitjançant l'activació de diferents vies de proteïna quinasa d'una manera jeràrquica
Jul 27, 2022
Per a més informació. contactetina.xiang@wecistanche.com
Resum: Túbuls proximals del ronyósón un segment clau en la reabsorció de soluts i aigua de l'ultrafiltrat glomerular, un procés essencial per mantenir l'homeòstasi en els compartiments de fluids corporals. L'abundant contingut de Na plus en el líquid extracel·lular determina la seva importància en la regulació del volum del líquid extracel·lular, que és particularment important per a diferents processos fisiològics, inclòs el control de la pressió arterial. Les membranes basolaterals de les cèl·lules del túbul proximal tenen el Nat-ATPasa clàssic Na més + K més -ATPasa i la Nat-ATPasa insensible a la ouabaïna, K més insensible i sensible a la furosemida, que participen en la reabsorció activa de Na més. Aquí, mostrem que les concentracions nanomolars de ceramida -1 fosfat (C1P), un esfingolípid bioactiu derivat de membranes biològiques de diferents vies metabòliques, promouen un fort efecte inhibidor sobre l'activitat de Nat-ATPasa (C1Pso ≈10 M), donant lloc a a una inhibició del 72 per cent de la segona bomba de sodi a les membranes basolaterals. La ceramida-1-fosfat modula directament la proteïna cinasa A i la proteïna cinasa C, que se sap que estan implicades en la modulació dels transportadors d'ions, inclosa la Na renal més -ATPasa. Per contra, no vam observar cap efecte sobre la Na més K més -ATPasa fins i tot a un ampli rang de concentració de ClP. L'efecte significatiu de la ceramida-1-fosfat va revelar un nou potent modulador fisiològic i fisiopatològic per a la Na més -ATPasa, que participa en la xarxa reguladora que inclou glicerol i esfingolípids presents a les membranes basolaterals decèl·lules del túbul renal.
Paraules clau: Na més -ATPasa; ceramida-1 fosfat; ronyó; túbuls proximals; membranes basolaterals; esfingolípids

Feu clic aquí per conèixer els beneficis de l'extracte de cistanche tubulosa
1. Introducció
Des dels estudis inicials dels anys 90, els esfingolípids bioactius han sorgit com una classe important de molècules de senyalització cel·lular, que es mobilitzen ràpidament després de l'estimulació cel·lular i poden desencadenar diferents cascades de senyalització cel·lular que culminen amb respostes cel·lulars específiques [1,2].
Entre els esfingolípids bioactius, hi ha un interès creixent per l'esfingosina (Sph), l'esfingosina-1-fosfat (S1P), la ceramida (Cer) i la ceramida-1-fosfat (C1P), que són els relacionats amb el -anomenat "reòstat esfingolípid" implicat en efectes oposats com la supervivència cel·lular o la mort, segons l'interruptor adequat [3,4].
Els diferents esfingolípids bioactius implicats en aquestes cascades de senyalització es poden mobilitzar per síntesi de novo o per activació directa del precursor de fosfolípids de membrana, principalment l'esfingomielina (SM)[5-7]. Diferents informes mostren que un pas inicial per a la senyalització cel·lular és l'activació de les esfingomielinases (casos), que escinden SM, donant lloc a la formació de Cer, que pot estar directament implicada en el muntatge de microdominis de membrana estructural i funcionalment complexos anomenats plataformes [{ {1}}] o com a substrat per a una ceramida quinasa (CerK), que condueix a la formació de C1P [11-13]. En un pas posterior, el ClP es pot desfosforilar a Cer, que es converteix en Sph per l'acció de les ceramidases [4,7,14,15]. Aquesta via que comença a SM condueix a la formació de dos mediadors importants que són substrats per a les cinases lipídiques, donant lloc a derivats fosforilats amb diferents capacitats [1,16,17]. En primer lloc, es va pensar que la fosforilació dels mediadors lipídics estava relacionada amb la terminació del senyal. En cas contrari, el progrés en el camp ens va permetre demostrar que els derivats fosforilats, i aquí augmentarem el C1P, poden provocar respostes cel·lulars diferents mitjançant interaccions directes amb dominis hidrofòbics inclosos C1 i C2 que estan presents en diferents possibles socis cel·lulars [{{14] }}], o, actuant mitjançant l'activació de receptors de membrana encara desconeguts, com ja s'ha suggerit [4,23].
En els últims quinze anys, el nostre grup ha estat estudiant la capacitat dels lípids bioactius per modular alguns dels principals transportadors d'ions i altres vies de senyalització cel·lular presents a les membranes basolaterals (BLM) dels túbuls proximals del ronyó[18,24-29] . Aquí, ampliem els nostres esforços per aportar noves idees sobre el paper de C1P dins deteixit renal, amb C1P el lípid bioactiu menys estudiat en l'escenari del reòstat d'esfingolípids, il·lustrant així la necessitat d'identificar molècules / vies diana intracel·lulars i mecanismes intracel·lulars per a ClP, i també descobrir qualsevol interacció amb altres lípids bioactius [30]. La capacitat de Cer i C1P per desencadenar diferents proteïnes quinases, i la llista creixent d'efectors que es mostra modulada per aquests esfingolípids [2,12,31,32] ens va permetre plantejar la hipòtesi que ambdós esfingolípids bioactius també podrien ser responsables de la regulació de Nat transportistes al BLM. Això podria ser particularment interessant no només per la capacitat de les ceràmides que desencadenen proteïnes efectores, com ja ha demostrat el nostre grup [18,33], sinó també per la importància de Cer per al muntatge de basses de membrana i caveolas, així com per membrana gran. microdominis, les anomenades plataformes, que són regions específiques de les membranes plasmàtiques on les molècules de senyalització i els efectors es co-localitzen [8,9,34,35].
Sent el túbul proximal, el segment de nefrona principal anomenat reabsorció de Nat, i amb ClP potencialment disponible i/o reclutat per a aquest nínxol, aquí, explorem l'acció de ClP en diferents quinases que se sap que modulen Nat més K més -ATPasa. i la Nat-ATPasa insensible a la ouabaïna, K*-insensible i sensible a la furosemida (coneguda a partir d'ara com a Nat-ATPasa), estudiant així la regulació d'aquests transportadors de Nat al BLM per ClP i també revelant les cascades de senyalització cel·lular implicades. . A partir dels resultats aquí presentats, aquestes vies descrites implicades en la xarxa reguladora responsable de la reabsorció de Nat poden proporcionar alguns mitjans per al desenvolupament de noves estratègies terapèutiques generalitzades per a diferentsmalalties renalsi també patologies més complexes com la hipertensió.

2. Materials i Mètodes
2.1.Material
Els productes químics generals utilitzats es van obtenir de Sigma Chemical Co. (St. Louis, MO, EUA) Percoll es va obtenir de Pharmacia (Uppsala, Suècia). Es va aplicar el sistema de resines Milli-Q (Millipore Corp., Bedford, MA, EUA) per obtenir aigua desionitzada utilitzada per preparar totes les solucions. *2P; es va obtenir de l'Instituto de Pesquisas Energetics e Nucleares (IPEN, Sao Paulo, Brasil).[y-3P]ATP es va preparar tal com es va descriure anteriorment [36]. El cotxe (del cervell boví), el C1P, la histona H8, el pèptid inhibidor de la subunitat catalítica de PKA 5-22 (PKAi) i l'inhibidor de PKC calfostina C es van comprar a Sigma Chemical Co. (St. Louis, MO, EUA). ). Els reactius eren de la puresa més alta disponible. El sistema ECLIM i les membranes de nitrocel·lulosa (Hybond) es van obtenir de GE Healthcare, (Sao Paulo, Brasil). Els ronyons de porc es van comprar tal com ja s'ha descrit [28], segons la legislació brasilera respectiva.
2.2. Aïllament de les membranes basolaterals (BLM)
Ronyonses van transportar ràpidament en una solució refrigerada (sacarosa 250mM, Hepes-Tris 10mM—pH7,6—EDTA 2mM, PMSFF 1mm i 0,15 mg/mL d'inhibidor de tripsina de soja). Les còrtexs de l'escorça es van eliminar amb cura i es van preparar fraccions de membrana basolateral (BLM) enriquides derivades dels túbuls proximals del ronyó tal com es va descriure anteriorment [37]. Els controls de contaminació amb altres membranes es van dur a terme tal com es va descriure anteriorment [38]. L'activitat de Nat més Kt-ATPasa es va enriquir fins a sis vegades (297,2 ± 1,2 nmol/mg per min) sobre l'homogeneïtat de còrtex inicial. Les alíquotes de BLM es van emmagatzemar en sacarosa 250 mM en N2 líquid.
2.3.Determinació de proteïnes
Els assajos de determinació de proteïnes es van realitzar mitjançant el mètode de fenol Folin [39] amb l'addició d'un 5% de SDS a les mostres utilitzant albúmina sèrica bovina com a estàndard.
2.4.Determinació de les activitats Nat més K més -ATPasa i Nat-ATPasa
Els assajos es van dur a terme en un medi de reacció (1 ml de volum final) que contenia 50mM de tampó de propà Bis-Tris (pH7,4), 5 mM MgClz, 10 mM NaNg, 2{{ 29}} uM Ca4* lliure (0.2mMEGTA, 238.3 uM CaCla) on les fraccions BLM (0.2mg/mL) es van preincubar durant 10 min a 37 graus amb les concentracions de ClP indicades a la xifres, seguida de 10 minuts de sonicació (240 W, 25 kHz, 24-25 grau; Netejador de sonificadors únic). Després, les mostres es van complementar amb 120 mM de KCl i 5 mM d'ATP. Quan s'indica, es van afegir 10 nM de PKAi (5-22 pèptid inhibidor de PKA) o 10 nM de calfostina C (inhibidor de PKC) al medi de preincubació. Després de 20 min, es va afegir 1,5 ml de carbó activat en HCl 0,1 N a cada tub i es va barrejar en un vòrtex per aturar la reacció i després es va centrifugar (2000 rpm). Les alíquotes de 0,5 ml dels sobrenedants es van transferir a nous tubs de vidre i es va determinar la quantitat de Pi alliberada mitjançant un mètode colorimètric [40]. L'activitat de Nat més Kt-ATPasa es va calcular com la diferència entre les activitats mesurades sense i amb ouabaïna 1 mM [35,38]. L'activitat nat-ATPasa es va analitzar mitjançant el mateix medi de reacció per a la determinació de l'activitat Nat més K més -ATPasa amb [y-32 P]ATP com a substrat per a l'ATPasa (108 CPM/tub de reacció). L'activitat Nat-ATPasa es va calcular tal com ja s'ha descrit [38, 41]. Breument, la reacció es va aturar després de 20 min afegint el carbó activat a cada tub, seguit de centrifugació (200 rpm). Les alíquotes de 0, 5 ml dels sobrenedants es van dispensar a tires de paper de filtre i es va determinar el [32P]Pi alliberat mitjançant un recompte de centelleig líquid. L'activitat nat-ATPasa es va determinar com la diferència entre les activitats mesurades sense i amb furosemida 2 mM, en presència de ouabaïna 1 mM.
La concentració de Ca2t lliure per a aquestes determinacions es va calcular mitjançant un programa informàtic que va tenir en compte les diferents espècies implicades en l'equilibri entre EGTA, Ca2 plus , i les diferents formes d'ATP, Mg2 plus , H plus , i K plus [42].
2.5.Determinació de l'activitat de la proteïna quinasa A (PKA).
La histona H8, un substrat general per a les proteïnes quinases, es va utilitzar en l'assaig d'activitat BLM PKA, com ja s'ha descrit [18]. L'activitat de PKA es va calcular com la diferència entre la radioactivitat total associada a les histones en presència o absència de PKAi (10 nM). Es va utilitzar un total de 100 nM d'AMPc com a control positiu per confirmar la presència de PKA a les fraccions BLM.
2.6.Determinació de l'activitat de la proteïna quinasa C(PKC).
Hem utilitzat el mateix mètode descrit per a la determinació de l'activitat de PKA [18], i l'activitat de PKC es va mesurar com la diferència entre la fosforilació d'histones en presència o absència de calfostina C 10 nM (inhibidor de PKC). L'acetat de -12-mirstat-13- de forbol (PMA, 1 pM), un èster de forbol que és un anàleg de DAG, es va utilitzar per confirmar la presència de PKC funcional a les fraccions BLM [35].
2.7.Anàlisi estadística
L'anàlisi estadística es va dur a terme mitjançant la prova ANOVA unidireccional i la prova posterior de Newman-Keuls. La significació estadística es va establir a la p<0.05. data="" were="" analyzed="" using="" the="" graphpad="" prism="" 5.0="">

3 .Resultats
La figura 1 mostra que l'activitat de Nat-ATPasa de BLM es va inhibir significativament per l'augment de les concentracions (en el rang nanomolar) de C1P, amb l'efecte de l'eficàcia fisiològica segons la concentració relativament baixa (c1 nM) que gairebé va abolir l'activitat de Nat-ATPasa. . A causa del nostre interès en la regulació del transport de Nat per C1P, també vam provar la capacitat d'aquest esfingolípid bioactiu en la modulació de la Nat més K*-ATPasa. Com es mostra a la figura 2, C1P va ser ineficaç per modular l'activitat de Nat més Kt-ATPasa, fins i tot a les concentracions més altes provades.
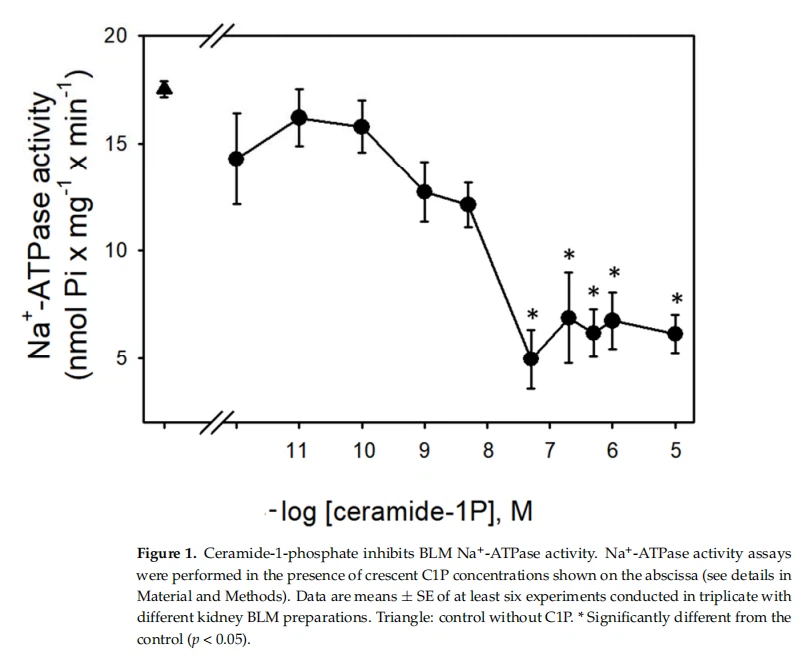
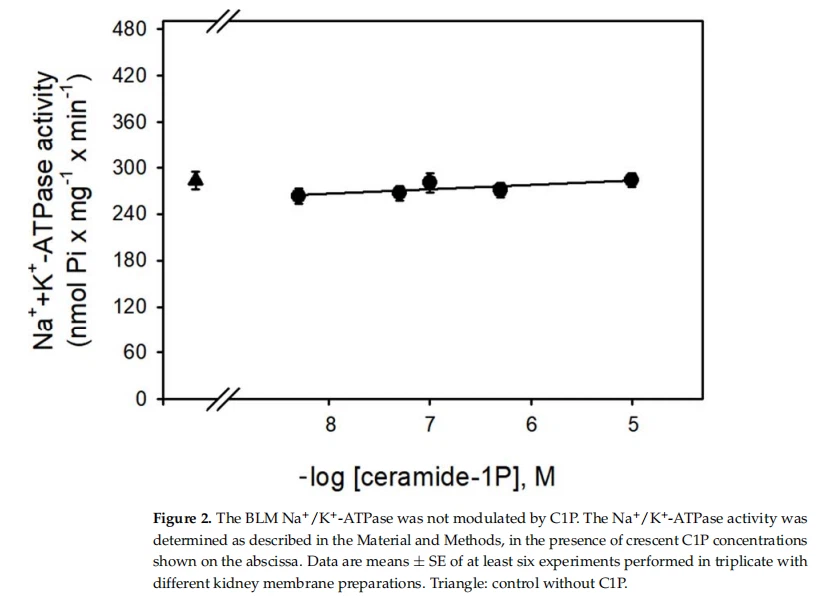
L'efecte modulador significatiu de ClP sobre l'activitat Nat-ATPasa es podria atribuir a (i) canvis estructurals en el BLM similars als observats amb l'activació de Smase i l'alliberament de Cer [31, 43] o (ii) a l'activació directa de proteïnes cinases que es coneixen com a dianes de les ceramides en diferents cèl·lules [12,18,44]. En un article anterior, vam demostrar que Cer era capaç de modular PKC i PKA al BLM[18,33]. Per tant, atès que la PKC i la PKA estaven especialment implicades en la modulació de la Nat-ATPasa [45-48], es van realitzar els experiments següents per investigar si l'efecte inhibidor de C1P sobre els transportadors de Nat actius als túbuls proximals del ronyó implicava PKC o PKA, dues de les principals quinases que ja mostra el nostre grup dins del BLM renal [18,33].
La figura 3 demostra la implicació d'un BLM-PKC en la modulació de la Nat-ATPasa. La bomba està fortament estimulada (≈64 per cent ) per PMA, un èster de forbol que imita DAG dins del medi de reacció, donant lloc a l'activació de PKC. Per contra, ClP va induir una inhibició significativa (≈43 per cent) de l'activitat de Nat-ATPasa, que es prevé completament quan les fraccions BLM es van pre-incubar amb el conegut inhibidor de PKC, calfostina-C. L'addició simultània de PMA i ClP no va afectar l'activitat ATPasa, cosa que suggereix una contraacció mútua a la bomba.

La figura 4 mostra clarament que la preincubació de BLM amb cAMP va provocar un augment robust (≈65 per cent) de l'activitat de Nat-ATPasa, cosa que suggereix que la PKA associada a BLM està llesta per activar-se i activar la segona bomba de sodi. D'altra banda, la preincubació de les fraccions BLM amb 100 nM C1P va provocar una inhibició significativa (c40 per cent) de la bomba, que no es va revertir en presència de cAMP, ni es va evitar preincubant les fraccions BLM amb 10 nM PKAi. Com era d'esperar, la preincubació del BLM amb el PKAi no va afectar l'activitat de Na més -ATPasa.

L'efecte de Ceron sobre l'activitat BLM-PKA i-PKC es va demostrar prèviament [18, 33], però segons el nostre coneixement, no hi havia dades sobre l'acció de C1P sobre les quinases associades a BLM. Així, vam decidir avaluar les activitats de PKA i PKC després de l'estimulació del BLM amb C1P. La figura 5A mostra que la incubació de les fraccions BLM amb 100 nM de C1P va provocar un augment de dues vegades en l'activitat PKA associada a BLM, que va ser la mateixa que s'obtenia quan les fraccions BLM es van incubar amb 100 nM cAMP. L'addició simultània de ClP i cAMP no va provocar un efecte additiu, cosa que suggereix que ClP i cAMP activen el mateix conjunt de PKA associat a BLM, o que si hi ha diferents grups de PKA, s'activen en la mateixa mesura. D'altra banda, la figura 5B mostra que C1P va inhibir significativament (en un ≈43 per cent ) l'activitat BLM-PKC, amb l'efecte que es va contrarestar completament quan es va afegir 10-12 M PMA simultàniament a l'assaig. Els resultats que es presenten aquí mostren clarament que 100 nM cAMP i 1 pM PMA van estimular tant la Nat-ATPasa com, respectivament, PKA i PKC en la mateixa mesura, mentre que la xarxa reguladora provocada per C1P no es va poder correlacionar directament. Això ens va portar a reforçar la hipòtesi plantejada en treballs anteriors[33] considerant que ha d'existir una jerarquia entre les activitats de PKA i PKC que desencadenen la Na més -ATPasa dins del BLM.

Figura 5. El fosfat de ceramida-1 modula diferencialment la PKC i la PKA al BLM. (A) l'activitat de la cinasa inhibida pel joc es va analitzar tal com es descriu al Material i Mètodes, ja sigui en absència o presència de CIP i AMPc afegits sols o en les combinacions que es mostren a l'abscissa. L'activitat de PKA es va determinar com la diferència entre la fosforilació total de la histona H8 i la mesurada en presència de PKA 10 nM: pèptid (5-22). (B) L'activitat de la cinasa inhibida per Calfostina C es va analitzar tal com es descriu al Material i Mètodes, ja sigui en absència o presència de CIP i PMA afegits sols o en les combinacions que es mostren a l'abscissa. L'activitat de PKC es va determinar com la diferència entre la fosforilació total d'histona H8 i la mesurada en presència de calfostina C. Les dades són les mitjanes ± SE d'almenys sis experiments realitzats per triplicat amb diferents preparacions de membrana renal. "Les estadístiques estadístiques sobre el control sense addicions. (pàg<>

