Un nou model de ratolí atàxic d'atàxia telangiectàsia causada per una mutació sense sentit clínicament rellevant (part 2)
Jun 10, 2022
Per obtenir més informació, contacteudavid.wan@wecistanche.com
3.0 Discussió
En augmentar l'estrès genotòxic mitjançant l'addició d'un èxit secundari a la via DDR, vam generar un nou model de ratolí que mostra el conjunt més complet de símptomes AT de qualsevol model fins ara. Això inclou atàxia severa i progressiva associada a l'atròfia cerebel·losa i les pertorbacions de les propietats de la PN juntament amb una alta incidència de càncer i defectes en el desenvolupament de les cèl·lules immunitàries. En conjunt, aquestes comorbiditats engloben les tres principals causes de mort prematura aAT: cadascú contribuinta aproximadament un terç de les morts. D'aquests, l'efecte incapacitant de l'atàxia és el més penetrant i els pacients i els cuidadors informen que té el major impacte en la seva qualitat de vida. Per aquest motiu, la presència d'atàxia i atròfia cerebel·losa en aquest nou model de ratolí és de gran importància, ja que proporciona per primera vegada un recurs no només per dilucidar els mecanismes de la disfunció neurològica, sinó també un model in vivo de necessitat crítica per prova les terapèutiques AT molt necessàries, com ara els compostos de lectura que descrivim aquí. Hem trobat diverses similituds entre la progressió global de l'atàxia a l'Atm3535; Ratolins Aptx ipacients amb AT. A l'AT clínica, els dèficits motors s'observen aproximadament als 2 anys d'edat, quan els pares i els metges detecten una capacitat reduïda de transició del nen a una porta suau i coordinada de manera reflexiva; malauradament, se sap poc sobre els defectes motors en etapes primerenques a causa de les malalties. baixa prevalença i manca actual de proves de diagnòstic precoç (Rothblum-Oviatt et al. 2016). Normalment, els pacients aprenen a caminar sense ajuda i els símptomes neurològics solen mantenir-se estables durant els primers 4 o 5 anys de vida (Rothblum-Oviatt et al. 2016). Hem trobat una progressió primerenca similar dels dèficits motors a Atm735 × R3x; Ratolins Aptx^', que detecten dèficits motors lleus primerencs a P8 (dèficit reflex de correcció) seguit d'un període d'estabilitat relativa, abans de l'aparició d'atàxia progressiva i severa que es va desenvolupar després de p210 que incloïa canvis en la marxa, reflex de sobresalt, tremolor i locomotora. activitat. D'aquestes troballes sorgeixen diverses preguntes importants, inclosa si l'ATM i/o l'APTX tenen un paper en el desenvolupament neurològic en el
cerebel. Els estudis futurs centrats en la fase inicial del trastorn seran crítics per entendre si el cerebel es desenvolupa normalment abans de la disfunció o si els defectes del desenvolupament són una causa inicial. També vam trobar, de manera similar als pacients amb AT, que la gravetat de l'atàxia de desenvolupament tardà era variable, amb alguns ratolins que deambulaven amb una porta posterior maldestra i de pas alt (vídeo 3) i d'altres es mouen gairebé completament mitjançant la contorsió del tronc posterior ( Fig.1E i vídeo 4) (Rothblum-Oviatt et al.2016; Levy i Lang 2018; Boder i Sedgwick 1958). En general, hem trobat que Atm?35×xR35×; Els ratolins Aptx van desenvolupar una pèrdua progressiva visualment profunda i mesurable de la coordinació motora similar a la observada en pacients amb AT, que va ser rescatada mitjançant l'expressió d'almenys una còpia de l'Atm o Aptx get he. La pèrdua de coordinació motora en AT s'ha atribuït a la degeneració cerebel·losa a causa de la seva neuropatologia relativament selectiva a tot el cervell i el seu paper causal en diverses formes diferents d'atàxia (Hoche et al.2012). Consistent ambpacient ATestudis de neuroimatge (Wallis et al.2007; Sahama et al.2015; Sahama et al. 2014; Dineen et al. 2020; Tavani et al. 2003; Quarantelli et al.2013), trobem que la mida del cerebel en Atm735×R3× ; Els ratolins Aptx són inicialment normals, però progressivament s'atrofien simultàniament amb els canvis en la funció neurològica. Tot i que la pèrdua de teixit cerebel·lar s'ha considerat una causa principal d'atàxia en humans, no està clar a partir de les dades clíniques si la gravetat de l'atàxia és un bon predictor de l'abast de la degeneració cerebel·losa trobada postmortem (Aguilar et al. 1968b: Crawford et al, 2006). : Dineen et al.2020). Al caixer automàtic?35×R35×; Els ratolins Aptx^, trobem una clara atròfia associada a l'aprimament de la capa dendrita de la neurona de Purkinje que precedeix els dèficits de comportament severs i tardans. Les nostres observacions histològiques a l'ATM?35xR35×; Els ratolins Aptx suggereixen que els canvis en la funció cerebel·losa en si, més que la pèrdua profunda de cèl·lules cerebel·loses, són suficients per provocar el fenotip atàxic, d'acord amb l'observació de defectes de comportament abans de la pèrdua significativa de PN en diversos SCA (Shakkottai et al. 2011: Lorenzetti et al., 2000; Clark et al., 1997; Jayabal et al., 2016). La raó per la qual es requereix una deficiència d'ATM i APTX per generar atàxia en ratolins quan la pèrdua d'un d'ells és suficient per provocar atàxia en humans encara no està clara. Una possibilitat és que el cervell dels rosegadors pugui utilitzar de manera més flexible vies compensatòries o proteïnes redundants mentre respon a les 10-20k lesions d'ADN que afecten les cèl·lules cada dia (Lindahl i Barnes 2000). Existeixen diverses formes de reparació de l'ADN per afrontar aquest repte, inclosa la reparació d'excisió de bases (BER), la reparació d'excisió de nucleòtids (NER),


Feu clic aquí per obtenir més informació sobre Cistanche
així com unió extrem homòloga i no homòleg (HEJ i NHEJ, respectivament), tots els quals s'han implicat ATM i APTX (Chou et al.2015; Caglayan et al.2017; Wakasugi et al. 2014; Tumbale et al. 2018; Chatterjee i Walker 2017) Alternativament, pot ser el cas que la deficiència d'ATM o APTX per si sol no afecti adequadament la salut cel·lular durant la vida útil relativament curta del ratolí i, per tant, és necessari eliminar ambdues proteïnes per aconseguir una acumulació suficient de danys a l'ADN per manifestar-se durant aquest període de temps. Aquesta possibilitat es veu reforçada pel fet que l'ATM i l'APTX tenen propietats bioquímiques i funcions funcionals diferents en la resposta al dany de l'ADN i, per tant, es preveu que una deficiència en ambdós provoqui un impacte més ampli en l'estabilitat del genoma (és a dir, un augment de l'estrès genotòxic). La nostra troballa que es necessiten dues proteïnes de la via d'estabilitat del genoma per induir defectes neurològics en ratolins suggereix fortament que és la pèrdua de l'Oriol d'ATM en la reparació de l'ADN, en lloc de funcions potencials en la senyalització de l'estrès oxidatiu, la mitofàgia o la funció mitocondrial les que causen els defectes cerebel·lars. Shiloh 2020). Les alternatives, però, no es poden descartar completament, ja que l'APTX, com l'ATM, s'ha observat dins dels mitocondris de les cèl·lules cerebrals, on es creu que suporta el processament de l'ADN mitocondrial (Meagher i Lightowlers 2014; Sykora et al. 2011). Aquest nou model de ratolí proporciona una nova eina per explorar aquestes possibilitats i definir de manera mecànica com la pèrdua d'ATM i APTX provoca, finalment, la disfunció cerebel·losa. Les pertorbacions biofísiques observades en PN registrades a partir de l'AtmR35XR35X; Els ratolins Aptx es troben de manera similar en diversos altres models de ratolí d'atàxia. Això inclou els canvis que hem observat en la resistència d'entrada de PN, la capacitat de la membrana i el llindar i l'amplada AP, que també s'han descrit en models de ratolí de SCA com 1, 3 i 7 (Stoyas et al.2020; Shakkottai et al.2011; Dell. 'Orco et al.2015). A més, la reducció progressiva de la freqüència de tret del potencial d'acció PN que informem es correlaciona positivament amb el desenvolupament d'atàxia a l'AtrnR35XR35X; Aptx'mice s'informa en un gran nombre de models de ratolí atàxic, inclosos els SCA 1, 2, 3,5, 6 i 13, així com algunes formes episòdiques (vegeu la revisió (Cook, Fields i Watt 2021)). Atesa la superposició significativa de les pertorbacions de PN observades en moltes atàxies diferents causades per defectes cel·lulars diferents, la restauració de les freqüències de tret de PN AP s'ha considerat com un enfocament terapèutic de base àmplia. Tanmateix, encara no està clar si la reducció del tret de PN és un factor causal de l'atàxia. A més, l'evidència experimental suggereix que els canvis en l'activitat de la NP poden ser, de fet, una resposta generalitzada per mantenir l'homeòstasi durant el deteriorament de la fisiologia de la NP relacionada amb la malaltia (Dell'Orco et al.2015). Per tant, calen esforços continuats a totes les atàxies cerebel·loses per vincular les alteracions genètiques, moleculars i cel·lulars causades per la malaltia amb els canvis específics en la senyalització neuronal cerebel·losa que finalment generen l'atàxia. En aquest esforç serà molt important determinar si els defectes cerebel·losos que causen malalties causen atàxia habitualment o de manera diferencial a través d'una pèrdua de la funció cerebel·losa (p. ex., pèrdua de senyals de coordinació durant el moviment) o per un efecte dominant-negatiu (p. circuits amb patrons de sortida neuronals anormals). En última instància, mentre que una estratègia terapèutica comuna per abordar les atàxies cerebel·loses tindria el major impacte, un enfocament dirigit que abordi les diferents causes genètiques i moleculars de la disfunció cel·lular pot ser, finalment, necessari per desenvolupar amb èxit una terapèutica eficaç. L'enllaç mecanicista entre una deficiència d'ADN proteïnes d'estabilitat com l'ATM i l'APTX i la disfunció PN està lluny de ser clara. Els nostres resultats suggereixen que l'efecte de la pèrdua d'ATM i APTX sobre els PN és intrínsec, ja que no trobem canvis en les propietats presinàptiques de les cèl·lules granulars ni evidència de la seva pèrdua cel·lular (cap canvi en el gruix de GCL). A més, tot i que vam observar diferències en la plasticitat a curt termini dels inputs d'olivars inferiors en PN i tipus salvatge amb deficiència d'ATM i APTX, aquests resultats probablement apunten a una interrupció de l'homeòstasi de Ca2 * potencialment mitjançant reduccions d'inositol 1,4,5- expressió del receptor de trifosfat 1(ltpr1), similar a les observades en models de ratolins SCA 1,2 i 3, així com en ratolins amb deficiència d'ATM (Kim et al.2020; Chen et al.2008; Demirci et al.2009; Shakkottai et al.2009; Shakkottai et al. al.2011). Tot i que això proporciona una via prometedora per a un examen i comparació futurs, encara no està clar, fins i tot per als SCA, si els canvis en l'homeòstasi de Ca²* són el factor causal o només un altre símptoma o fins i tot una resposta compensatòria de les NP malaltes o alterades (Dell 'Orco et al.2015). En el sistema immunitari, l'ATM està implicat en la reparació de trencaments d'ADN que es produeixen de manera natural durant la reordenació gènica dels gens del receptor d'antigen en els precursors de cèl·lules B i T, un fenomen crític per a la diversitat de receptors d'antigen (LG i TCR) d'aquestes cèl·lules. trobant aixòCèl·lula Tles proporcions a la sang es redueixen significativament és coherent amb estudis previs en humans i ratolins nocauts AT (Schubert, Reichenbach i Zielen 2002; Hathcock et al.2013; Chao, Yang i Xu 2000; Barlow et al.1996). Aquesta reducció de cèl·lules T a la perifèria probablement es correlaciona amb un defecte de la immunitat tant cel·lular com humoral. És important destacar que vam trobar que l'expressió d'una còpia del gen ATM és suficient per restaurar els dèficits de CD4 més a la sang, cosa que indica que les teràpies capaços de restaurar l'expressió parcial de l'ATM tindrien eficàcia terapèutica. Tot i que no hem avaluat el desenvolupament de cèl·lules B en aquest article, és probable que conclusions similars s'apliquin a aquest procés donades les seves similituds mecanicistes (Marshall et al. 2018). Com era d'esperar, la reducció de cèl·lules T a la sang perifèrica es correlaciona amb el desenvolupament defectuós dels timòcits. En el tim, hem trobat dos defectes principals. Un, induït principalment per la deficiència d'APTX, es manifesta com un defecte en la transició de DN3 a DN4 coincidint amb la reordenació primerenca del locus TCR. L'altre defecte, causat principalment per la deficiència d'ATM, es correlaciona amb la progressió reduïda de CD4 * CD8 doble positiu a cèl·lules monopositives, principalment timòcits CD4'. Tot i que la troballa d'APTX va ser sorprenent, ja que la seva deficiència (AOA 1) no està associada a dèficits immunitaris, se sap que APTX interacciona amb proteïnes de reordenació del gen TCR, inclosa XRCC4 (Clements et al. 2004). Els futurs estudis dirigits a definir el paper de l'APTX en els mecanismes d'unió final durant la reordenació del gen TCR seran


important, i la possibilitat que mecanismes d'unió d'extrems alternatius, com l'ús de microhomologies, expliquen la manca d'un dèficit immunitari en la seva absència necessita més investigació (Bogue et al. 1997). La supervivència d'Atm?35×/R35×; Aptx'mice és considerablement més llarg que els models de ratolí AT anteriors. En comparació, el primerA KOmodel de ratolí reportat per Barlow et al. morien a causa dels timomes, normalment en 2-4 mesos després del naixement (Barlow et al. 1996). La disminució de la supervivència del càncer en aquest i en molts altres models de ratolí AT eliminatoris és probablement genètica, ja que s'ha demostrat que la soca de fons que alberga la mutació té efectes significatius en la prevalença i la supervivència del càncer, amb A/J i C57BL/6.
antecedents que han augmentat significativament la supervivència respecte a les soques BALBC i 129S (Genik et al. 2014). El fet que els nostres ratolins amb deficiència d'ATM s'hagin creat en un fons C57BL/6 probablement subjau; que els ratolins Aptx*t no desenvolupen atàxia, és la seva vida útil relativament llarga. Tenint en compte que l'Atm35xR35×; És poc probable que la mort primerenca en els ratolins AT KO impedeixi l'observació d'un fenotip atàxic que d'altra manera es desenvoluparia en aquests ratolins. Tanmateix, es desconeix si el fons C57BL/6 confereix resiliència al desenvolupament d'atàxia, com ho fa amb el càncer. Definir els factors genètics o possiblement epigenètics que influeixen en la gravetat de la malaltia podria proporcionar vies per al desenvolupament terapèutic futur. Atesa la naturalesa global de la mutació nul·la ATM i APTX al nostre model de ratolí, no podem descartar completament que els defectes extracerebel·losos també puguin contribuir al fenotip atàxic greu i, per tant, un examen futur fora del cerebel al cervell anterior, tronc cerebral i medul·la espinal. , i fins i tot s'haurà de fer múscul. Dins del cerebel, tot i que vam trobar algunes diferències anatòmiques en les propietats de tret de PN dins de diferents regions del cerebel, no vam detectar diferències regionals en l'amplada de ML o la densitat de PN. Tanmateix, hi ha reptes a l'hora d'utilitzar l'anatomia regional com a factor d'agrupació al cerebel, ja que els plecs físics del teixit no necessàriament es correlacionen amb els límits dels dominis funcionals, d'expressió molecular o de propietats fisiològiques que s'han descrit (Apps i Hawkes 2009). ; Tsutsumi et al.2015; Gao, van Beugen i De Zeeuw 2012; Zhou et al.2014). Els experiments centrats a examinar l'extensió dels defectes cerebel·losos dins d'aquests dominis seran importants en estudis futurs i en comparació amb els informes anecdòtics de diferències anatòmiques en pacients amb AT (Verhagen et al.2012; De Leon, Grover i Huff 1976; Amromin, Boder, i Teplitz 1979; Monaco et al. 1988; Terplan i Krauss 1969; Strich 1966; Solitare 1968; Solitare i Lopez 1967; Aguilar et al. 1968a; Paula-Barbosa et al. 1983). Mentre detectem dues etapes potencials en la progressió de l'atàxia a l'Atm735wR35x; Els ratolins Aptx, l'etapa posterior de l'atàxia severa es desenvolupa a l'edat adulta en ratolins, en comparació amb l'inici de la infància en humans. Això pot limitar el seu ús en alguns estudis de neurodesenvolupament. A més, la interpretació de futurs experiments ha de tenir en compte el fet que aquest nou model expressa mutacions nul·les en dos gens d'estabilitat del genoma alhora, una situació que no s'ha detectat en pacients humans amb AT o AOA1. Finalment, identificar on, quan i com la deficiència d'ATM causa patologia cerebel·losa i atàxia ha estat un repte, ja que els ratolins anteriors amb deficiència d'ATM generalment no tenen les característiques necessàries per vincular causalment els dèficits cel·lulars i moleculars amb el fenotip atàxic. S'han definit múltiples vies d'investigació prometedores, incloses les enfocades a nivell neuronal, on l'ATM està implicada en la senyalització de l'estrès oxidatiu (Chen et al.2003) i la funció sinàptica (Li et al.2009; Vail et al.2016), com així com la funció glial, on l'evidència recent suggereix que la patologia glial pot ser un factor principal en la patologia cerebel·losa (Kaminsky et al. 2016; Campbell et al. 2016; Petersen, Rimkus i Wassarman 2012; Weyemi et al. 2015). Aquest nou model animal proporciona una nova eina per provar hipòtesis mecanicistes sobre com la deficiència d'ATM provoca patologia cerebel·losa i atàxia. A més, aquest model pot servir de manera més important com a eina preclínica crítica per provar candidats terapèutics proposats anteriorment (Browne et al. 2004; Chen et al. 2003) i els nostres propis compostos SMRT (Du et al. 2013). No es poden exagerar les greus limitacions de no tenir un model preclínic adequat per a les proves terapèutiques, especialment per a trastorns rars com l'AT i l'AOA1.
4.0 Materials i mètodes





4.1 Declaració Ètica
Aquest estudi es va realitzar d'acord amb les recomanacions de la Guia per a la cura i l'ús d'animals de laboratori dels Instituts Nacionals de Salut. Tots els animals es van manipular d'acord amb els protocols aprovats del Comitè Institucional de Cura i Ús d'Animals (IACUC) a The Lundquist Institute (31374-03,31773-02) i UCLA (ARC-2007-082, ARC{{3}). }). El protocol va ser aprovat pel Comitè d'ètica dels experiments amb animals de l'Institut Lundquist (número d'assegurança: D16-00213). Es va fer tot el possible per minimitzar el dolor i el sofriment proporcionant suport quan fos necessari i escollint punts finals ètics.
4.2 Ratolins
All mice were group-housed and kept under a 12-h day/night cycle with food and water available ad libitum. Animals were housed within the general mouse house population, and not in specialized pathogen-free rooms. Older animals were made available wetted food or food gel packs on the ground of the cages as ataxia developed. Atm35 and Atm935×mice were created and provided by Dr. Hicks and colleagues at the University of Manitoba. These mice were created to contain the c.103C>La mutació T es troba en una gran població del nord d'ÀfricaATpacients using recombineering Gateway technology and site-directed mutagenesis. A C>T mutation at this position in the mouse Atm gene creates a TAG G stop codon. The same mutation in the human ATM gene produces a TGA G stop codon. In consideration of the use of these models for therapeutic interventions, we chose to create a mouse model for each of the two PTC codons(Fig.1A). A modified Gateway R3-R4-destination vector was used to pull out the desired region of the mouse Atm gene from a Bacterial Artificial Chromosome (BAC) and subsequently mutated to create either a TAG G stop codon at codon 35(M00001, position 103(C>T))or a TGA G stop codon (M00002, position 103 (CAG>TGA), replicant l'AT PTC humà). Els al·lels genòmics es van clonar després en una versió modificada del vector d'orientació a mamífers NorCOMM mitjançant una 3-way Gateway Reaction (Bradley et al. 2012). Els vectors d'orientació resultants es van electroporar a cèl·lules C2 ES (C57BI/6N, derivades al laboratori A. Nagy, Toronto, Canadà) i es van identificar clons dirigits amb èxit mitjançant la selecció amb G418 (Gertsenstein et al.2010). La integració del casset d'orientació mutat al locus del gen Atm es va confirmar mitjançant Southern blot, i mitjançant la seqüenciació de productes de PCR per confirmar la presència de la mutació Atm PTC, orientació sense errors al locus Atm i components funcionals sense errors del
vector (dades no mostrades). Es van utilitzar clons ES positius per a la injecció de blastocist per obtenir les línies transgèniques. L'al·lel transgènic contenia un promotor-delta de beta-actina humana floxadaTK1-Neo cassette in the intron upstream of the region containing the mutated exon. This floxed cassette was subsequently excised by crossing with a Cre driver mouse(B6.C-Tg(CMV-are)1Cgn/J) to generate Atm3x+ and AtmM1(103CTMFcc, respectively) mouse lines Atm35×+ (MGI nomenclature: AtmTM1(103CAG>TGA)MFGCc;(Fig.1A). El genotipat de les dues línies Atm es va realitzar utilitzant els següents cebadors a Tm 62 graus: primer (F) del gen Atm: 5'-CCTTTGAGGCATAAGTTGCAACTTG-3'; i el cebador invers (R) del gen Atm: 5'-GTACAGTGTATCAGGTTAGGCATGC-3', creant un producte al·lel de tipus salvatge de 151 pb o un producte al·lel objectiu de 241 pb (Figs. 1A, 1B). Atmn35~ i Atm035×v eren retrocreuat amb ratolins C57Bl/6J durant 9 generacions (99,2 per cent isogènics) abans de la criopreservació i la posterior derivació mitjançant mares substitutes C57BI/6J. Atm735× i Atm?35x i Atm 35×/Q35× eren criadors obtinguts de ratolins F1 germans Atm35 i Atm835X plus. AtmR35×k35×: es va trobar que tots dos eren fèrtils. Els ratolins Aptx knockout (Aptx) van ser creats i subministrats al Dr. Mathews com a embrions del Dr. McKinnon (Ahel et al.2006), i posteriorment es van tornar a derivar mitjançant mares substitutes C57Bl/6J. Els ratolins Aptx es troben en un fons mixt C57Bl/6 i 129. Atm35k35; Es van crear ratolins Aptx de diverses combinacions de tipus salvatge, heterozigots i homozigots a partir d'Atm35X; Els criadors Aptxt es van generar encreuant ratolins Atm?35×R35 i Aptx^. Es va utilitzar una cohort de ratolins de doble mutant i de control corresponent en l'estudi longitudinal de comportament per a anàlisis de la marxa i proves SHERPA (Figs. 2, 3). Es van utilitzar múltiples cohorts addicionals de ratolins mutants dobles i control de l'edat per a experiments electrofisiològics, immunohistològics i de prova de pol vertical (Figs.4, 7). Els experiments immunològics i d'expressió de proteïnes es van dur a terme amb ratolins criats dels ratolins originals AtmR35× i Atm35×rederivats (Figs. 5, 6 i 8). El genotipat es va realitzar a partir de mostres de teixit de l'oïda de ratolins P8-11. Es van utilitzar mètodes de PCR en temps real realitzats per Transnetyx Inc. per determinar el genotip de cada animal. Els animals es van fer identificables mitjançant tatuatges als dits dels peus fets al mateix temps que la biòpsia de l'oïda. Es van quantificar els primers únics per a Atm35× i Atm35× per identificar ratolins de tipus salvatge, heterozigots i homozigots (llistats anteriorment). Es van utilitzar cebadors Aptx'i Aptx*" per avaluar els seus genotips.
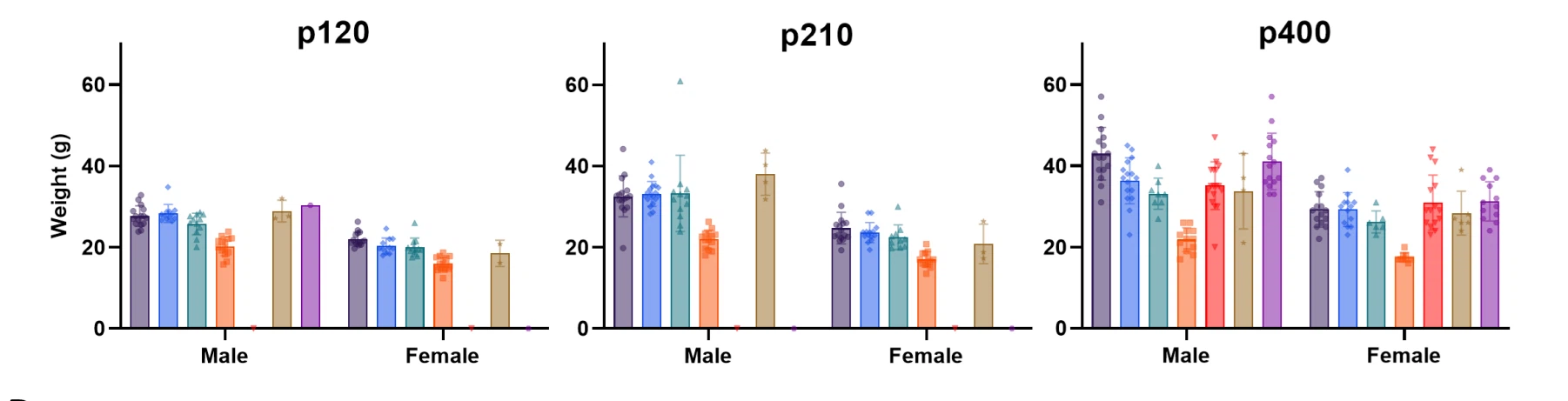

4.3 Sanitat animal
Els animals es van pesar mitjançant una bàscula digital a P8, 45, 120.210.400. La mort de l'animal es va registrar com el dia de la mort, o el dia de l'eutanasia quan els animals van arribar a un punt final humà (animal incapaç d'arreglar-se dins dels anys 60, un important pèl que indica la manca d'autopreparació o una angoixa excessiva tal com va assenyalar el veterinari). personal). Les carcasses d'animals es van congelar immediatament després de la mort i es van realitzar necròpsies post mortem per lots. La probable causa de la mort es va determinar en la mesura que vam poder en col·laboració amb el veterinari del personal (Dra. Catalina Guerra) mitjançant una inspecció visual dels òrgans interns. Alguns ratolins van ser canibalitzats o eliminats accidentalment pel personal del vivari i ho van ser
per tant, etiquetats com a "desapareguts". Els ratolins sense una causa visual de mort discernible es van etiquetar "indeterminables". les causes probables de mort (p. ex., fetge augmentat, bloqueig urinari) es van etiquetar "altres".
4.4 Comportament
Abans de realitzar qualsevol prova de comportament, els ratolins es van aclimatar a la suite de comportament durant uns 20 minuts. Els ratolins es van provar en diferents moments del dia, d'acord amb el seu cicle diari. Es va realitzar una bateria de proves de comportament en ratolins dobles mutants ingènus dels genotips indicats en diversos moments segons el comportament, però en la mateixa cohort de ratolins. La bateria de proves incloïa l'avaluació Catwalk Gait (P45, 120,210, 400) i un subconjunt de les proves SmithKline-Beecham Harwell Imperial-College i Royal-London-Hospital Phenotype Assessment (SHERPA) (P30 i 400). Aquestes proves van ser realitzades pel UCLA Behavioral Core. Els ratolins dobles mutants i control es van examinar addicionalment a la prova del pol vertical. Tots els aparells de comportament es van netejar amb etanol (70 per cent) entre cada subjecte de prova.

Anàlisi de la marxa
Hem utilitzat un sistema d'anàlisi Noldus Catwalk Gait dissenyat per mesurar i analitzar de manera semiautomàtica la marxa dels ratolins durant la deambulació normal. Breument, el moviment dels ratolins a través d'un passadís amb fons de vidre es grava en vídeo des d'una posició central. Les empremtes de potes es destaquen al vídeo a causa de la il·luminació lleugera a través de la plataforma de vidre. Cada pas del ratolí dins d'un vídeo es detecta posteriorment mitjançant Catwalk XT (Noldus) de manera semiautomatitzada. Una carrera per a cada ratolí consta de 3 proves de deambulació consistent a través de la plataforma monitoritzada. Només s'accepten proves consistents, i els ratolins poden trigar fins a 10 intents per completar 3 assaigs compatibles en qualsevol direcció a través del corredor. Els assaigs de compliment es van definir com aquells amb moviment a través de la plataforma de menys de 5 s de llarg i amb una variació de velocitat no superior al 60 per cent. Un cop col·locats a la plataforma, els ratolins generalment corrien d'anada i tornada sense necessitat d'incitació a l'experimentador.
Pol Vertical
Els ratolins es col·loquen a la part superior d'un cargol de 80 cm d'alçada amb el nas cap avall i les potes posteriors el més a prop possible de la part superior. Els ratolins s'alliberen immediatament i el temps comença immediatament després de la col·locació.
El temps s'atura quan la primera pota anterior toca la superfície per sota del pol. La predilecció natural d'un ratolí és baixar immediatament pel pal, i se'ls dóna fins a 60 segons per travessar el pal, en cas contrari, se'ls ajuda a sortir del pal. A una prova no completada se li dóna automàticament un temps de 30 segons, ja que el 95 per cent dels ratolins que no van baixar en 30 segons encara estaven al pal a la marca dels 60. Les proves de comportament SHIRPA van ser realitzades per la Universitat de Califòrnia, Los Angeles Behavioral Core a P30
i P400. Tots els paràmetres es puntuen per proporcionar una avaluació quantitativa. que permet comparar els resultats tant en el temps com entre diferents laboratoris. Cada ratolí es va provar seqüencialment en tots els comportaments en un període de temps de ~20-min abans de passar al següent ratolí. L'experimentador estava cec al genotip animal. La pantalla es va realitzar tal com es va descriure anteriorment (Rogers et al. 1997).


Observació de la conducta
La pantalla principal proporciona un perfil d'observació del comportament i l'avaluació de cada animal comença observant el comportament no pertorbat en un pot de visualització (10 cm de diàmetre) durant 5 minuts. A més de les conductes puntuades de la posició corporal, l'activitat espontània, la freqüència respiratòria i el tremolor, l'observador registra qualsevol cas de comportament estrany o estereotipat i convulsions, llepades compulsives, mossegada autodestructiva i retropulsió (caminant cap enrere) i indicis d'espai. desorientació.
Comportament de l'arena
Després, el ratolí es trasllada a l'arena (30 cm x 50 cm) per provar l'excitació de la transferència i l'observació del comportament normal. L'arena està marcada en una quadrícula de quadrats de 10 x 10 cm² per mesurar l'activitat locomotora en un període de 30 s. Mentre el ratolí està actiu a l'arena, es registren les mesures de resposta de sobresalt, marxa, elevació pèlvica i elevació de la cua.
Contenció supina
L'animal està subjecte en posició supina per registrar els comportaments autònoms. Durant aquesta avaluació, es van avaluar la força d'adherència, el to corporal, el reflex del pavelló, el reflex de la còrnia, el pessic del dit del peu, la maniobra de filferro i la freqüència cardíaca.
Equilibri i Orientació
Finalment, es van realitzar diverses mesures de la funció del sistema vestibular. Es van realitzar les proves de reflex d'adreçament, reflex de contacte i de geotaxi negativa. Al llarg d'aquest procediment es va registrar la vocalització, la micció i la por general, la irritabilitat o l'agressivitat.

Equipament utilitzat
1.Pavelló de plexiglàs transparent (dimensions interiors aproximades 55x33 x18 cm). Al terra de l'arena hi ha una làmina de plexiglàs marcada amb 15 quadrats (11 cm). Un cable horitzontal rígid (3 mm de diàmetre) està subjecte a la cantonada posterior dreta de manera que els animals no puguin tocar els costats durant la maniobra del cable. Una quadrícula (40x 2{0 cm) amb una malla de 12 mm (aproximadament) està assegurada a tota l'amplada de la caixa per mesurar la suspensió de la cua i el comportament de la força d'adherència. 2. Es va utilitzar un cilindre de plexiglàs transparent (15 x ll cm) com a pot de visualització. 3. Un terra de reixeta (40x 2{0 cm) amb malles de 12 mm sobre les quals es troben els pots de visualització.4. Quatre suports cilíndrics d'acer inoxidable (3 cm de llarg x 2,5 cm de diàmetre) per aixecar les reixetes del banc. 5. Una placa d'acer inoxidable quadrada (13 cm) per al trasllat d'animals a l'arena. 6. Talleu longituds de 3/0 Mersilk subjectes a les pinces per a les proves de reflex de la còrnia i el pavelló 7. Es va esmolar una vareta de plàstic fins a una punta de llapis per provar la salivació i la mossegada.8. Un parell de pinces d'equip de dissecció, corbades amb puntes fines (pinces de 125 mm, Philip Harris Scientific, Cat. núm. D46-174), per a la pinça dels dits. 9.Un cronòmetre.10. S'utilitza un quadre de clic de IHR per provar les respostes de sobresalt. La caixa de clic genera un to breu de 20 kHz a 90 dB SPL quan es manté a 30 cm per sobre del ratolí. Contacteu amb el professor KP Steel, MRC Institute of Hearing Research, University Park, Nottingham NG7 2RD. 11.Una regla.12.Un tub de plexiglàs transparent de 30 cm amb un diàmetre intern de 2,5 cm per al reflex d'adreçament de contacte.4.5 Electrofisiologia Preparació de la rodanxa cerebel·losa aguda Es van preparar boniques rodanxes parasagitals de 300 μm de gruix a partir del cerebel de ratolins experimentals i de control. seguint els mètodes publicats (Hansen et al., 2013). En resum, el cerebel es va eliminar ràpidament i es va submergir en una solució extracel·lular freda amb gel amb la composició de (mM): 119 NaCl, 26 NaHCOg, 11 glucosa, 2,5 KCl, 2,5 CaCla, 1,3 MgCla i 1 NaHzPOa, pH 7,4 quan gasificat amb un 5% de CO-/95% d'O2. La cerebel·la es va seccionar parasagitalment mitjançant un vibratom (Leica VT-100, Leica Biosystems, Nussloch, Alemanya) i es va incubar inicialment a 35 graus durant {-30 min, i després es va equilibrar i emmagatzemar a temperatura ambient fins al seu ús. Electrofisiologia extracel·lular Els enregistraments extracel·lulars i intracel·lulars es van obtenir a partir de neurones de Purkinje (PN) en rodanxes perfuses constantment amb una solució extracel·lular amb bombolles de carbogen i mantingudes a 37 graus C (extracel·lular) o 32 graus (intracel·lular) ± 1 grau (vegeu més amunt). Les cèl·lules es van visualitzar amb òptica DIC i un objectiu d'immersió en aigua 40 × (NA 0,75) mitjançant un microscopi Zeiss Examiner. Les pipetes de vidre de ~ 3 MQ de resistència (Model P-1000, Sutter Instruments, Novato, CA) es van omplir amb solució extracel·lular i es van col·locar a prop dels turons d'axons PN per mesurar els transitoris de corrent capacitiu associats al potencial d'acció en mode de pinça de tensió. amb el potencial de la pipeta mantingut a 0 mV. Per als enregistraments de pinça de pegat de cèl·lules senceres, les pipetes es van omplir amb una solució intracel·lular (mM): 140 mesos (CH3KO3S), 10 NaCl, 2 MgCl2, 0,2 CaClz, 10 HEPES, 14 Fosfocreatina (sal tris), 1 EGTA, 4 Mg -ATP, 0,4 Na-GTP. Es va afegir picrotoxina (Sigma) de 100 μM per bloquejar les entrades sinàptiques inhibidores de GABAegeric. Les dades es van adquirir utilitzant
un amplificador MultiClamp 700B a 20 o 100 kHz en mode de tensió o corrent, Digidata 1440 amb pClamp10 (Molecular Devices, Sunnyvale, CA) i filtrat de 2 a 4 kHz. La resistència en sèrie sol ser d'entre 10 i 15 MQ. La resistència de la sèrie es va compensar en un 80 per cent només per a experiments de plasticitat a curt termini. Per als enregistraments extracel·lulars, es van registrar un total de 20 a 45 PN per a cada animal de tots els genotips, sexes i grups d'edat. Els enregistraments es van distribuir tant per l'eix medial-lateral com per l'eix rostrocaudal del cerebel. Només es van examinar cèl·lules amb un aspecte "saludable" (baix contrast de les vores cel·lulars) i una velocitat de tret regular i ininterrompuda. Durant l'anàlisi, es va trobar que algunes cèl·lules tenien llacunes en la cocció de més de 2 segons, i aquestes cèl·lules es van eliminar de l'anàlisi, ja que aquest tipus de cocció s'associa a ser "poc saludable". El teixit mutant doble no difereix qualitativament en aparició sota la microscòpia DIC abans dels enregistraments, ni el nombre de cèl·lules "poques" va ser més gran que el d'altres genotips (7 per cent enfront del 4 a l'11 per cent de totes les cèl·lules dels genotips de control a P400). La comparació espacial de l'activitat neuronal es va obtenir mitjançant l'enregistrament de seccions en sèrie a les rodanxes flòculs, laterals (2"d o 3'), intermèdies (6" o 7è) i medials (11" o 12t). Es van utilitzar rodanxes de nombre inferior en els grups d'edat més joves (P45 i 110) per fer coincidir aproximadament el posicionament relatiu dels enregistraments entre grups d'edat. 0-3 Els enregistraments es van fer des de cada lòbul dins de cada porció en funció de la qualitat i la salut dels teixits. Cada enregistrament va durar {{29} Es van utilitzar de 3 a 5 ratolins per a cada grup d'edat i l'experimentador va quedar cec al genotip, l'edat i el sexe.
Els enregistraments intracel·lulars es van obtenir a partir de PN al lòbul IIl o VIl del cerebel medial (és a dir, vermis); no es van observar diferències estadístiques de propietats entre lòbuls.
Anàlisis


Es van detectar i analitzar els intervals d'interestímuls potencials d'acció espontània mitjançant rutines estàndard i personalitzades a ClampFit (Dispositiu molecular), GoPro (Wavemetrics) i Excel (Microsoft). Concretament, es van detectar el llindar dels potencials d'acció i es van determinar les estadístiques d'augment (és a dir, la freqüència i la durada de l'interval) mitjançant prorutines adaptades (TaroTools; https://sites.google.com/site/tarotoolsregister/). El coeficient de variació de l'interval mitjà entre puntes (CV) i l'interval mitjà entre puntes (CV2=2 ISIn més 1-ISInl/(ISIn més 1 més ISIn)) es va calcular a Excel mitjançant macros personalitzades. Les propietats estàndard de la membrana es van analitzar mitjançant lgorPro. La RM es va determinar fent una mitjana de 3 respostes de traça de tensió a un pols de pas de -5 mV a partir d'un potencial de retenció de {-80 mV i mesurant la desviació del corrent resultant entre 900 i 1000 ms després de l'inici. La constant de temps de la membrana es va mesurar ajustant una única exponencial a la fase de decadència inicial del 90% al 10% del pic. El CM es va calcular dividint la constant de temps de la membrana per la RM. Els esdeveniments sEPSC es van registrar durant una època de 1-minuts i es van detectar i mesurar mitjançant Neuroexpress (v21.1.13). Els axons de fibra paral·lel i escalant es van estimular mitjançant elèctrodes de vidre theta (WPI) i un aïllador d'estímul controlat per TTL (ISO-Flex, AMPI). Les amplituds EPSC evocades i les constants de temps de decadència (1 exp. per a paral·leles i 2 exp. per a fibres enfiladisses) es van analitzar mitjançant rutines personalitzades a lgorPro. Els potencials d'acció es van examinar com a part d'un conjunt d'injeccions de corrent d'1 s entre -500 i 2250 pA (passos de 250 pA) amb un corrent de retenció ajustat per mantenir un potencial de ~ 70 mV. Les formes d'ona del potencial d'acció es van mesurar mitjançant personalitzat
rutines a lgorPro. El llindar del potencial d'acció es va definir com la primera tensió de membrana en què la primera derivada superava els 30 mV/ms (Zhu et al.2006).

4.6 Examen de l'atròfia cerebel·losa
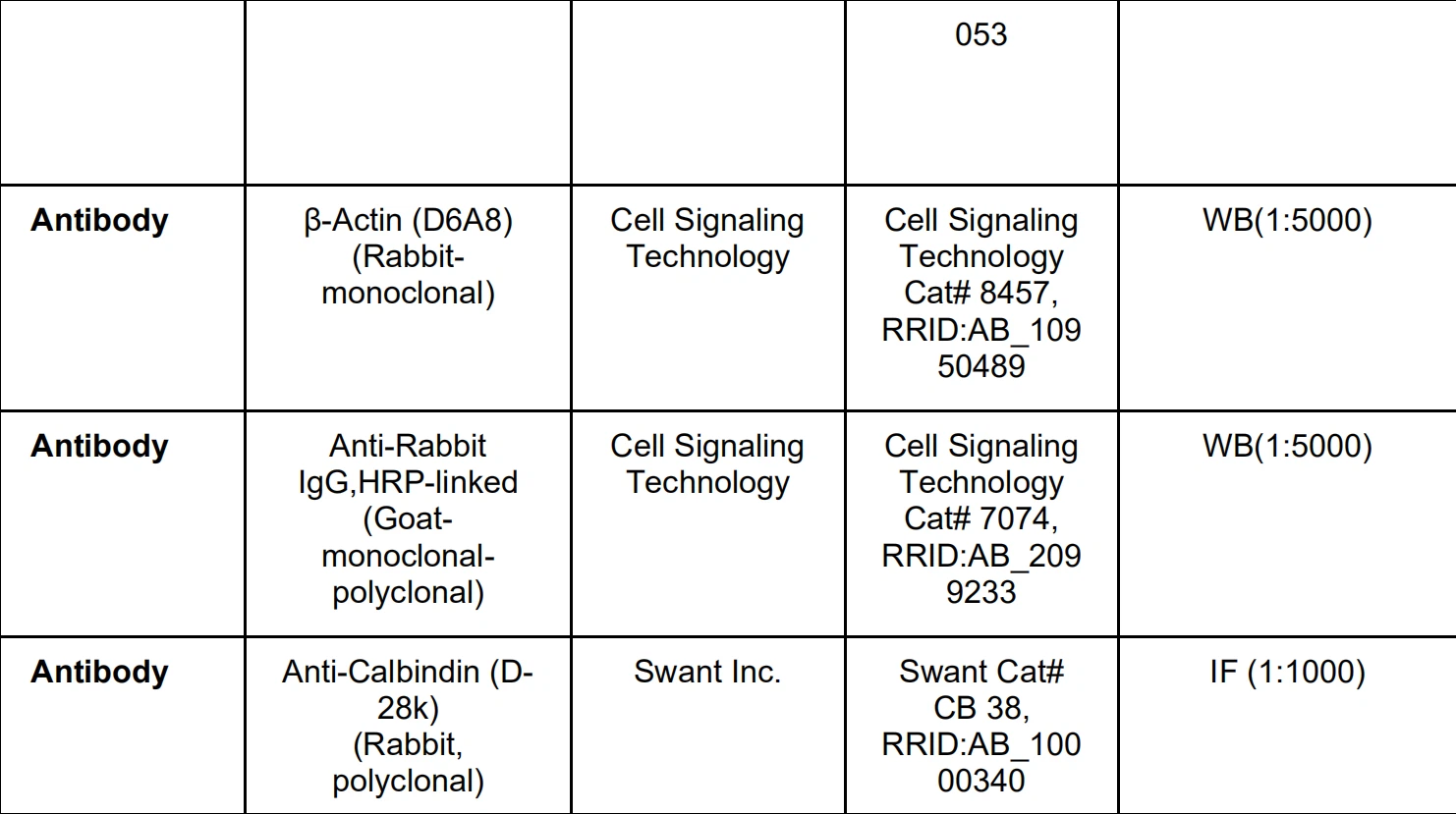
Mida del cerebel Immediatament després de l'eliminació del cervell del crani, es va obtenir una imatge dorsal de muntatge complet. A continuació, les imatges es van processar mitjançant Fiji (NIH). Les mides del cervell anterior i del cerebel es van avaluar delineant el seu 2-espai dimensional i després calculant l'àrea. Hem normalitzat les possibles diferències en la mida global del cervell dividint els resultats del cerebel per la mida del prosencèfal per produir una proporció relativa del cerebel a prosencèfal. Els experimentadors estaven cecs al genotip de l'animal. Immunohistoquímica Als respectius punts finals de l'estudi (P45, 120,210,4{{7{{104}}}}0), ratolins mascles i femelles de tots els genotips representat en aquest estudi es va anestesiar amb isoflurà i es va sotmetre a perfusió transcàrdica amb solució salina tamponada amb fosfat seguida d'un 4% (p/v) de paraformaldehid tamponat (PFA) i després es va disseccionar per extreure el cervell. Les imatges de tot el cervell es van prendre immediatament després d'eliminar el cervell del crani i els cervells es van submergir en un 4% de PFA durant 24 hores, i després es van crioprotegir en solució salina tamponada amb Tris (TBS) amb un 0,05% d'azida i un 30% de sacarosa durant 72 hores. hores i emmagatzemat a 4 graus fins a un nou ús. El cerebel es va separar del cervell anterior i es va seccionar el parasagital mitjançant un micròtom lliscant (Microm HM 430, Thermo Scientific) ajustat a la secció a 40 μm de gruix. Les seccions de cerebel es van recollir en una sèrie de sis i es van emmagatzemar en TBS-AF (TBS amb un 30 per cent de sacarosa, un 0, 05 per cent d'azida de sodi i un 30 per cent de etilenglicol) a 4 graus o -20 graus fins a un nou ús. Per a la visualització immunofluorescent de les neurones de Purkinje, seccions del cerebel de les dues Atm*; Aptx*t i Atm?35×R35×; Aptx ^ (n=5 per genotip) es van rentar durant 5 minuts en TBS tres vegades i després es van bloquejar en sèrum de cabra normal al 15 per cent a temperatura ambient durant 30 minuts seguit d'una incubació flotant en conill o ratolí anti-calbindina D. -28k (1:1000) durant 1 hora a temperatura ambient en un agitador orbital. A continuació, es van rentar les seccions durant 5 minuts amb TBS tres vegades, seguida d'una incubació flotant lliure en Alexa Fluor 488 (1:1000) de cabra anti-conill o ratolí durant 1 h a les fosques a temperatura ambient en un agitador orbital. Després de la incubació d'anticossos secundaris, les seccions es van rentar durant 5 minuts en TBS tres vegades, després es van muntar i es van col·locar amb Fluoromount-G amb DAPI. Per a algunes seccions, també es van sondar anticossos anti-caspasa-3(1:200) i anti-CD68 (1:400) en paral·lel amb Calbindin mitjançant un anticòs secundari Alexa Fluor 647 (1:500). Les diapositives es van escanejar amb Stereo Investigator (MBF Bioscience, ver. 2020) en un microscopi Zeiss equipat amb un ApoTome 2 (Carl Zeiss Microscopy, Axio Imager.M2) utilitzant un objectiu de 2,5, 10, 20, 40 o 63x i imatges. capturat amb una càmera CMOS Hamamatsu (Hamamatsu Photonics, ORCA Flash 4.0 LT plus). Per quantificar el nombre de cèl·lules reactives a la calbindina a cada lòbul a les imatges resultants, vam utilitzar Stereo Investigator per dibuixar aleatòriament 2 línies entre 300 i 500 μm de llarg en Cada lòbul i va comptar manualment el nombre total de PN al llarg de la longitud dins dels 40 µm de gruix de la llesca de teixit amb un augment de 40x. La densitat 2D (nombre de PNs / (longitud lineal * 40 µm de gruix)) de les dues mostres per lòbul van ser llavors mitjana per a una comparació addicional entre lòbuls i animals. Les amplades de dendrites PN positives de Calbindin es van mesurar en una ubicació predefinida al lòbul VI de cada animal en seccions de teixit de 25 o 40 um de gruix amb un augment de 20x. Les amplades dendrítiques de les branques primàries i secundàries es van mesurar a la línia mitjana entre els cossos cel·lulars PN i la vora de la capa molecular. Es van mesurar entre 7 i 13 dendrites per secció, una secció per animal. Per a les mesures somàtiques de PN, es va utilitzar Stereo Investigator per seleccionar aleatòriament els PN distribuïts per tota la secció medial amb un augment de 20x. L'amplada mitjana de PN per animal es va determinar mitjançant la mitjana de resultats en 3 seccions en sèrie (de 16 a 37 PN per secció). L'amplada de la capa molecular i la capa de cèl·lules granulàries (visualitzades amb taques de Calbindin i DAPI, respectivament) es van avaluar a Stereo Investigator fent una mitjana de dues mesures d'amplada en ubicacions predefinides per a cada lòbul, aproximadament a la meitat, juntament amb l'extensió llarga de cada lòbul amb un augment de 2,5x. CD68 La positivitat a les seccions cerebel·lososes es va quantificar mesurant el percentatge total d'àrea de CD68 més la tinció positiva a tota la secció cerebel·losa medial. Les imatges cosides 10x es van llindar al control negatiu i es van quantificar mitjançant ImageJ, una secció per animal. Per quantificar el percentatge de PN positius per Calbindina que eren positius per a la caspasa escindida-3, vam comptar els PN a tot el cerebel mitjançant Stereo Investigator. Es van examinar tres imatges cosides amb augment de 20x per animal i es van promediar els resultats. El llindar per a la positivitat de la caspasa-3 es va establir a partir de seccions de control tenyides només amb els anticossos secundaris. Per a l'anàlisi histològica no fluorescent, 25-um gruixut, seccions de teixit flotant lliurement sobre portaobjectes carregats positivament i assecat a l'aire durant la nit. El teixit es va rentar amb solució salina tamponada amb fosfat (PBS) dues vegades durant 5 minuts, després es va tenyir seqüencialment amb hematoxilina al 0,1 per cent en etanol al 95 per cent durant ~ 25 segons i eosina al 0,5 per cent en etanol al 95 per cent durant ~ 3 segons i es va rentar amb aigua destil·lada doblement després. cada taca. Posteriorment, el teixit es va deshidratar durant 1 min en rentats d'etanol al 95 per cent, etanol al 100 per cent i xilè al 100 per cent, i després es va cobrir amb Permount. Les diapositives es van fotografiar mitjançant una càmera de color (Q Imaging, MBF Biosciences) al mateix microscopi Zeiss i programari d'adquisició MBF. Els experimentadors es van cegar al genotip del ratolí en què es van examinar les seccions i es va intercalar l'ordre d'examen per a totes les mesures histològiques.

4.7 Mesures de citometria de flux
L'anàlisi de citometria de flux de cèl·lules sanguínies i de tim es va realitzar tenyint amb anticossos específics anti-ratolí ∶ CD4, CD8, CD3, CD44 i CD25. Breument, es van tacar mostres de sang sencera (50 μ) amb anticossos marcats amb fluorescents, després es van lisar els glòbuls vermells mitjançant una solució de lisi BD mentre que els glòbuls blancs vius es van tacar amb una taca de viabilitat. Els timis es van dissociar mecànicament. D'1 a 2 milions de cèl·lules del timus es van tacar de manera similar mitjançant anticossos específics per a CD4, CD8, CD44 i CD25. L'anàlisi de glòbuls blancs immunotacats o mostres de tim es va realitzar mitjançant FACS ARIA l i les dades es van analitzar mitjançant el programari FlowJo tal com es va informar anteriorment (Sanghez et al. 2017).
4.8 Western BIots
Els extractes de proteïnes (cèl·lules/teixits) es van homogeneïtzar en un tampó de lisi d'assaig de radioimmunoprecipitació (RIPA) (NaCl 150 mM, 1% de Nonidet P-40 [NP-40],0 0,5% desoxicolat,0,1% SDS, 50 mM Tris, pH 8,0) amb inhibidors de la proteasa (10 ug/ml AEBSF, 10 ug/ml leupeptina, 5 ug/ml pepstatina, 5 ug/ml quimotripsina, 10 ug/ml d'aprotinina). Els extractes de proteïnes es van sonicar i després es van sedimentar per centrifugació a 13, 000 rpm durant 15 min a 4ºC. Es va utilitzar l'assaig de proteïnes BCA per quantificar les concentracions de proteïnes. Les mostres que contenien quantitats iguals de proteïna de 50 a 100 ug per carril es van separar mitjançant gels prefabricats TGX de gradient del 4 al 12 per cent i després es van transferir mitjançant el sistema TransBlot Semi-Dry BioRad mitjançant un paquet de transferència de nitrocel·lulosa. Les taques transferides es van tacar amb la tinció de Ponceau S per a una càrrega igual de proteïnes, després es van rentar i es van bloquejar amb un 5% de llet seca sense greix en TBST durant 60 min a temperatura ambient. Els anticossos primaris es van incubar amb agitació durant la nit a 4 graus. Es van sondar els anticossos següents: ATM (D2E2) Senyalització de cèl·lules mAb de conill, a una dilució 1:1000, -Actina (D6A8) Senyalització de cèl·lules mAb de conill, GAPDH (D16H11) Senyalització de cèl·lules mAb de conill seguit de la peroxidasa de rave picant adequada (- HRP) secundari Anti-conill, Anti-ratolí durant 2 hores a temperatura ambient. Després de diversos rentats amb TBST, es va detectar l'expressió de proteïnes mitjançant el substrat de quimioluminescència Radiance Plus mitjançant els sistemes d'imatge d'Azure c400 i BioRad ChemiDoc. L'anàlisi densitomètrica de l'ATM es va realitzar mitjançant ImageJ. Es van realitzar experiments amb 2 rèpliques tècniques i 2-3 biològiques tal com s'indica.

4.9 Avaluació estadística
El nombre d'animals escollits per a cada grup es va basar en anàlisis de potència a priori utilitzant GPower v3.1 basades en una mida de 0,5, potència de 0,8 i mides de l'efecte estimades a partir de dades preliminars o estudis previs. Hem utilitzat tant ANOVA paramètrics (1-i 2-via) per a mètodes estadístics distribuïts normalment i no paramètrics (Kruskal Wallace) per a dades d'interval per comprovar les diferències entre grups seguits de proves de comparació múltiple per parelles, tal com s'indica a el text. Valors atípics per a les dades immunes a les Figs. 6 i 7 es van excloure mitjançant el mètode ROUT (Q=2 per cent). Les anàlisis específiques utilitzades per a cada conjunt de dades s'anoten a la llegenda de cada figura. Per a totes les xifres: ns no significatiu,*p Menor o igual a 0,05,** p<0.01,***><0.001,****><0.0001. data="" are="" reported="" as="" mean="" ±="" sem="" and="" box="" and="" whisker="" plots="" indicate="" the="" minimum,="" first="" quartile,="" median,="" third="" quartile,="" and="" maximum="" data="" values.="" all="" figures="" and="" statistical="" analyses="" were="" completed="" using="" excel="" (microsoft="" 360)="" or="" prism="" v8="" and="" 9="">
