Impacte de les toxines urèmiques sobre la disfunció endotelial en la malaltia renal crònica: una revisió sistemàtica
Jun 30, 2023
Resum
Els pacients amb malaltia renal crònica (ERC) tenen un risc molt elevat de complicacions cardiovasculars, amb un augment de la inflamació vascular, una aterogènesi accelerada i un risc trombòtic millorat. Tenint en compte el paper central de l'endoteli en la protecció de l'aterogènesi i la trombosi, així com el seu paper cardioprotector en la regulació de la vasorelaxació, aquest estudi tenia com a objectiu integrar sistemàticament la literatura sobre la disfunció endotelial associada a la CKD, inclosos els mecanismes moleculars subjacents, en una visió general completa. Per tant, hem realitzat una revisió sistemàtica de la literatura que descriu sèrum urèmic o disfunció vascular induïda per toxina urèmica amb un enfocament especial a l'endoteli. Això va revelar 39 estudis que analitzaven els efectes del sèrum urèmic o de les toxines urèmiques sulfat d'indòxil, cianat, LDL modificat, els productes finals de glicació avançada N-carboximetil-lisina i N-carboxietil-lisina, p-cresol i p-cresil sulfat, fosfat, àcid úric i dimetilarginina asimètrica. La majoria dels estudis van descriure un augment de la inflamació, l'estrès oxidatiu, la migració i l'adhesió de leucòcits, la mort cel·lular i un fenotip trombòtic en condicions urèmiques o tractament amb toxina urèmica de cèl·lules endotelials. Les vies de senyalització cel·lular que s'activaven amb freqüència incloïen les vies ROS, MAPK/NF-κB, el receptor d'aril-hidrocarburs i les vies RAGE. En general, aquesta revisió proporciona una visió detallada dels mecanismes fisiopatològics i moleculars subjacents a la disfunció endotelial en la CKD. Orientar aquestes vies pot proporcionar noves estratègies terapèutiques per reduir l'augment del risc cardiovascular d'ERC.
Paraules clau
malaltia renal crònica; toxines urèmiques; disfunció vascular; fisiopatologia vascular; cèl·lules endotelials; disfunció endotelial; malaltia cardiovascular.

Feu clic aquí per saber quin és el benefici de Cistanche for Kidney
Introducció
A mesura que la funció renal disminueix gradualment, augmenta el risc de complicacions cardiovasculars. Això es reflecteix en el fet que aproximadament la meitat dels pacients amb malaltia renal crònica greu (estadi 4-5 d'ERC) moren per malaltia cardiovascular (ECV) [1], en comparació amb el 26% dels pacients amb una funció renal saludable [2,3]. ]. L'estenosi de la vàlvula aòrtica, la hipertròfia ventricular esquerra, la isquèmia miocàrdica i la insuficiència cardíaca són les principals causes de mort en pacients amb ERC [4]. Com a principal mecanisme subjacent de la isquèmia miocàrdica, els pacients amb ERC tenen un major risc d'aterosclerosi, un procés inflamatori dins de la capa íntima de la paret del vas [5]. En la CKD, la formació i la progressió d'aquestes lesions ateroscleròtiques són molt accelerades [6]. A més, a mesura que avança la CKD, la rigidesa vascular augmenta [7], amb la rigidesa vascular com a predictor important de la mortalitat cardiovascular en pacients amb CKD [8].
La disfunció endotelial és la base tant de l'aterosclerosi com de la rigidesa vascular i s'associa amb un augment del risc de mort cardiovascular [9]. La vasoreactivitat depenent de l'endotelial coronària es va identificar com a predictor de futurs esdeveniments cardiovasculars i progressió de la malaltia [10].
Les lesions ateroscleròtiques comencen com a pegats de cèl·lules endotelials (EC) disfuncionals [11]. A mesura que la barrera endotelial es torna disfuncional i perd la seva integritat, la permeabilitat augmenta i les lipoproteïnes de baixa densitat (LDL) s'acumulen dins de la paret del vaso, sobre les quals s'oxida la LDL i s'inicia un procés d'inflamació [12]. Les quimiocines es segreguen i les molècules d'adhesió s'expressen mitjançant EC inflamades, provocant el reclutament de leucòcits, la seva adhesió a les EC, així com la seva migració a la paret del vas [11, 13]. A més, l'augment de l'estrès oxidatiu i la producció d'espècies reactives d'oxigen (ROS) redueixen la biodisponibilitat de l'òxid nítric (NO) [13], que al seu torn provoca una reducció de la vasodilatació depenent de l'EC i, com a tal, un augment de la rigidesa vascular. Simultàniament, els EC disfuncionals perden les seves propietats antitrombòtiques i prevalen les propietats protrombòtiques, augmentant encara més el risc d'aterotrombosi [14]. A més, els EC disfuncionals mostren una capacitat de supervivència i proliferació reduïda, processos necessaris per restaurar la barrera endotelial protectora i contrarestar l'estenosi induïda per lesions després d'una lesió vascular [15,16]. Els processos fisiopatològics combinats d'inflamació, estrès oxidatiu, així com la supervivència deteriorada, la proliferació i la reparació d'EC contribueixen a la disfunció endotelial i les ECV (figura 1A).
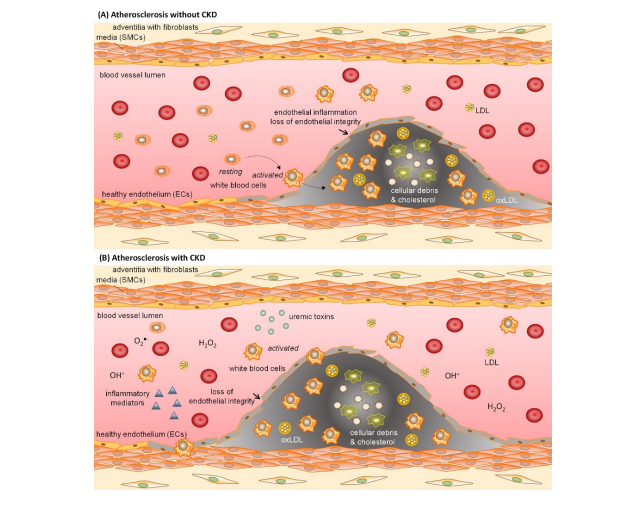
Figura 1. La inflamació endotelial i la pèrdua d'integritat endotelial contribueixen a la disfunció endotelial i a la formació de lesions ateroscleròtiques a la paret del vas. L'aterosclerosi es caracteritza per una inflamació endotelial i un augment de la permeabilitat vascular. Les cèl·lules endotelials inflamades segreguen quimiocines que recluten glòbuls blancs, que migren a través de la barrera endotelial disfuncional cap a la paret del vaso. A més, l'LDL migra a la paret del vas on s'oxida a ox-LDL (A). En pacients amb ERC, el procés de formació de lesions ateroscleròtiques està avançat a causa de factors associats a la CKD, com ara la inflamació sistèmica crònica de baix grau, l'augment dels marcadors d'estrès oxidatiu i l'oxidació de lipoproteïnes, així com l'acumulació de toxines urémiques, tot promovent el dany a la malaltia. la paret del vas (B). ECs=cèl·lules endotelials; LDL=lipoproteïna de baixa densitat; oxLDL=LDL oxidat; SMC=cèl·lules musculars llises.
Diversos estudis indiquen que els factors associats a la CKD, com la inflamació crònica sistèmica de baix grau, l'augment de l'estrès oxidatiu i les toxines urèmiques acceleren l'aterosclerosi en la CKD (figura 1B), tot i que els mecanismes moleculars subjacents no s'entenen completament [17, 18]. Els pacients amb CKD presenten inflamació sistèmica i crònica de baix grau, així com un augment de l'estrès oxidatiu fins i tot en les primeres etapes de la CKD [18–20], caracteritzat per alts nivells de proteïnes inflamatòries circulants (CRP, IL6) i biomarcadors d'estrès oxidatiu [19]. Com més progressa la CKD, més augmenten els nivells d'estrès oxidatiu [20]. A més, es va demostrar que els marcadors d'estrès oxidatiu (inclosos marcadors de peroxidació lipídica i propensió a l'oxidació de lipoproteïnes, entre d'altres) es correlacionen inversament amb la vasodilatació dependent de l'endotelial en pacients amb ERC, independentment dels factors de risc clàssics d'aterosclerosi com el gènere, l'edat, la pressió arterial, diabetis i tractament hipolipemiant [21]. La modificació dels lípids, com l'oxidació de LDL, augmenta en la CKD i afavoreix encara més el dany vascular [22]. A més, els alts nivells de fosfat típics dels trastorns ossis minerals relacionats amb la CKD causen disfunció endotelial canviant la morfologia de l'EC, disminuint la viabilitat i promovent la senescència [6].
En cas de disfunció renal, els soluts s'acumulen a la circulació que normalment són excretades pels ronyons. L'acumulació d'aquestes toxines urèmiques provoca una intoxicació endògena gradual. A la literatura, s'ha descrit que més de 140 toxines urèmiques s'elevaven a causa de la disfunció renal [23,24]. Les toxines urèmiques com el sulfat d'indòxil (IS) i el sulfat de p-cresil (PCS) s'han associat amb un major risc d'esdeveniments cardiovasculars i mortalitat cardiovascular en pacients amb ERC. Mecànicament, moltes d'aquestes toxines urèmiques s'han relacionat amb la inflamació i l'estrès oxidatiu [25,26], però també amb la rigidesa arterial i la disfunció endotelial in vitro [27]. Tenint en compte el paper central de l'endoteli en la preservació de la salut vascular i en la contraresta de l'aterosclerosi i el risc cardiovascular, aquest manuscrit va revisar sistemàticament la disfunció de l'EC induïda per la toxina urémica i les seves implicacions per a la malaltia cardiovascular específicament en el context de la CKD.

pastilles de Cistanche
Materials i mètodes
Aquesta revisió sistemàtica es fa segons les directrius proporcionades per la declaració PRISMA [28]. La llista de verificació PRISMA completada es pot trobar als Materials suplementaris.
1. Estratègia de cerca
Es va realitzar una cerca avançada de literatura a PubMed i Web of Science per a estudis que descriuen els mecanismes subjacents a la fisiopatologia vascular en la CKD, amb un enfocament especial en la disfunció endotelial induïda per la CKD. A més, per comparar els processos de senyalització patològics dins de diferents tipus de cèl·lules presents a les plaques ateroscleròtiques, es van recuperar estudis sobre la disfunció induïda per CKD de cèl·lules musculars llises, monòcits i macròfags. Es van avaluar els estudis publicats fins al juny de 2021. La taula suplementària S2 ofereix una visió general dels termes i condicions que es van utilitzar en la cerca bibliogràfica.
2. Criteris de selecció d'estudis
Dos revisors (EH i JW) van seleccionar de forma independent estudis que presentaven dades originals mitjançant criteris d'elegibilitat predefinits. Es van incloure estudis que descriuen mecanismes responsables de la disfunció vascular induïda per CKD per a una anàlisi posterior. Aquests estudis van descriure l'efecte del sèrum urèmic o de les toxines urèmiques individuals sobre la funció endotelial. També es van incloure informes sobre els efectes de la CKD en diferents tipus de cèl·lules presents a la placa ateroscleròtica. En el cas que es van mesurar marcadors de funció endotelial o vies de senyalització induïdes per la toxina urèmica en poblacions de pacients amb ERC, també es van incorporar aquests estudis de pacients. Es van excloure els duplicats, els articles de revisió, els resums de pòsters i els articles no escrits en anglès, així com els estudis que es van concentrar en la calcificació vascular induïda per la CKD o els estudis en què mancava una visió mecanicista. Tots dos revisors van haver de posar-se d'acord en la inclusió. En cas de desacord, es va consultar un tercer revisor (CB) per aconseguir consens. A la figura 2 es presenta una visió gràfica del nombre d'estudis inclosos i exclosos al llarg del procés de selecció.

Figura 2. Diagrama de flux de selecció d'estudis. Diagrama de flux de la selecció de treballs originals que il·lustra el nombre d'estudis inclosos i exclosos al llarg del procés de selecció.
3. Extracció de dades
Per resumir els efectes fisiopatològics de la urèmia o de les toxines urèmiques individuals sobre les cèl·lules endotelials, es van classificar els estudis en funció de les toxines investigades i els seus efectes clau sobre la funció endotelial. Aquests efectes clau es van definir com a inflamació, estrès oxidatiu, mort cel·lular, adhesió i migració de leucòcits, proliferació cel·lular i trombosi. Per a una descripció dels mecanismes moleculars subjacents a la disfunció endotelial induïda per la toxina urémica, es va extreure informació sobre les vies de senyalització d'estudis in vivo i in vitro. A partir d'estudis de pacients, es va extreure informació sobre marcadors de la funció endotelial o coneixements sobre les vies de senyalització induïdes per la toxina urèmica.

Cistanche tubulosa
Discussió
Els pacients amb ERC tenen un risc més elevat de desenvolupar ECV [104] i a mesura que la funció renal disminueix, el risc d'esdeveniments cardiovasculars augmenta i la funció endotelial disminueix [50,105]. Atès que la disfunció endotelial és clau en l'inici i la progressió de l'aterosclerosi i contribueix a la disminució de la reactivitat vascular, vam investigar la disfunció endotelial induïda per la toxina urèmica i els seus mecanismes subjacents mitjançant una revisió sistemàtica. En general, els processos cel·lulars afectats per condicions urèmiques o toxines urèmiques van ser la inflamació, la migració i l'adhesió de leucòcits, l'estrès oxidatiu, la mort cel·lular, la proliferació i la trombosi. A més, les toxines urèmiques semblaven compartir vies de senyalització comunes a les cèl·lules endotelials, incloses les vies vinculades a MAPK, AhR, el receptor RAGE o factors de transcripció proinflamatoris, per exemple, NF-κB. A més d'això, ROS com a transductor de senyal proinflamatori va ser compartit per múltiples toxines urèmiques.
p38-MAPK és un mediador conegut de l'expressió de citocines proinflamatòries i regulador de l'activació de NF-κB. Les toxines urèmiques com el senyal IS mitjançant p38-MAPK/NF-κB per induir l'expressió ICAM-1 o MCP{-1 i, per tant, contribueixen a les respostes inflamatòries de les cèl·lules endotelials [38,42,44] . El paper de NF-κB en l'alliberament de citocines induït per la toxina urèmica es va confirmar en macròfags per una expressió de TNF- NF-κB induïda per IS i AhR [40].
IS augmenta l'expressió intracel·lular d'AhR en diferents tipus de cèl·lules contribuint a la progressió de les ECV [37,40,68,69]. A més, IS, així com altres toxines urèmiques derivades del metabolisme del triptòfan, són lligands de AhR [106]. Es va demostrar que l'activació de la senyalització AhR a les cèl·lules endotelials millora una resposta inflamatòria tal com es demostra, per exemple, amb l'augment dels nivells d'expressió d'E-Selectina [37]. En pacients amb ERC, es va demostrar que l'E-Selectin sèrica era un predictor d'esdeveniments cardiovasculars, amb nivells elevats d'E-Selectin associats a un pitjor resultat [107]. A més, l'AhR com a contribuent a la ECV independent de la CKD es descriu en diversos estudis [108,109]. A més, l'expressió de RAGE a les cèl·lules endotelials va augmentar en resposta al sèrum urèmic [30], AGEs com CML [30,49,50] i pCS [30], induint disfunció endotelial i inflamació. En pacients amb ERC, l'augment dels nivells de CML es va correlacionar amb els nivells de proteïna RAGE mRNA i VCAM-1 i inversament amb la reactivitat endotelial [50]. En pacients sense ERC, l'associació entre l'augment de l'expressió de RAGE i ECV és controvertida [110], tanmateix, estudis in vitro van relacionar la senyalització de RAGE amb processos patològics cardiovasculars també en absència de CKD [111,112]. Combinat, això suggereix una amplificació tant de les vies AhR com de RAGE a causa de l'acumulació de toxines urèmiques a la CKD i, com a tal, una contribució més gran als processos inflamatoris i al desenvolupament de l'aterosclerosi.
Diferents toxines urèmiques com IS, fosfat, cianat, AGEs i àcid úric van provocar una disminució de l'expressió i/o activitat d'eNOS, donant lloc a una reducció de la producció de NO i una disminució de la vasorelaxació [42,45,49,50,55,60] . Com que el NO també és un inhibidor de trombòcits, la disminució dels nivells de NO en combinació amb l'augment del factor del teixit endotelial i l'expressió de PAI en resposta a l'augment de proteïnes carbamilades o cianats com cLDL, creen un entorn protrombòtic [45,47], que podria contribuir a la risc molt elevat d'esdeveniments trombòtics en pacients amb ERC [113,114].
A més, més enllà de les toxines urèmiques identificades mitjançant la nostra recerca sistemàtica de literatura, el factor de creixement de fibroblasts de l'hormona fosfatúrica 23 (FGF23) també està molt augmentat en la CKD i se sap que perjudica la vasorelaxació dependent de l'endotelial. Els mecanismes subjacents inclouen l'augment de la producció de ROS i la reducció de la biodisponibilitat de NO, molt probablement independentment del cofactor FGF23 Klotho [115,116]. En canvi, Klotho es redueix en pacients amb CKD i té principalment un paper protector a les cèl·lules endotelials donant suport a la producció de NO i la vasorelaxació, tal com es mostra tant en models animals de deficiència i sobreexpressió de Klotho com en experiments in vitro [116–120]. A més, Klotho és capaç de reduir la inflamació endotelial, també quan és induïda per IS, [40,121,122], i s'ha demostrat que redueix la permeabilitat endotelial i l'apoptosi [123]. En particular, les toxines urèmiques poden reduir els nivells de Klotho, per exemple, com es mostra per als AGE en podòcits de ratolí [124] i per a IS en SMC [125].

Cistanche estandarditzada
Un exemple clar de com les modificacions post-traduccionals poden contribuir al desenvolupament i progressió de l'aterosclerosi el proporcionen els efectes perjudicials de l'LDL oxidat a la paret vascular, provocant una disfunció endotelial [12]. Tanmateix, altres modificacions post-traduccionals també són importants en la mediació de les ECV, amb modificacions específiques catalitzades per toxines urèmiques [126]. Així, s'espera que la contribució d'aquestes modificacions post-traduccionals a les ECV sigui encara més rellevant en la ERC. A més d'afectar la funció de les cèl·lules endotelials, les modificacions post-traduccionals induïdes per la CKD també afecten negativament altres tipus de cèl·lules importants en les ECV. Per exemple, l'augment de l'acetilació de LDL en la CKD va provocar un augment de l'apoptosi dels macròfags induïda per l'estrès ER [87]. En conjunt, això demostra que es necessiten coneixements addicionals sobre les modificacions post-traduccionals induïdes per la CKD i els seus efectes patològics pel que fa a les ECV per permetre el desenvolupament d'estratègies per reduir les modificacions post-traduccionals induïdes per la CKD.
El que es desprèn de la nostra recerca bibliogràfica és que la majoria dels estudis van investigar l'efecte de les toxines urèmiques individuals sobre les funcions cel·lulars endotelials individuals o les vies de senyalització. Aquí, un enfocament de proteòmica, metabolòmica o combinat proporcionaria una visió àmplia del funcionament cel·lular i podria ajudar en el descobriment de nous mediadors i vies de senyalització implicades. A més, tot i que és important estudiar la toxina urèmica individual per dilucidar els mecanismes de senyalització subjacents, la vasculatura dels pacients amb CKD està exposada contínuament a una multitud de toxines urèmiques, que després combinades contribueixen a la disfunció endotelial; per tant, també s'hauria d'investigar la diafonia entre diferents toxines i les seves vies de senyalització combinant toxines o utilitzant sèrum urèmic o hemofiltració obtinguda després de la diàlisi de pacients amb ERC, per estudiar un espectre més ampli d'efectes cel·lulars induïts per la urèmia induïda per la CKD. Dels estudis identificats, dos estudis van investigar sèrum urèmic així com toxines individuals. Saum et al. va demostrar que un 10 per cent de sèrum urèmic, així com CML-BSA, van disminuir igualment l'expressió de KLF2; tanmateix, l'efecte de CML-BSA sobre la formació de ROS i l'adhesió de monòcits va ser més fort que el del sèrum urèmic [30]. Això es podria explicar per la dilució dels estudis de cèl·lules in vitro de sèrum urèmic, que resulta en concentracions més baixes de toxines urèmiques en comparació amb pacients amb insuficiència renal greu. A més, la composició tant del sèrum com de l'hemofiltració difereix dràsticament del plasma, a causa de la coagulació en el cas de la preparació del sèrum i, per a l'hemofiltració, per l'absència de metabòlits urèmics més grans que es retenen a la sang durant la diàlisi, així com la baixa diàlisi. eficiència cap a les toxines urèmiques unides a proteïnes. En general, ja sigui estudiant toxines urèmiques individuals, pools de toxines, sèrum urèmic o hemofiltració, no hi ha una solució perfecta per imitar les condicions d'ERC in vitro; cada enfocament té els seus avantatges i inconvenients, i aquests s'han de considerar en funció de l'objectiu específic de l'estudi a l'hora de dissenyar l'experiment.
Aquesta revisió subratlla la importància de millorar els tractaments de diàlisi actuals i desenvolupar estratègies noves i més eficients per eliminar les toxines urèmiques del torrent sanguini i, com a tal, aturar el dany endotelial induït per la toxina urèmica. Especialment, les toxines urèmiques unides a proteïnes com l'IS són notòriament difícils de dialitzar i la seva acumulació té conseqüències importants per a la salut endotelial, tal com es resumeix en aquesta revisió. Com que actualment no hi ha una tècnica universal que elimini de manera òptima tot tipus de toxines urèmiques (unides a proteïnes), calen més investigacions per millorar l'eliminació de la toxina urèmica i, per tant, millorar la salut cardiovascular dels pacients amb ERC. En l'última dècada, s'ha centrat en l'eliminació millorada de toxines urèmiques unides a proteïnes mitjançant tècniques d'adsorció, tal com s'ha comentat amb més detall en altres llocs. Aquesta revisió destaca les vies de senyalització que les toxines urèmiques utilitzen freqüentment per exercir efectes cel·lulars perjudicials, com a possible enfocament complementari per reduir la càrrega cardiovascular d'aquestes toxines urèmiques en la ERC.

Càpsules de Cistanche
Conclusions
En resum, aquesta revisió connecta els coneixements actuals sobre els mecanismes fisiopatològics i moleculars subjacents a l'augment del risc cardiovascular en la ERC, contribuint a una comprensió més profunda de la senyalització induïda per la toxina urémica i proporcionant indicacions sobre factors que s'han de tenir en compte en una anàlisi posterior dels efectes patològics induïts per la toxina urémica. . En general, l'acumulació de toxines urèmiques a la ERC desencadena la disfunció endotelial i contribueix a la inflamació, l'estrès oxidatiu, la trombosi i la mort cel·lular, accelerant així el desenvolupament i la progressió de les ECV. Les toxines urèmiques solen desencadenar vies dependents de ROS, MAPK/NF-κB, RAGE i/o AhR. Tot i que ja es coneixen en relació amb el desenvolupament de les ECV i també en absència d'ERC, aquesta revisió resumeix com les toxines urèmiques acceleren o amplifiquen aquests mecanismes patològics. Orientar aquestes vies, o interferir amb l'acumulació de toxines urémiques o les modificacions post-traduccionals induïdes per les toxines urémiques, pot obrir estratègies terapèutiques per reduir el risc cardiovascular molt augmentat en pacients amb ERC.
Referències
1. Stevens, P.; O'Donoghue, D.; de Lusignan, S.; Van Vlymen, J.; Klebe, B.; Middleton, R.; La Haia, N.; Nou, J.; Farmer, C. Gestió de la malaltia renal crònica al Regne Unit: resultats del projecte NEOERICA. Ronyó Int. 2007, 72, 92–99. [Ref creuat]
2. Drey, N.; Roderick, P.; Mullee, M.; Rogerson, M. Un estudi basat en la població de la incidència i els resultats de la malaltia renal crònica diagnosticada. Am. J. Ronyó Dis. 2003, 42, 677–684. [Ref creuat]
3. Thompson, S.; Jaume, M.; Wiebe, N.; Hemmelgarn, B.; Manns, B.; Klarenbach, S.; Tonelli, M. Causa de mort en pacients amb funció renal reduïda. Melmelada. Soc. Nefrol. 2015, 26, 2504–2511. [Ref creuat]
4. Masuda, C.; Dohi, K.; Sakurai, Y.; Bessho, Y.; Fukuda, H.; Fujii, S.; Sugimoto, T.; Tanabe, M.; Onishi, K.; Shiraki, K.; et al. Impacte de la malaltia renal crònica sobre la presència i la gravetat de l'estenosi aòrtica en pacients amb alt risc de malaltia arterial coronària. Cardiovasc. Ultrasò 2011, 9, 31. [CrossRef]
5. Hansson, GK; Hermansson, A. El sistema immunitari en l'aterosclerosi. Nat. Immunol. 2011, 12, 204–212. [Ref creuat]
6. Valdivielso, JM; Rodríguez-Puyol, D.; Pascual, J.; Barris, C.; Bermúdez-López, M.; Sánchez-Niño, MD; Pérez-Fernández, M.; Ortiz, A. L'aterosclerosi en la malaltia renal crònica: més, menys o només diferent? Arter. Tromb. Vasc. Biol. 2019, 39, 1938–1966. [Ref creuat]
7. Briet, M.; Bozec, E.; Laurent, S.; Fassot, C.; Londres, G.; Jacquot, C.; Froissart, M.; Houillier, P.; Boutouyrie, P. Rigidesa arterial i augment de la malaltia renal crònica lleu a moderada. Ronyó Int. 2006, 69, 350–357. [Ref creuat]
8. Temar, M.; Liabeuf, S.; Renard, C.; Czernichow, S.; El Esper, N.; Shahapuni, I.; Presne, C.; Makdassi, R.; Andrejak, M.; Tribouilloy, C.; et al. Velocitat de l'ona de pols i calcificació vascular en diferents estadis de la malaltia renal crònica. J. Hipertensos. 2010, 28, 163–169. [CrossRef] [PubMed]
9. Katz, SD; Hryniewicz, K.; Hriljac, I.; Balidemaj, K.; Dimayuga, C.; Hudaihed, A.; Yasskiy, A. Disfunció endotelial vascular i risc de mortalitat en pacients amb insuficiència cardíaca crònica. Circulació 2005, 111, 310–314. [CrossRef] [PubMed]
10. Schächinger, V.; Britten, MB; Zeiher, AM Impacte pronòstic de la disfunció vasodilatadora coronària sobre el resultat advers a llarg termini de la malaltia coronària. Circulació 2000, 101, 1899–1906. [Ref creuat]
11. Weber, C.; Noels, H. Atherosclerosis: Current pathogenesis and therapeutic options. Nat. Med. 2011, 17, 1410–1422. [CrossRef] [PubMed]
12. Soppert, J.; Lehrke, M.; Marx, N.; Jankowski, J.; Noels, H. Lipoproteïnes i lípids en malalties cardiovasculars: des de coneixements mecànics fins a l'orientació terapèutica. Adv. Entrega de drogues. Rev. 2020, 159, 4–33. [Ref creuat]
13. Cai, H.; Harrison, DG Disfunció endotelial en malalties cardiovasculars: el paper de l'estrès oxidant. Circ. Res. 2000, 87, 840–844. [CrossRef] [PubMed]
14. Tu, JW; Teoh, H.; Verma, S. Control endotelial de la trombosi. BMC Cardiovasc. Desordre. 2015, 15, 130. [CrossRef]
15. Hutter, R.; Carrick, FE; Valdiviezo, C.; Wolinsky, C.; Rudge, JS; Wiegand, SJ; Fuster, V.; Badimon, JJ; Sauter, BV El factor de creixement de l'endotelial vascular regula la reendotelialització i la formació de neoíntima en un model de ratolí de lesió arterial. Circulació 2004, 110, 2430–2435. [CrossRef] [PubMed]
16. Noels, H.; Zhou, B.; Tilstam, PV; Theelen, W.; Li, X.; Pawig, L.; Schmitz, C.; Akhtar, S.; Simsekyilmaz, S.; Shagdarsuren, E.; et al. La deficiència de Cxcr4 endotelial redueix la reendotelialització i millora la hiperplàsia neointimal després de lesions vasculars en ratolins propensos a l'aterosclerosi. Arter. Tromb. Vasc. Biol. 2014, 34, 1209–1220. [Ref creuat]
17. Vanholder, R.; Argilés, A.; Baurmeister, U.; Brunet, P.; Clark, W.; Cohen, G.; Dedeyn, P.; Deppisch, R.; Descamps-Latscha, B.; Henle, T.; et al. Toxicitat urémica: estat actual de la tècnica. Int. J. Artif. Orgues 2001, 24, 695–725. [Ref creuat]
18. Nowak, KL; Jovanovich, A.; Farmer-Bailey, H.; Bispham, N.; Struemph, T.; Malaczewski, M.; Wang, W.; Chochol, M. Disfunció vascular, estrès oxidatiu i inflamació en la malaltia renal crònica. Ronyó360 2020, 1, 501–509. [CrossRef] [PubMed]
19. Oberg, BP; McMenamin, E.; Lucas, FL; McMonagle, E.; Morrow, J.; Ikizler, TA; Himmelfarb, J. Augment de la prevalença de l'estrès oxidant i la inflamació en pacients amb malaltia renal crònica de moderada a severa. Ronyó Int. 2004, 65, 1009–1016. [Ref creuat]
20. Cachoeiro, V.; Goicochea, M.; de Vinuesa, SG; Oubiña, P.; Lahera, V.; Luño, J. L'estrès oxidatiu i la inflamació, un vincle entre la malaltia renal crònica i la malaltia cardiovascular. Ronyó Int. 2008, 74, S4–S9. [Ref creuat]
21. Annuk, M.; Zilmer, M.; Lind, L.; Linde, T.; Fellström, B. Estrès oxidatiu i funció endotelial en insuficiència renal crònica. Melmelada. Soc. Nefrol. 2001, 12, 2747–2752. [Ref creuat]
22. Noels, H.; Lehrke, M.; Vanholder, R.; Jankowski, J. Lipoproteïnes i àcids grassos en la malaltia renal crònica: alteracions moleculars i metabòliques. Nat. Reverent Nephrol. 2021, 17, 528–542. [Ref creuat]
23. Vanholder, R.; De Smet, R.; Glorieux, G.; Argilés, A.; Baurmeister, U.; Brunet, P.; Clark, W.; Cohen, G.; De Deyn, PP; Deppisch, R.; et al. Revisió de les toxines urèmiques: classificació, concentració i variabilitat interindividual. Ronyó Int. 2003, 63, 1934–1943. [Ref creuat]
24. Duranton, F.; Cohen, G.; De Smet, R.; Rodríguez, M.; Jankowski, J.; Vanholder, R.; Argiles, A.; en nom del Grup de Treball Europeu de Toxina Urèmica. Concentracions normals i patològiques de toxines urèmiques. Melmelada. Soc. Nefrol. 2012, 23, 1258–1270. [Ref creuat]
25. Watanabe, H.; Miyamoto, Y.; Honda, D.; Tanaka, H.; Wu, Q.; Endo, M.; Noguchi, T.; Kadowaki, D.; Ishima, Y.; Kotani, S.; et al. El sulfat de p-cresil causa dany a les cèl·lules tubulars renals induint estrès oxidatiu mitjançant l'activació de la NADPH oxidasa. Ronyó Int. 2013, 83, 582–592. [CrossRef] [PubMed]
26. Holmar, J.; De La Puente-Secades, S.; Floege, J.; Noels, H.; Jankowski, J.; Orth-Alampour, S. Toxines urèmiques que afecten la calcificació cardiovascular: una revisió sistemàtica. Cells 2020, 9, 2428. [CrossRef] [PubMed]
27. Dou, L.; Bertrand, E.; Cerini, C.; Faure, V.; Sampol, J.; Vanholder, R.; Berland, Y.; Brunet, P. Els soluts urèmics p-cresol i indoxil sulfat inhibeixen la proliferació endotelial i la reparació de ferides. Ronyó Int. 2004, 65, 442–451. [Ref creuat]
28. Moher, D.; Liberati, A.; Tetzlaff, J.; Altman, DG; El Grup PRISMA. Elements d'informe preferits per a revisions sistemàtiques i metaanàlisis: la declaració PRISMA. PLoS Med. 2009, 6, e1000097. [CrossRef] [PubMed]
29. Jeròtic, D.; Suvakov, S.; Matic, M.; Alqudah, A.; Grieve, DJ; Pljesa-Ercegovac, M.; Savic-Radojevic, A.; Damjanovic, T.; Dimkovic, N.; McClements, L.; et al. GSTM1 modula l'expressió de molècules d'adhesió endotelial en el entorn urèmic. Oxidativa Med. Cèl·lula. Longev. 2021, 2021, 6678924. [CrossRef]
30. Saum, K.; Campos, B.; Celdran-Bonafonte, D.; Nayak, L.; Sangwung, P.; Thakar, C.; Roy-Chaudhury, P.; OwensIII, AP Uremic Advanced Glycation End Products i soluts lligats a proteïnes indueixen una disfunció endotelial mitjançant la supressió del factor KrüppelLike 2. J. Am. Cor Assoc. 2018, 7, e007566. [CrossRef] [PubMed]
31. García-Jérez, A.; Luengo, A.; Carracedo, J.; Ramírez-Chamond, R.; Rodríguez-Puyol, D.; Rodríguez-Puyol, M.; Calleros, L. L'efecte de la urèmia sobre el dany de les cèl·lules endotelials està mediat per la via de la cinasa lligada a la integrina. J. Physiol. 2014, 593, 601–618. [Ref creuat]
32. Eloueyk, A.; Osta, B.; Alameldinne, R.; Awad, D. El sèrum urèmic indueix inflamació en cèl·lules endotelials humanes cultivades i desencadena mecanismes de reparació vascular. Inflamació 2019, 42, 2003–2010. [Ref creuat]
33. Nilsson, L.; Lundquist, P.; Kågedal, B.; Larsson, R. Concentracions de cianat plasmàtic en insuficiència renal crònica. Clin. Chem. 1996, 42, 482–483. [Ref creuat]
34. La base de dades europea de toxines urèmiques (EUTox). 2021. Disponible en línia: www.uremic-toxins.org (consultat l'1 de juny de 2021).
35. Speer, T.; Owala, FO; Sant, EW; Zewinger, S.; Frenzel, FL; Stähli, BE; Razavi, M.; Triem, S.; Cvija, H.; Rohrer, L.; et al. La lipoproteïna de baixa densitat carbamilada indueix una disfunció endotelial. Eur. Cor J. 2014, 35, 3021–3032. [Ref creuat]
36. Moore, LW; Nolte, JV; Gaber, AO; Suki, WN Associació de concentració de fosfat dietètic i fòsfor sèric per nivells de funció renal. Am. J. Clin. Nutr. 2015, 102, 444–453. [CrossRef] [PubMed]
37. Ito, S.; Osaka, M.; Edamatsu, T.; Itoh, Y.; Yoshida, M. Paper crucial del receptor d'hidrocarburs d'aril (AhR) en la inflamació vascular induïda per sulfat d'indoxy. J. Ateroescler. Tromb. 2016, 23, 960–975. [Ref creuat]
38. Masai, N.; Tatebe, J.; Yoshino, G.; Morita, T. El sulfat d'indoxyl estimula l'expressió de la proteïna quimioatraient monòcits-1 a les cèl·lules endotelials de la vena umbilical humana induint estrès oxidatiu mitjançant l'activació de la via NADPH oxidasa-factor nuclear-κB. Circ. J. 2010, 74, 2216–2224. [CrossRef] [PubMed]
39. Tumur, Z.; Shimizu, H.; Enomoto, A.; Miyazaki, H.; Niwa, T. El sulfat d'indoxyl regula l'expressió d'ICAM-1 i MCP-1 mitjançant l'activació de NF-kappa B induïda per l'estrès oxidatiu. Am. J. Nefrol. 2010, 31, 435–441. [CrossRef] [PubMed]
40. Kim, HY; Jo, T.-H.; Hwang, Y.; Lee, GH; Kim, B.; Jang, J.; Yu, HT; Kim, MC; Cho, JY; Lee, CJ; et al. La disfunció immune mediada per indoxil sulfat (IS) provoca danys endotelials en pacients amb malaltia renal terminal (ESRD). Ciència. Rep 2017, 7, 3057. [CrossRef]
41. Dou, L.; Jourde-Chiche, N.; Faure, V.; Cerini, C.; Berland, Y.; Dignat-George, F.; Brunet, P. El solut urémic indoxyl sulfate indueix estrès oxidatiu a les cèl·lules endotelials. J. Tromb. Haemost. 2007, 5, 1302–1308. [Ref creuat]
42. Yang, K.; Nie, L.; Huang, Y.; Zhang, J.; Xiao, T.; Guan, X.; Zhao, J. Millora de la disfunció de les cèl·lules endotelials induïda per la toxina urémica indoxil sulfat per la proteïna Klotho. Toxicol. Lett. 2012, 215, 77–83. [CrossRef] [PubMed]
43. Li, S.; Xie, Y.; Yang, B.; Huang, S.; Zhang, Y.; Jia, Z.; Ding, G.; Zhang, A. MicroRNA-214 s'adreça a COX-2 per antagonitzar l'apoptosi de cèl·lules endotelials induïda per indoxil sulfat (IS). Apoptosi 2019, 25, 92–104. [CrossRef] [PubMed]
44. El-Gamal, D.; Holzer, M.; Gauster, M.; Schicho, R.; Enquadernador, V.; Konya, V.; Wadsack, C.; Schuligoi, R.; Heinemann, A.; Marsche, G. El cianat és un nou inductor de l'expressió ICAM-1 endotelial. Antiòxid. Senyal redox. 2012, 16, 129–137. [Ref creuat]
45. El-Gamal, D.; Rao, SP; Holzer, M.; Hallström, S.; Haybaeck, J.; Gauster, M.; Wadsack, C.; Kozina, A.; Frank, S.; Schicho, R.; et al. El producte de descomposició de la urea cianat promou la disfunció endotelial. Ronyó Int. 2014, 86, 923–931. [Ref creuat]
46. Ambrosch, A.; Müller, R.; Freytag, C.; Borgmann, S.; Kraus, J.; Dierkes, J.; Neumann, KH; König, W. Les lipoproteïnes de baixa densitat de mida petita de la subclasse B de pacients amb malaltia renal en fase terminal augmenten eficaçment les propietats adhesives induïdes del factor de necrosi tumoral- -a les cèl·lules endotelials humanes. Am. J. Ronyó Dis. 2002, 39, 972–984. [Ref creuat]
47. Sant, EW; Akhmedov, A.; Speer, T.; Camici, GG; Zewinger, S.; Bonetti, N.; Cervesa, JH; Lüscher, TF; Tanner, FC Les lipoproteïnes de baixa densitat carbamilades indueixen un estat protrombòtic mitjançant LOX-1 Impacte en la formació de trombos arterials in vivo. Melmelada. Coll. Cardiol. 2016, 68, 1664–1676. [Ref creuat]
48. Apostolov, EO; Ray, D.; Alobuia, WM; Mikhailova, MV; Wang, X.; Basnakian, AG; Shah, SV L'endonucleasa G media la mort de les cèl·lules endotelials induïda per LDL carbamilada. Am. J. Physiol. Circ. Physiol. 2011, 300, H1997–H2004. [Ref creuat]
49. Wang, C.-C.; Lee, A.-S.; Liu, S.-H.; Chang, K.-C.; Shen, M.-Y.; Chang, C.-T. L'espironolactona millora la disfunció endotelial mitjançant la inhibició de l'eix AGE/RAGE en un model de rata d'insuficiència renal crònica. BMC Nephrol. 2019, 20, 351. [CrossRef]
50. Linden, E.; Cai, W.; Ell, JC; Xue, C.; Li, Z.; Winston, J.; Vlassara, H.; Uribarri, J. Disfunció endotelial en pacients amb malaltia renal crònica. Resultats de la inhibició mediada de productes finals de glicació avançada (AGE) de la sintasa d'òxid nítric endotelial mitjançant l'activació de RAGE. Clin. Melmelada. Soc. Nefrol. 2008, 3, 691–698. [CrossRef] [PubMed]
51. Zhu, J.; Yang, K.; Jing, Y.; Du, R.; Zhu, Z.; Lu, L.; Zhang, R. Els efectes de dosis baixes de Nepsilon-(carboximetil)lisina (CML) i Nepsilon-(carboxietil)lisina (CEL), dos principals adductes lliures de glicació considerats com a potencials toxines urèmiques, sobre la funció de les cèl·lules progenitores endotelials. Cardiovasc. Diabetol. 2012, 11, 90. [CrossRef] [PubMed]
52. Jing, YJ; Ni, JW; Ding, FH; Fang, YH; Wang, XQ; Wang, HB; Chen, XN; Chen, N.; Zhan, WW; Lu, L.; et al. El sulfat de p-cresil s'associa amb l'arteriosclerosi caròtida en pacients amb hemodiàlisi i promou l'aterogènesi en ratolins apoE–/–. Ronyó Int. 2016, 89, 439–449. [Ref creuat]
53. Watanabe, H.; Miyamoto, Y.; Enoki, Y.; Ishima, Y.; Kadowaki, D.; Kotani, S.; Nakajima, M.; Tanaka, M.; Matsushita, K.; Mori, Y.; et al. El sulfat de p-cresil, una toxina urémica, provoca danys en les cèl·lules endotelials i musculars llises induint estrès oxidatiu. Pharmacol. Res. Perspectiva. 2014, 3, e00092. [Ref creuat]
54. Meijers, BKI; Van Kerckhoven, S.; Verbeke, K.; Dehaen, W.; Vanrenterghem, Y.; Hoylaerts, MF; Evenepoel, P. El solut de retenció urèmica sulfat de p-cresil i marcadors de dany endotelial. Am. J. Ronyó Dis. 2009, 54, 891–901. [Ref creuat]
55. Peng, A.; Wu, T.; Zeng, C.; Rakheja, D.; Zhu, J.; Sí, T.; Hutcheson, J.; Vaziri, ND; Liu, Z.; Mohan, C.; et al. Efectes adversos de la hiper- i hipo-fosfatèmia simulada sobre la funció i la viabilitat de les cèl·lules endotelials. PLoS ONE 2011, 6, e23268. [CrossRef] [PubMed]
56. Hsu, Y.-J.; Hsu, S.-C.; Huang, S.-M.; Lee, H.-S.; Lin, S.-H.; Tsai, C.-S.; Shih, C.-C.; Lin, C.-Y. La hiperfosfatèmia indueix autofàgia protectora a les cèl·lules endotelials mitjançant la inhibició de la senyalització Akt/mTOR. J. Vasc. Surg. 2014, 62, 210–221.e2. [Ref creuat]
57. Abbasian, N.; Burton, J.; Herbert, K.; Tregunna, B.-E.; Brown, JR; Ghaderi-Najafabadi, M.; Brunskill, NJ; Goodall, A.; Bevington, A. Hiperfosfatèmia, fosfoproteïna fosfatases i alliberament de micropartícules en cèl·lules endotelials vasculars. Melmelada. Soc. Nefrol. 2015, 26, 2152–2162. [CrossRef] [PubMed]
58. Guo, W.; Diao, Z.; Liu, W. La dimetilarginina asimètrica regula a la baixa el calci-ATPasa 3 del reticle sarco/endoplasmàtic i indueix l'estrès del reticle endoplasmàtic a les cèl·lules endotelials de la vena umbilical humana. Mol. Med. Rep. 2017, 16, 7541–7547. [CrossRef] [PubMed]
59. Zhang, Y.; Hong, Q.; Huang, Z.; Xue, P.; Lv, Y.; Fu, B.; Chen, X.; Wu, D. ALDR Enhanced Endothelial Injury in Hyperuricemia Screened using SILAC. Cèl·lula. Physiol. Bioquímica. 2014, 33, 479–490. [Ref creuat]
60. Li, P.; Zhang, L.; Zhang, M.; Zhou, C.; Lin, N. L'àcid úric millora la fosforilació d'eNOS depenent de PKC i media l'estrès ER cel·lular: un mecanisme per a la disfunció endotelial induïda per l'àcid úric. Int. J. Mol. Med. 2016, 37, 989–997. [CrossRef] [PubMed]
61. Komori, H.; Yamada, K.; Tamai, I. La hiperuricèmia millora l'acumulació intracel·lular d'urat mitjançant la regulació a la baixa de l'expressió BCRP/ABCG2 a la superfície cel·lular a les cèl·lules endotelials vasculars. Biochim. Biofísica. Acta (BBA)-Biomembr. 2018, 1860, 973–980. [Ref creuat]
62. Pawlak, K.; Kowalewska, A.; Mysliwiec, M.; Pawlak, D. 3-L'àcid hidroxiantranílic s'associa de manera independent amb la proteïna quimioatraient monòcits-1 (CCL2) i la proteïna inflamatòria dels macròfags-1 beta (CCL4) en pacients amb malaltia renal crònica. Clin. Bioquímica. 2010, 43, 1101–1106. [Ref creuat]
63. Frericks, M.; Meissner, M.; Esser, C. Anàlisi de microarrays del sistema AHR: flexibilitat específica del teixit en gens senyal i diana. Toxicol. Appl. Pharmacol. 2007, 220, 320–332. [Ref creuat]
64. Stockinger, B.; Di Meglio, P.; Gialitakis, M.; Duarte, JH El receptor d'hidrocarburs arils: multitasca en el sistema immunitari. Ann. Reverent Immunol. 2014, 32, 403–432. [CrossRef] [PubMed]
65. Vogel, CFA; Sciullo, E.; Matsumura, F. Activació dels mediadors inflamatoris i el paper potencial dels lligands del receptor Ah en la formació de cèl·lules d'escuma. Cardiovasc. Toxicol. 2004, 4, 363–374. [Ref creuat]
66. Vogel, CFA; Sciullo, E.; Wong, P.; Kuzmicky, P.; Kado, N.; Matsumura, F. Inducció de citocines proinflamatòries i proteïna C reactiva en la línia cel·lular de macròfags humans U937 exposada a partícules de contaminació de l'aire. Entorn. Perspectiva de la Salut. 2005, 113, 1536–1541. [CrossRef] [PubMed]
67. Wu, D.; Nishimura, N.; Kuo, V.; Fiehn, O.; Shahbaz, S.; Van Winkle, L.; Matsumura, F.; Vogel, CFA L'activació del receptor d'hidrocarburs aril indueix la inflamació vascular i promou l'aterosclerosi en ratolins apolipoproteïnes E–/–. Arter. Tromb. Vasc. Biol. 2011, 31, 1260–1267. [Ref creuat]
68. Wakamatsu, T.; Yamamoto, S.; Ito, T.; Sato, Y.; Matsuo, K.; Takahashi, Y.; Kaneko, Y.; Goto, S.; Kazama, JJ; Gejyo, F.; et al. El sulfat d'indoxyl afavoreix la producció de macròfag IL-1 activant les cascades del receptor d'hidrocarburs aril/NF-κ/MAPK, però l'inflamsoma NLRP3 no es va activar. Toxines 2018, 10, 124. [CrossRef] [PubMed]
69. Kim, HY; Jo, TH; Cho, JY; Kim, HC; Lee, WW El TNF-alfa induït per indoxil sulfat està regulat per la diafonia entre el receptor d'hidrocarburs aril, NF-kappa B i SOCS2 en macròfags humans. FASEB J. 2019, 33, 10844–10858. [CrossRef] [PubMed]
70. Dou, L.; Sallée, M.; Cerini, C.; Poitevin, S.; Gondouin, B.; Jourde-Chiche, N.; Fallague, K.; Brunet, P.; Calaf, R.; Dussol, B.; et al. L'efecte cardiovascular del solut urèmic àcid indol-3 acètic. Melmelada. Soc. Nefrol. 2014, 26, 876–887. [Ref creuat]
71. Brito, JSD; Borges, NA; Anjos, JSD; Nakao, LS; Stockler-Pinto, MB; Paiva, BR; Cardoso-Weide, LDC; Cardozo, LFMDF; Mafra, D. Receptor d'hidrocarburs aril i toxines urèmiques de la microbiota intestinal en pacients amb malaltia renal crònica: hi ha una relació entre ells? Bioquímica 2019, 58, 2054–2060. [Ref creuat]
72. Shah, SV; Shukla, AM; Bose, C.; Basnakian, AG; Rajapurkar, M. Avenços recents en la comprensió de la patogènesi de l'aterosclerosi en pacients amb ERC. J. Ren. Nutr. 2015, 25, 205–208. [CrossRef] [PubMed]
73. Lin, C.-Y.; Hsu, S.-C.; Lee, H.-S.; Lin, S.-H.; Tsai, C.-S.; Huang, S.-M.; Shih, C.-C.; Hsu, Y.-J. Expressió millorada del transportador de glucosa -1 a les cèl·lules musculars llises vasculars mitjançant la subunitat 2 del complex Akt/esclerosi tuberosa (TSC2)/objectiu de mamífers de la via rapamicina (mTOR)/proteïna quinasa S6 ribosòmica (S6K) en la insuficiència renal experimental. J. Vasc. Surg. 2013, 57, 475–485. [CrossRef] [PubMed]
74. Bell, J.; Lee, J.; Lee, H.; Sadler, P.; Wilkie, D.; Woodham, R. Estudis de ressonància magnètica nuclear de plasma sanguini i orina de subjectes amb insuficiència renal crònica: identificació de trimetilamina-N-òxid. Biochim. Biofísica. Acta (BBA)-Mol. Base Dis. 1991, 1096, 101–107. [Ref creuat]
75. Blackmore, DJ; Elder, WJ; Bowden, CH Distribució de la urea en la insuficiència renal. J. Clin. Pathol. 1963, 16, 235–243. [Ref creuat]
76. Wang, Z.; Nicholls, S.; Rodríguez, ER; Kummu, O.; Hörkkö, S.; Barnard, JW; Reynolds, WF; Topol, E.; DiDonato, JA; Hazen, SL La carbamilació de proteïnes enllaça la inflamació, el tabaquisme, la urèmia i l'aterogènesi. Nat. Med. 2007, 13, 1176–1184. [CrossRef] [PubMed]
77. Arlandson, M.; Decker, T.; Roongta, VA; Bonilla, L.; Mayo, KH; MacPherson, JC; Hazen, SL; Slungaard, A. Eosinòfil peroxidasa oxidació del tiocianat. Caracterització dels principals productes de reacció i un potencial sistema de citotoxicitat dirigit a sulfhidril. J. Biol. Chem. 2001, 276, 215–224. [Ref creuat]
78. Baldus, S.; Eiserich, JP; Mani, A.; Castro, L.; Figueroa, M.; Chumley, P.; Ma, W.; Tousson, A.; blanc, CR; Bullard, DC; et al. La transcitosi endotelial de la mieloperoxidasa confereix especificitat a les proteïnes ECM vasculars com a objectius de la nitració de tirosina. J. Clin. Investig. 2001, 108, 1759–1770. [CrossRef] [PubMed]
79. Kalim, S.; Karumanchi, SA; Thadhani, RI; Berg, AH Carbamilació de proteïnes en malaltia renal: patogènesi i implicacions clíniques. Am. J. Ronyó Dis. Apagat. J. Natl. Trobat ronyó. 2014, 64, 793–803. [Ref creuat]
80. Apostolov, EO; Ray, D.; Savenka, AV; Shah, SV; Basnakian, AG La urèmia crònica estimula la carbamilació de LDL i l'aterosclerosi. Melmelada. Soc. Nefrol. 2010, 21, 1852–1857. [Ref creuat]
81. Apostolov, EO; Shah, SV; Ray, D.; Basnakian, AG Scavenger Receptors de cèl·lules endotelials medien l'absorció i els efectes proaterogènics cel·lulars de la LDL carbamilada. Arter. Tromb. Vasc. Biol. 2009, 29, 1622–1630. [Ref creuat]
82. Basnakian, AG; Shah, SV; D'acord, E.; Altunel, E.; Apostolov, EO LDL carbamilat. Adv. Clin. Chem. 2010, 51, 25–52. [PubMed]
83. Gonen, B.; Goldberg, AP; Harter, RRHH; Schonfeld, G. Propietats anormals interactives amb cèl·lules de les lipoproteïnes de baixa densitat aïllades de pacients amb insuficiència renal crònica. Metabolisme 1985, 34, 10–14. [Ref creuat]
84. Hörkkö, S.; Huttunen, K.; Kervinen, K.; Kesäniemi, YA Disminució de l'eliminació de la lipoproteïna de baixa densitat urèmica i lleugerament carbamilada. Eur. J. Clin. Investig. 1994, 24, 105–113. [Ref creuat]
85. D'acord, E.; Basnakian, AG; Apostolov, EO; Barri, YM; Shah, SV La lipoproteïna de baixa densitat carbamilada indueix la mort de les cèl·lules endotelials: un enllaç amb l'aterosclerosi en pacients amb malaltia renal. Ronyó Int. 2005, 68, 173–178. [Ref creuat]
86. Chu, M.; Wang, AYM; Chan, IHS; Chui, SH; Lam, CWK Anomalies de LDL denses petites en sèrum en pacients amb malaltia renal crònica. Br. J. Biomed. Ciència. 2012, 69, 99–102. [Ref creuat]
87. Tao, J.-L.; Ruan, X.-Z.; Li, H.; Li, X.-M.; Moorhead, JF; Varghese, Z. L'estrès del reticle endoplasmàtic està implicat en l'apoptosi induïda per lipoproteïnes de baixa densitat acetilades en macròfags diferenciats amb THP-1. Barbeta. Med. J. 2009, 122, 1794–1799.
88. Miyata, T.; Strihou, CVYD; Kurokawa, K.; Baynes, JW Alteracions en bioquímica no enzimàtica en urèmia: origen i significació de l'"estrès carbonílic" en complicacions urèmiques a llarg termini. Ronyó Int. 1999, 55, 389–399. [Ref creuat]
89. Peppa, M.; Uribarri, J.; Cai, W.; Lu, M.; Vlassara, H. Glicoxidació i inflamació en pacients amb insuficiència renal. Am. J. Ronyó Dis. 2004, 43, 690–695. [Ref creuat]
90. Martínez, AW; Recht, NS; Hostetter, TH; Meyer, TW Eliminació del sulfat de P-Cresol per hemodiàlisi. Melmelada. Soc. Nefrol. 2005, 16, 3430–3436. [Ref creuat]
91. Meijers, B.; Bammens, B.; De Moor, B.; Verbeke, K.; Vanrenterghem, Y.; Evenepoel, P. El p-cresol lliure s'associa amb malalties cardiovasculars en pacients amb hemodiàlisi. Ronyó Int. 2008, 73, 1174–1180. [Ref creuat]
92. Watanabe, H.; Sakaguchi, Y.; Sugimoto, R.; Kaneko, K.-I.; Iwata, H.; Kotani, S.; Nakajima, M.; Ishima, Y.; Otagiri, M.; Maruyama, T. Els transportadors d'anions orgànics humans funcionen com un transportador d'alta capacitat per al sulfat de p-cresil, una toxina urémica. Clin. Exp. Nefrol. 2013, 18, 814–820. [Ref creuat]
93. Giachelli, CM; Speer, MEU; Li, X.; Rajachar, RM; Yang, H. Regulació de la calcificació vascular: rols del fosfat i l'osteopontina. Circ. Res. 2005, 96, 717–722. [Ref creuat]
94. Mizobuchi, M.; Towler, D.; Slatopolsky, E. Calcificació vascular: l'assassí de pacients amb malaltia renal crònica. Melmelada. Soc. Nefrol. 2009, 20, 1453–1464. [CrossRef] [PubMed]
95. Martínez-Moreno, JM; Muñoz-Castañeda, JR; Herencia, C.; De Oca, AM; Estepa, JC; Canalejo, R.; Rodríguez-Ortiz, ME; Martínez, PP; Aguilera-Tejero, E.; Canalejo, A.; et al. A les cèl·lules musculars llises vasculars, el paricalcitol impedeix l'activació de Wnt/-catenina induïda per fosfats. Am. J. Physiol. Physiol. 2012, 303, F1136–F1144. [CrossRef] [PubMed]
96. Martínez-Moreno, JM; Herencia, C.; de Oca, AM; Díaz-Tocados, JM; Vergara, N.; Gómez-Luna, MJ; López-Argüello, SD; Camargo, A.; Peralbo-Santaella, E.; Rodríguez-Ortiz, ME; et al. Un alt fosfat indueix una resposta proinflamatòria per part de les cèl·lules musculars llises vasculars i la modulació per derivats de la vitamina D. Clin. Ciència. 2017, 131, 1449–1463. [Ref creuat]
97. Konya, H.; Miuchi, M.; Satani, K.; Matsutani, S.; Yano, Y.; Tsunoda, T.; Ikawa, T.; Matsuo, T.; Ochi, F.; Kusunoki, Y.; et al. Dimetilarginina asimètrica, un biomarcador de complicacions cardiovasculars en la diabetis mellitus. Món J. Exp. Med. 2015, 5, 110–119. [Ref creuat]
98. Böger, RH; Maas, R.; Schulze, F.; Schwedhelm, E. Dimetilarginina asimètrica (ADMA) com a marcador prospectiu de malalties cardiovasculars i mortalitat: una actualització de les poblacions de pacients amb una àmplia gamma de risc cardiovascular. Pharmacol. Res. 2009, 60, 481–487. [Ref creuat]
99. Woehlbier, U.; Hetz, C. Modulant les respostes a l'estrès per part de l'UPRosome: una qüestió de vida o mort. Tendències Bioquímica. Ciència. 2011, 36, 329–337. [Ref creuat]
100. Walter, P.; Ron, D. La resposta proteica desplegada: de la via de l'estrès a la regulació homeostàtica. Ciència 2011, 334, 1081–1086. [Ref creuat]
101. Snauwaert, E.; Holvoet, E.; Van Biesen, W.; Raes, A.; Glorieux, G.; Walle, JV; Roels, S.; Vanholder, R.; Askiti, V.; Azukaitis, K.; et al. Les concentracions de toxina urémica estan relacionades amb la funció renal residual en la població pediàtrica en hemodiàlisi. Toxines 2019, 11, 235. [CrossRef] [PubMed]
102. Kanbay, M.; Segal, M.; Afsar, B.; Kang, D.-H.; Rodríguez-Iturbe, B.; Johnson, RJ El paper de l'àcid úric en la patogènesi de la malaltia cardiovascular humana. Cor 2013, 99, 759–766. [CrossRef] [PubMed]
103. Ryu, E.-S.; Kim, MJ; Shin, H.-S.; Jang, Y.-H.; Choi, HS; Jo, I.; Johnson, RJ; Kang, D.-H. La transició fenotípica induïda per l'àcid úric de les cèl·lules tubulars renals com a nou mecanisme de malaltia renal crònica. Am. J. Physiol. Ren. Physiol. 2013, 304, F471–F480. [CrossRef] [PubMed]
104. Sarnak, MJ; Levey, AS; Schoolwerth, AC; Coresh, J.; Culleton, B.; Hamm, LL; McCullough, PA; Kasiske, BL; Kelepouris, E.; Klag, MJ; et al. La malaltia renal com a factor de risc per al desenvolupament de la malaltia cardiovascular. Circulació 2003, 108, 2154–2169. [CrossRef] [PubMed]
105. Ortiz, PA; Covic, A.; Fliser, D.; Fouque, D.; Orfebre, D.; Kanbay, M.; Mallamaci, F.; Massy, ZA; Rossignol, P.; Vanholder, R.; et al. Epidemiologia, col·laboradors i assaigs clínics de risc de mortalitat en insuficiència renal crònica. Lancet 2014, 383, 1831–1843. [Ref creuat]
106. Sallée, M.; Dou, L.; Cerini, C.; Poitevin, S.; Brunet, P.; Burtey, S. L'efecte activador del receptor d'hidrocarburs aril de les toxines urèmiques del metabolisme del triptòfan: un nou concepte per entendre les complicacions cardiovasculars de la malaltia renal crònica. Toxines 2014, 6, 934–949. [Ref creuat]
107. Malatino, LS; Stancanelli, B.; Cataliotti, A.; Villanueva, I.; Fatuzzo, PM; Rapisarda, FA; Leonardis, D.; Tripepi, G.; Mallamaci, F.; Zoccali, C. E-selectina circulant com a marcador de risc en pacients amb malaltia renal terminal. J. Intern. Med. 2007, 262, 479–487. [Ref creuat]
108. Yi, T.; Wang, J.; Zhu, K.; Tang, Y.; Huang, S.; Shui, X.; Ding, Y.; Chen, C.; Lei, W. Aryl Hydrocarbon Receptor: Un nou jugador de patogènesi i teràpia en malalties cardiovasculars. BioMed Res. Int. 2018, 2018, 6058784. [CrossRef]
109. Zhu, K.; Meng, Q.; Zhang, Z.; Yi, T.; Ell, Y.; Zheng, J.; Lei, W. Aryl via del receptor d'hidrocarburs: paper, regulació i intervenció en la teràpia de l'aterosclerosi (revisió). Mol. Med. Rep. 2019, 20, 4763–4773. [Ref creuat]
110. Reichert, S.; Triebert, EUA; Santos, AN; Hofmann, B.; Schaller, H.-G.; Schlitt, A.; Schulz, S. Forma soluble de receptor per a productes finals de glicació avançada i incidència de nous esdeveniments cardiovasculars entre pacients amb malaltia cardiovascular. Aterosclerosi 2017, 266, 234–239. [Ref creuat]
111. Uekita, H.; Ishibashi, T.; Shiomi, M.; Koyama, H.; Ohtsuka, S.; Yamamoto, H.; Yamagishi, S.; Inoue, H.; Itabe, H.; Sugimoto, K.; et al. El paper integral del receptor de productes finals de glicació avançada (RAGE) en l'aterosclerosi no diabètica. Fukushima J. Med. Ciència. 2019, 65, 109–121. [Ref creuat]
112. Jandeleit-Dahm, K.; Cooper, ME El paper dels AGE en les malalties cardiovasculars. Curr. Farmàcia. Des. 2008, 14, 979–986. [Ref creuat]
113. Baaten, CC; Sternkopf, M.; Henning, T.; Marx, N.; Jankowski, J.; Noels, H. Funció plaquetària en ERC: una revisió sistemàtica i metaanàlisi. Melmelada. Soc. Nefrol. 2021, 32, 1583–1598. [Ref creuat]
114. Silswal, N.; Touchberry, CD; Daniel, DR; McCarthy, DL; Zhang, S.; Andresen, J.; Stubbs, JR; Wacker, MJ FGF23 afecta directament la vasorelaxació dependent de l'endoteli augmentant els nivells de superòxid i reduint la biodisponibilitat de l'òxid nítric. Am. J. Physiol. Metab. 2014, 307, E426–E436. [Ref creuat]
115. Sis, I.; Okazaki, H.; Brut, P.; Cagnard, J.; Boudot, C.; Maizel, J.; Drueke, TB; Massy, ZA Direct, efectes aguts de Klotho i FGF23 sobre el múscul llis vascular i l'endoteli. PLoS ONE 2014, 9, e93423.
116. Saito, Y.; Yamagishi, T.; Nakamuraa, T.; Ohyamaa, Y.; Aizawaa, H.; Sugaa, T.; Matsumuraab, Y.; Masudaab, H.; Kurabayashia, M.; Kuro-Ob, M.; et al. La proteïna Klotho protegeix contra la disfunció endotelial. Bioquímica. Biofísica. Res. Commun. 1998, 248, 324–329. [Ref creuat]
117. Nagai, R.; Saito, Y.; Ohyama, Y.; Aizawa, H.; Suga, T.; Nakamura, T.; Kurabayashi, M.; Kuro-o, M. Disfunció endotelial en el ratolí Klotho i regulació a la baixa de l'expressió del gen klotho en diversos models animals de malalties vasculars i metabòliques. Cèl·lula. Mol. Ciència de la vida. 2000, 57, 738–746. [Ref creuat]
118. Shimada, T.; Takeshita, Y.; Murohara, T.; Sasaki, K.-I.; Egami, K.; Shintani, S.; Katsuda, Y.; Ikeda, H.; Nabeshima, Y.-I.; Imaizumi, T. L'angiogènesi i la vasculogènesi es veuen alterades en el ratolí klotho d'envelliment precoç. Circulació 2004, 110, 1148–1155. [CrossRef] [PubMed]
119. Saito, Y.; Nakamura, T.; Ohyama, Y.; Suzuki, T.; Iida, A.; Shiraki-Iida, T.; Kuro-o, M.; Nabeshima, Y.-I.; Kurabayashi, M.; Nagai, R. In Vivo, el lliurament de gens klotho protegeix contra la disfunció endotelial en la síndrome de múltiples factors de risc. Bioquímica. Biofísica. Res. Commun. 2000, 276, 767–772. [CrossRef] [PubMed]
120. Maekawa, Y.; Ishikawa, K.; Yasuda, O.; Oguro, R.; Hanasaki, H.; Kida, I.; Takemura, Y.; Ohishi, M.; Katsuya, T.; Rakugi, H. Klotho suprimeix l'expressió induïda per TNF-alfa de molècules d'adhesió a l'endoteli i atenua l'activació de NF-kappaB. Endocrine 2009, 35, 341–346. [CrossRef] [PubMed]
121. Chen, C.; Wu, L.; Xie, C.; Zhao, X.; Mao, H.; Xing, C. El paper de la proteïna quinasa activada per AMP 1- va mediar l'estrès del reticle endoplasmàtic per alleujar l'efecte tòxic de la toxina urémica indoxil sulfat sobre les cèl·lules endotelials vasculars per part de Klotho. J. Appl. Toxicol. 2021, 41, 1446–1455. [CrossRef] [PubMed]
122. Kusaba, T.; Okigaki, M.; Matui, A.; Murakami, M.; Ishikawa, K.; Kimura, T.; Sonomura, K.; Adachi, Y.; Shibuya, M.; Shirayama, T.; et al. Klotho s'associa amb el receptor de VEGF-2 i el potencial del receptor transitori canònic-1 Ca2 més el canal per mantenir la integritat endotelial. Proc. Natl. Acad. Ciència. EUA 2010, 107, 19308–19313. [CrossRef] [PubMed]
123. Kang, JS; Fill, SS; Lee, J.-H.; Lee, SW; Jeong, AR; Lee, ES; Cha, S.-K.; Chung, CH Efectes protectors de klotho sobre la lesió de podòcits induïda per palmitat en la nefropatia diabètica. PLoS ONE 2021, 16, e0250666.
124. Chen, J.; Zhang, X.; Zhang, H.; Liu, T.; Zhang, H.; Teng, J.; Ji, J.; Ding, X. Indoxyl Sulfate Millorar la hipermetilació de Klotho i promoure el procés de calcificació vascular en la malaltia renal crònica. Int. J. Biol. Ciència. 2016, 12, 1236–1246. [Ref creuat]
125. Gajjala, PR; Fliser, D.; Speer, T.; Jankowski, V.; Jankowski, J. Paper emergent de les modificacions post-traduccionals en la malaltia renal crònica i la malaltia cardiovascular. Nefrol. Marqueu. Trasplantament. 2015, 30, 1814–1824. [CrossRef] [PubMed]
126. Saar-Kovrov, V.; Zidek, W.; Orth-Alampour, S.; Fliser, D.; Jankowski, V.; Biessen, EAL Reducció de toxines urèmiques unides a proteïnes en plasma de pacients amb insuficiència renal crònica: una revisió sistemàtica. J. Intern. Med. 2021, 290, 499–526. [CrossRef] [PubMed]
Eva Harlacher 1 , Julia Wollenhaupt 1 , Constance CFMJ Baaten 1,2 i Heidi Noels 1,2
1 Institut d'Investigació Cardiovascular Molecular, Hospital Universitari d'Aquisgrà, Rheinisch-Westfälische Technische Hochschule Aachen University, 52074 Aquisgrà, Alemanya; evstraussfel@ukaachen.de (EH); jwirth@ukaachen.de (JW)
2 Departament de Bioquímica, Cardiovascular Research Institute Maastricht, Universitat de Maastricht, 6200 MD Maastricht, Països Baixos






