Part Ⅱ Comprensió metabòlica de la desregulació genètica en el microentorn tumoral del carcinoma de cèl·lules clares renals del ronyó
May 08, 2023
Resultat
1. Identificació de gens metabòlics expressats de manera diferencial en KIRC.
Per explorar la desregulació metabòlica a KIRC, vam explorar les dades de TCGA disponibles per obtenir una visió profunda de la terapèutica dirigida al metabolisme a la clínica. Amb aquesta finalitat, vam seleccionar un conjunt de 1916 gens metabòlics que es van tallar a partir de dos conjunts de dades diferents [16, 17] i vam seleccionar 1100 gens expressats de manera diferencial en teixits tumorals i normals (taula suplementària 2). Aquests gens metabòlics expressats de manera diferent es van representar en volcans i mapes de calor (figures 1 (a) i 1 (b)). Dels 1100 gens metabòlics expressats de manera diferent, 78 gens es van regular a l'alça i 163 gens es van regular a la baixa. A més, hi havia 859 gens sense canvis. El mapa de calor representa l'índex d'expressió individual d'aquests gens metabòlics diferencials en mostres tumorals i normals (figura 1 (b)). A continuació, vam identificar els 10 gens metabòlics expressats de manera diferent; entre ells, ENPP3, NNMT, CYP2J2, SCD i HK2 van ser regulats a la baixa i HSD11B2, HMGCS2, HPD, HS6ST2 i ALDOB. Els diagrames de caixa d'aquests DEmG es mostren a la figura 1 (c). Entre els gens regulats a l'alça, ENPP3 s'expressa ~7- vegades en tumors. Alternativament, el gen ALDOB està ~5-regulat a la baixa en mostres de tumor analitzades.
A més, vam avaluar la via KEGG i les anàlisis GO de DEmG. L'anàlisi de la via KEGG va revelar que els gens regulats es van enriquir significativament en el metabolisme del carboni, la senyalització HIF1 i la glucòlisi/gluconeogènesi amb una proporció de gens més alta (8-9 nombre de gens a cada via) (Figura 1 (d)). De la mateixa manera, entre els DEmG regulats a la baixa, vam trobar que el metabolisme del carboni i la degradació de valina, leucina i isoleucina eren les principals vies afectades pels gens metabòlicament actius (Figura 1 (e)). Les vies relacionades amb els orgànuls del peroxisoma també es van enriquir significativament en un grup de mostres de tumors gènics regulats. Cal destacar que, en comparació amb els dels gens regulats a l'alça, les vies implicades en els gens regulats a la baixa tenen valors p significatius més alts. Val la pena esmentar que la majoria de les vies KEGG enriquides en categories de gens regulats a la baixa estaven relacionades amb el metabolisme dels aminoàcids. Per disseccionar encara més la implicació de DEmG en la tumorigènesi, es van realitzar les anàlisis funcionals GO de gens regulats a l'alça i a la baixa. Vam dividir l'ontologia GO en tres grups de subontologia funcional, BP (procés biològic), CC (component cel·lular) i MF (funció molecular) (figures 1 (f) i 1 (g)). A més, l'anàlisi GSEA va revelar un augment significatiu de l'enriquiment dels gens associats amb BENPORATH_MYC_TARGET{_WITH_EBOX en tumors, mentre que BROWN{{11} } MIELOIDE_DESENVOLUPAMENT_CEL·LULAR{_UP, KEGG_ALFA{_ LINOLENIC_METABOLIME{_i KEGG{ S'ha trobat que el {19}}ÈTER_ LÍPID_METABOLISME estava enriquit negativament. En la següent etapa, vam construir una xarxa PPI d'interacció proteïna-proteïna amb DEmGs regulats a l'alça i a la baixa. Alguns dels gens van mostrar interacció entre ells. Mitjançant les interaccions d'aquests gens, vam aïllar els gens centrals. Cada node és discret de l'altre en funció del valor del grau; a més, vam aïllar els 7 gens principals per a PPI. També vam explorar la correlació entre aquesta expressió gènica central i les característiques clinicopatològiques de KIRC en conjunts de dades TCGA.

Feu clic aquí per saber-hoquins són els beneficis de Cistanche.
2. L'anàlisi de la xarxa revela canvis metabòlics bàsics en diverses ontologies tumorals.
A continuació, es van seleccionar i utilitzar les dades d'expressió de DEmG com a dades d'entrada per a WGCNA, que va identificar 6 mòduls de coexpressió diferents que contenien un nombre diferent de gens per a cada mòdul (figura 2 (a)). Vam correlacionar gens diferencials amb trets externs i vam identificar els mòduls que estaven associats significativament amb trets clínics (figura 2 (b)). A partir del coeficient de correlació, vam trobar que els mòduls MEturquesa estaven correlacionats negativament amb l'estat de supervivència. Les anàlisis d'enriquiment de les vies GO i KEGG es van realitzar mitjançant gens d'aquests mòduls (figures 2 (c) i 2 (d)). Les vies KEGG més enriquides van ser la degradació de la valina, la leucina i la isoleucina; metabolisme del carboni; metabolisme del propanoat; metabolisme dels àcids grassos; degradació d'àcids grassos; metabolisme del peroxisome i del butanoat; metabolisme de glioxilat i dicarboxilat; i el metabolisme del triptòfan (figura 2 (c)). Els gens relacionats amb els termes BP es van enriquir predominantment en processos catabòlics de molècules petites, àcids carboxílics i àcids orgànics. Els gens relacionats amb termes CC es van enriquir principalment a la matriu mitocondrial. Els gens expressats de manera diferencial relacionats amb la MF es van enriquir principalment en la unió de coenzims (figura 2 (d)). A més, vam realitzar una anàlisi de supervivència de 8 gens al mòdul de supervivència. Els pacients amb una expressió més alta d'ACADSB, PANK1, SLC25A4, PCCA, HADH, AUH, ACAT1 i ALDH6A1 tenien una taxa de supervivència més llarga que els que tenien una expressió més baixa d'aquests gens (p=0) (Figures 2 (e) - 2 ( l)).
3. Agrupació dels pacients KIRC.
Hem seleccionat els DEmG principals per a l'anàlisi de clúster; els pacients amb KIRC es van agrupar en tres grups basats en l'expressió diferencial dels gens metabòlics. La figura 3 (a) mostra els mapes de calor de DEmG als pacients amb KIRC. L'escala de color indica el valor d'expressió (el blau clar indica un valor d'expressió més baix; el blau més fosc indica valors d'expressió gènica més alts).
Es van representar les corbes KM per comparar la supervivència global dels tres grups per als pacients amb KIRC. Les taxes de supervivència generals van variar significativament entre els tres grups (p <{{0}}: 01 Figura 3 (b)). El clúster 1 va mostrar una pitjor taxa de supervivència en comparació amb el clúster 2 i el clúster 3. La taxa de supervivència de PFS també va variar significativament entre els 3 grups (p <0:001, figura 3 (c)) i el clúster 1 va mostrar una pitjor taxa de supervivència de PFS en comparació. amb el clúster 2 i el clúster 3.
Els diferents colors del nostre model representen paràmetres clínics i estadis patològics subjacents (figura 3 (d)). El clúster 3 té unes proporcions de Mo més baixes i un valor M1 més alt en comparació amb els grups 1 i 2, cosa que suggereix una metàstasi del càncer més alta i un estadi més avançat dels tumors al clúster 3 que als grups 1 i 2. De la mateixa manera, al clúster 3, el càncer s'ha estès més als ganglis limfàtics. (N1 més alt) en comparació amb els dels grups 1 i 2. La majoria dels pacients amb KIRC es van diagnosticar en les etapes III i IV (figures 3 (e) i 3 (f)), cosa que suggereix tumors més grans o expandits, a més de passar per la sang o el sistema limfàtic a una regió llunyana del cos.

4. Estat immunitari de tres clústers.
Hem utilitzat l'algoritme ESTIMATE per estimar les puntuacions estromals i immunitàries d'una sèrie de teixits KIRC en funció dels seus perfils transcripcionals metabòlics (Figura 4 (a)). Més tard, es van tenir en compte aquestes puntuacions per desenvolupar una signatura de gens metabòlics basada en la puntuació estromal-immune per a l'estratificació del pronòstic a KIRC. Com es mostra a la figura 4 (a), es van estratificar tres grups de clústers (C1, C2 i C3) en quadres de caixa en funció de la seva puntuació estromal-immune. Entre els tres grups, C1 va mostrar una puntuació significativa més alta tant en classificacions estromals com immunes.
A més, CIBERSORT va analitzar tres clústers amb un valor p < 0.1 (Figura 4 (b)). La puresa del tumor, la puntuació immune i la puntuació estromal juntament amb les etapes patològiques de 3 grups es mostren a la part superior del mapa de calor. En aquesta anàlisi, vam trobar principalment que les cèl·lules T reguladores (Tregs) es van enriquir al clúster C1 i els pacients a C1 es trobaven principalment en estadis patològics III i IV. A més, les cèl·lules NK activades, les cèl·lules CD8 més T, les cèl·lules auxiliars fol·liculars T i els macròfags M0 al clúster C1; Cèl·lules T CD8 més i cèl·lules T auxiliars fol·liculars al clúster C2; i també es van detectar mastòcits en repòs, macròfags M2, cèl·lules T CD4 de memòria en repòs, monòcits, cèl·lules B ingènues i macròfags M1 al clúster C3 (figura 4 (b)).
A part de CIBERSORT, hem utilitzat altres paquets algorítmics per comprovar l'estat de la infiltració immune. El mapa de calor jeràrquic de l'anàlisi MCP es mostra a la figura 4 (c). Les conclusions clau de l'anàlisi MCP van ser la infiltració de neutròfils i la infiltració de cèl·lules endotelials al clúster C3 que faltava al clúster C1. Aquesta anàlisi també va revelar la infiltració de cèl·lules NK, llinatge monocític i cèl·lules dendrítiques mieloides al clúster C3. Altres poblacions de cèl·lules immunitàries es van barrejar en tres grups analitzats (figura 4 (c)).
Per complementar les anàlisis CIBERSORT i MCP, vam aplicar ssGSEA per quantificar els nivells d'infiltració dels tipus de cèl·lules immunitàries implementades al paquet R GSVA. Les dades de tres clústers es van introduir al paquet ssGSEA i es van obtenir riquesa de 28 cèl·lules i tipus relacionats amb el sistema immunitari en mostres KIRC. Els resultats van revelar que C1 i C2 tenien més infiltració immune; algunes cèl·lules immunitàries innates, incloent NK, neutròfils i eosinòfils, es van barrejar en 3 grups (figura 4 (d)).

5. Construcció i validació del model predictiu basat en DEmG.
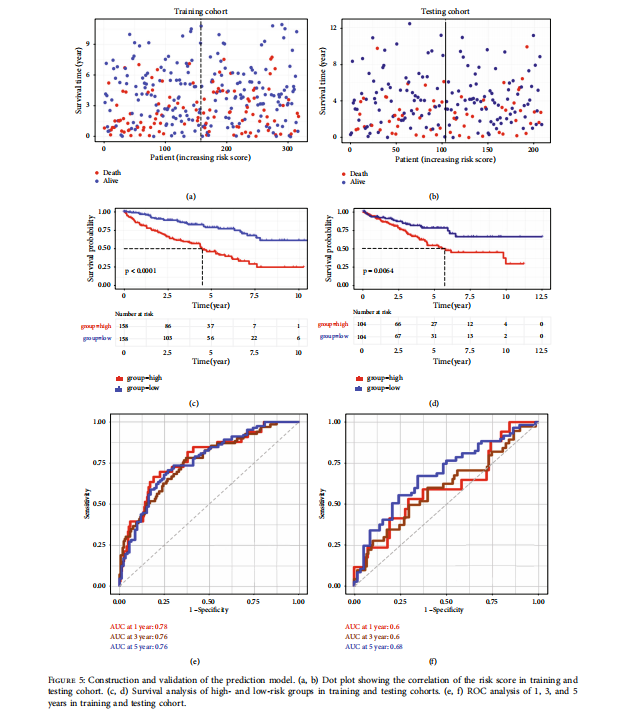
Finalment, hem construït i validat el model de predicció basat en l'expressió diferencial dels gens metabòlics. Hem calculat la puntuació de risc de DEmG relacionada amb la immunitat en funció de la supervivència global. Amb aquesta finalitat, hem creat dos grups per avaluar la correlació de la puntuació de risc; un és per a la cohort de formació i l'altre per a la cohort de proves. Vam trobar que la supervivència global era baixa i es trobava dispersa per la puntuació de risc (figures 5 (a) i 5 (b)). A continuació, en funció de la puntuació mitjana del risc, vam assignar pacients amb KIRC a grups de risc alt i baix per a una avaluació posterior. A continuació, vam realitzar una anàlisi de supervivència d'aquests dos grups de risc en cohorts d'entrenament i proves. Com era d'esperar, es va trobar que els grups d'alt risc tenien una supervivència baixa en comparació amb els grups de baix risc (figures 5 (c) i 5 (d)). A més, es va realitzar una anàlisi de la corba ROC per a cohorts de formació i prova. Vam observar una puntuació ROC de 0.68 als 5 anys en les cohorts de proves, la qual cosa indica un bon rendiment per predir el pronòstic de KIRC (figures 5 (e) i 5 (f)). A més de l'anàlisi de la corba ROC, també vam executar el model de regressió LASSO COX per validar el nostre model pronòstic tal com indica la desviació de probabilitat parcial (figura suplementària 5 (a)) i el coeficient de regressió dels DEmG (figura suplementària 5 (b)). Finalment, es va predir que cinc gens (ABCG1, CRYL1, FDX1, PANK1 i SLC44A) eren possibles factors pronòstics amb HR < 1 (figura suplementària 5 (c)).
6. Mecanismes subjacents de la progressió del KIRC.
Per investigar més el mecanisme subjacent per a la progressió de KIRC, vam realitzar una anàlisi d'expressió diferencial entre tots els clústers i vam utilitzar un mapa de calor per visualitzar els resultats (figura 6 (a)). Per identificar les vies de senyalització dels DEmG, vam realitzar anàlisis d'enriquiment KEGG i GO dels DEG en tres grups. En resum, aquests resultats van revelar que els DEG de tres cúmuls es van enriquir principalment en l'adhesió focal, la via de senyalització Foxo i la via de senyalització Apelin per al clúster C3 i l'absorció de minerals, la formació de trampa extracel·lular de neutròfils i la infecció per estafilococ aureus per al clúster C2 (Figura 6). (b)). A més, l'anàlisi funcional de GO dels DEG va descobrir ontologies relacionades amb MF, CC i BP que es mostren a la figura 6 (c). Curiosament, l'anàlisi d'expressió diferencial va revelar un comportament anormal de la regulació dels gens en tres grups. Principalment, NUDT1 es va expressar molt en C1, que va tenir la pitjor supervivència. Una investigació posterior va revelar que l'expressió NUDT1 es va reduir significativament a través de la progressió de C1 a C3 (Figura 6 (d)). A més, es va trobar que el NUDT1 estava regulat a les mostres de tumor KIRC (figura 6 (e)). A continuació, vam destacar l'expressió NUDT1 en les etapes de cada tumor (figura 6 (f)). El traçador de Kaplan-Meier també va realitzar una anàlisi de supervivència global i vam trobar que els pacients amb una expressió més alta de NUDT1 tenien una pitjor supervivència global (HR=1:82 (1,34–2,48), log-rank p {{27} }:00012) (Figura 6 (g)).

Finalment, vam realitzar anàlisis d'enriquiment funcional KEGG i GO per a gens que interactuen amb NUDT1. Els gens es van dividir en dos grups: correlacionats positivament amb NUDT1 i correlacionats negativament amb NUDT1. L'anàlisi de la via KEGG va demostrar que els gens correlacionats positivament es van enriquir principalment en la via ribosòmica, la malaltia de Huntington, l'esclerosi lateral amiotròfica i la malaltia d'Alzheimer. D'altra banda, els gens correlacionats negativament es van enriquir principalment en la senyalització de l'hepatitis B i Foxo (Figura 6 (h)). A més, a la figura 6 (i) es va mostrar l'ontologia GO de tres grups diferents MF, CC i BP per a gens correlacionats positivament i negativament. A més, vam trobar que l'expressió de NUDT1 estava altament correlacionada amb la infiltració de cèl·lules immunitàries (figura suplementària 6) i diferents característiques clíniques dels pacients amb KIRC (taula 1).

Suplements de cistanche
7. La pèrdua de NUDT1 inhibeix la proliferació i migració de cèl·lules canceroses renals.
A continuació, vam comparar el nivell d'expressió de NUDTI als teixits KIRC i els seus teixits normals associats, cosa que va revelar que NUDT1 està molt expressat als teixits KIRC (Figura 7 (a)). A més, vam determinar els efectes de la pèrdua de NUDT1 sobre les línies cel·lulars de càncer renal mitjançant la inhibició mediada per siRNA. NUDT1 es va dirigir a la derrota de siRNA en dues línies cel·lulars 786- O i ACHN i els nivells d'ARNm de NUDT1 es van inhibir amb èxit, tal com ho demostra l'anàlisi qPCR (figura 7 (b)). Després de la derrota de NUDT1 mediada per siRNA, l'assaig de viabilitat cel·lular va mostrar una viabilitat cel·lular reduïda en ambdues línies cel·lulars (figures 7 (c) i 7 (d)). Després, l'assaig de migració cel·lular després de la derrota de NUDT1 va mostrar una migració cel·lular significativament reduïda a les cèl·lules NUDT1-esgotades 786-O i ACHN (figures 7 (e) i 7 (f)). La capacitat de migració de les cèl·lules 786-O es va reduir a un 50% aproximadament i es va observar una reducció del 70% a les cèl·lules ACHN després de la derrota de NUDT1 (figura 7 (f)). La invasió cel·lular també es va inhibir en ambdues línies cel·lulars quan es va enderrocar el gen NUDT1 (figures 7 (g) i 7 (h)). Per complementar la migració, també vam realitzar un assaig de cicatrització de ferides quan NUDT1 es va esgotar de les línies cel·lulars 786-O i ACHN i vam observar resultats similars de capacitat de curació de ferides reduïdes en ambdues línies cel·lulars sense NUDT1 (figures 7 (l) -). 7(n)). A partir d'aquests resultats, vam plantejar la hipòtesi que la pèrdua de NUDT1 podria conduir a l'apoptosi a les cèl·lules canceroses renals. Per tant, vam mesurar el percentatge de cèl·lules apoptòtiques després del silenciament de NUDT1. Curiosament, vam descobrir que el percentatge de cèl·lules apoptòtiques augmentava significativament a les cèl·lules esgotades de NUDT 1- (figures 7 (i)-7 (k)).

Discussió
El carcinoma de cèl·lules clares renals de ronyó (KIRC) és un dels càncers més freqüents a tot el món, generalment no mostra símptomes primerencs fins que el tumor es fa prou gran; per tant, la taxa de mortalitat és relativament alta [18–20]. Per tant, és necessari investigar la carcinogènesi de KIRC i identificar biomarcadors útils per al seu diagnòstic precoç. Tanmateix, fins ara s'ha establert un coneixement limitat sobre la patogènesi i la carcinogènesi de KIRC. A més, no s'han validat molts marcadors moleculars per a la pràctica clínica. La tecnologia avançada de seqüenciació d'alt rendiment i bioinformàtica permet seleccionar biomarcadors efectius [21]. Les dades de seqüenciació de l'ARN i les anotacions clíniques de més de cinc-cents casos de KIRC estan disponibles gratuïtament a la base de dades TCGA. Aprofitant aquestes dades disponibles gratuïtament de TCGA, vam analitzar les dades de la seqüència d'ARN per a gens metabòlics expressats de manera diferencial en mostres de teixit tumoral i normal. Entre els gens regulats a l'alça i a la baixa, vam identificar els 10 gens metabòlics expressats de manera diferent (DEmG). Creiem que els gens metabòlics tenen funcions diverses en KIRC; tot i així, trobar marcadors diagnòstics i terapèutics adequats podria ser un repte del conjunt de gens amb funcions diversificades.
Anteriorment, els estudis havien estimat la infiltració de cèl·lules immunitàries en el microambient tumoral de diversos càncers. Es va estudiar una relació entre les cèl·lules immunitàries del tumor i l'angiogènesi a les dades de mostres de KIRC obtingudes de TCGA i es van identificar RFX2, SOX13 i THRA com els tres principals MTF en la regulació de la signatura de l'angiogènesi en pacients KIRC [4]. A més, dos patrons de modificació independents de m6A controlen les funcions biològiques, les característiques immunològiques i els pronòstics de KIRC [22]. La proteïna 5 relacionada amb l'autofàgia (ATG5) s'ha relacionat amb la progressió de diversos càncers inclòs KIRC [23]. En l'anàlisi actual, alguns dels gens expressats de manera diferent, inclosos PBRM1, SET2, VHL i BAP1, van mostrar una correlació significativa amb les vies metabòliques a les dades KIRC. Per a una investigació més profunda, vam agrupar els pacients en funció dels DEmG; el clúster 1 va mostrar una taxa de supervivència global pitjor en comparació amb els altres clústers; de totes maneres, els pacients amb KIRC del clúster 3 tenen estadis tumorals avançats i tenen ganglis limfàtics alts (N1 més alt) en comparació amb els dels grups 1 i 2, mostrant metàstasi del càncer i expansió dels tumors al clúster 3. Mostra un nombre menor de gens metabòlics. en grups associats a metàstasi del càncer.
A més, les puntuacions d'infiltració immune en diferents clústers mostren C1 amb puntuacions altes en classificacions estromals i immunes. Cal destacar que els pacients amb C1 en estadis patològics III i IV tenen una alta infiltració de cèl·lules T juntament amb cèl·lules T CD8 més, cèl·lules T auxiliars fol·liculars i macròfags. Tot i que també té abundants Tregs. Els Tregs tenen un paper vital en la tolerància immune i l'homeòstasi [24]. En molts càncers com el càncer de còlon, càncer de mama i càncer de pàncrees, l'augment del percentatge de Tregs s'associa amb el mal pronòstic del càncer [25, 26]. El macròfag M0 indueix la invasió i la proliferació de cèl·lules [27], i els nivells elevats dels macròfags s'associen amb un pronòstic deficient en RCC [28]. De la mateixa manera, les cèl·lules CD8 més T es coneixen com les cèl·lules antitumorals clau i la millor opció per a la teràpia de cèl·lules immunitàries dirigides per als càncers [29]. Tot i que C1 té la infiltració més alta de cèl·lules T CD8 més que altres grups, va tenir la pitjor supervivència global.

Herba Cistanche
Hem utilitzat tres mètodes CIBERSORT, MCP i ssGSEA per estudiar la infiltració de cèl·lules immunitàries al microentorn del tumor KIRC. El mètode tradicional per mesurar la infiltració immune del tumor és mitjançant la histologia en seccions de teixit i subconjunts immunitaris inferits per immunohistoquímica de marcadors individuals. No obstant això, hi ha diverses limitacions en què la immunohistoquímica no pot identificar moltes poblacions immunes i té un mal rendiment en la captura de fenotips funcionals (p. ex., limfòcits activats versus en repòs). Per tant, hem utilitzat CIBERSORT, un enfocament computacional desenvolupat per [30] que aborda els reptes als quals s'enfronta la immunohistoquímica. A part de CIBERSORT, hem utilitzat altres paquets algorítmics per comprovar l'estat de la infiltració immune. Això es deu al fet que CIBERSORT només mesura proporcions intramostre de poblacions de cèl·lules immunitàries que es poden resoldre mitjançant un altre paquet, com ara el comptador MCP, que pot estimar la població de cèl·lules en abundància que permet una comparació entre mostres de cèl·lules infiltrades al microambient tumoral [31]. Per complementar les anàlisis CIBERSORT i MCP, vam aplicar ssGSEA per quantificar els nivells d'infiltració dels tipus de cèl·lules immunitàries implementades al paquet R GSVA [32, 33]. El GSA és un mètode basat en el rang que calcula una sobreexpressió per a la llista d'interès d'un gen en relació amb la resta de gens del genoma. El CIBERSORT va mostrar millors resultats en comparació amb els altres dos mètodes; així, es van fer més anàlisis a partir de les dades obtingudes de CIBERSORT.
A més, ens vam centrar en el mecanisme subjacent de la progressió de KIRC mitjançant l'anàlisi d'expressió diferencial basada en les dades d'ARN-seq. En general, ens vam dirigir a l'expressió diferencial anormal dels gens comuns entre tres grups. La majoria dels gens estaven regulats a la baixa, excepte NUDT1 a C1; tanmateix, la seva expressió es va reduir significativament a través de la progressió de C1 a C3. Així, NUDT1 es va validar encara més pel seu paper en la progressió de KIRC. La inhibició mediada per siRNA de l'expressió del gen NUDTI en dues línies cel·lulars KIRC (786-O i ACHN) va reduir la viabilitat cel·lular i la migració cel·lular i va augmentar l'apoptosi, la qual cosa confirma el seu paper en la progressió del tumor. Anteriorment, s'ha informat que el nivell d'expressió NUDT1 es correlacionava amb el grau del tumor, estadi, mida, diferenciació, grau d'invasió vascular, supervivència global (SO) i supervivència lliure de malaltia (DFS) en pacients amb HCC, també predits com a un marcador pronòstic amb potencials terapèutics en pacients amb HCC [34]. La sobreexpressió de NUDT1 en la hipertensió arterial pulmonar redueix l'estrès oxidatiu i el dany a l'ADN, per tant promou la proliferació cel·lular i redueix l'apoptosi [35]. S'ha demostrat que els pacients amb carcinoma de cèl·lules escamoses orals (OSCC) que tenen una alta expressió de NUDT1 han mostrat una taxa de supervivència baixa [36]. A partir del fet que no hi ha prou literatura disponible sobre el paper de NUDTI en els càncers i, fins ara, cap estudi ha informat mai del seu paper a KIRC, per tant, estem informant per primera vegada del paper de NUDTI en la progressió de KIRC. L'estudi actual tenia algunes limitacions; tot i que la nostra investigació va trobar que la signatura podria estar associada amb la immunoteràpia de KIRC, l'eficàcia de la signatura no es va poder validar a causa de la manca de dades, els possibles mecanismes subjacents i els rols funcionals de NUDT1 en KIRC i la pràctica clínica necessiten una exploració més profunda.

Cistanche tubulosa
Conclusions
Vam examinar gens metabòlics desregulats entre teixits normals i tumorals i vam explorar la seva funció. L'anàlisi WGCNA va identificar un grup de gens correlacionats amb l'estat de supervivència de KIRC. La agrupació de consens basada en gens relacionats amb la supervivència va demostrar tres grups amb diferents taxes de supervivència i patrons d'infiltració immune. NUDT1 es va correlacionar negativament amb la supervivència, i anàlisis posteriors van revelar que la derrota de NUDT1 inhibeix la proliferació i la migració de cèl·lules tumorals. Cal destacar que es va construir un model de predicció basat en gens relacionats amb la supervivència, que va mostrar una alta eficiència per predir la supervivència de KIRC. En conclusió, vam realitzar una anàlisi exhaustiva dels gens metabòlics a KIRC i vam identificar NUDT1 com un oncogen que es podria utilitzar com a objectiu terapèutic i pronòstic.
L'efecte de l'extracte de Cistanche sobre la transparència renal
Hi ha evidència científica limitada sobre l'efecte de Cistanche sobre la transparència renal. Tanmateix, alguns estudis suggereixen que l'extracte de Cistanche pot tenir un impacte positiu en la salut renal.
Els ronyons són els responsables de filtrar els residus i les toxines de l'organisme, i la seva salut és essencial per al benestar general. Els estudis han demostrat que l'extracte de Cistanche té potents propietats antioxidants i antiinflamatòries, que poden ajudar a protegir contra l'estrès oxidatiu i la inflamació als ronyons.
En la medicina tradicional xinesa, el Cistanche també s'utilitza per tonificar els ronyons i millorar-ne la funció. Alguns professionals creuen que el consum regular d'extracte de Cistanche pot ajudar a millorar la transparència renal, encara que aquesta afirmació no està recolzada per una investigació clínica sòlida.
Per tant, es requereix una investigació més rigorosa per entendre completament els beneficis potencials de l'extracte de Cistanche sobre la transparència renal. No obstant això, com amb qualsevol suplement dietètic o teràpia alternativa, és important consultar amb un professional de la salut abans d'incorporar noves addicions a la vostra dieta, especialment si teniu afeccions mèdiques preexistents.
Referències
[18] RL Siegel, KD Miller i A. Jemal, "Cancer statistics, 2019", CA: A Cancer Journal for Clinicians, vol. 69, núm. 1, pàgines 7–34, 2019.
[19] RL Siegel, KD Miller, HE Fuchs i A. Jemal, "Cancer statistics, 2021", CA: A Cancer Journal for Clinicians, vol. 71, núm. 1, pàgines 7–33, 2021.
[20] JC Angulo i O. Shapiro, "El paisatge terapèutic canviant del càncer renal metastàtic", Càncers, vol. 11, núm. 9, pàg. 1227, 2019.
[21] AK Sharma, "Tendències emergents en el descobriment de biomarcadors: facilitat de pronòstic i predicció en càncer", Seminaris en biologia del càncer, vol. 52, part 1, pàgs. iii–iv, 2018.
[22] H. Li, J. Hu, A. Yu et al., "La modificació de l'ARN de la N6- metiladenosina prediu fenotips immunes i oportunitats terapèutiques en el carcinoma de cèl·lules clares renals del ronyó", Frontiers in Oncology, vol. 11, article 642159, 2021.
[23] C. Xu, Y. Zang, Y. Zhao, et al., "L'anàlisi integral del càncer de panxa va confirmar que l'ATG5 va promoure el manteniment del metabolisme del tumor i l'aparició d'escapament immune del tumor", Frontiers in Oncology, vol. 11, article 652211, 2021.
[24] Y. Takeuchi i H. Nishikawa, "Roles of regulatory T cells in cancer immunity", International Immunology, vol. 28, núm. 8, pàgines 401–409, 2016.
[25] C. Zhuo, Y. Xu, M. Ying, et al., "FOXP3 més Tregs: fenotips heterogenis i impactes conflictius en els resultats de supervivència en pacients amb càncer colorectal", Immunologic Research, vol. 61, núm. 3, pàgines 338–347, 2015.
[26] H. Wang, F. Franco i PC Ho, "Regulació metabòlica de Tregs en càncer: oportunitats per a la immunoteràpia", Trends Cancer, vol. 3, no. 8, pàgines 583–592, 2017.
[27] BZ Qian i JW Pollard, "La diversitat dels macròfags millora la progressió del tumor i la metàstasi", Cell, vol. 141, núm. 1, pàgs. 39–51, 2010.
[28] A. Hajiran, N. Chakiryan, AM Aydin, et al., "Reconeixement de l'heterogeneïtat espacial del microentorn immune del tumor en el carcinoma de cèl·lules renals metastàtics i la correlació amb la resposta a la immunoteràpia", Immunologia clínica i experimental, vol. 204, núm. 1, pàgines 96–106, 2021.
[29] B. Farhood, M. Najafi i K. Mortezaee, "Limfòcits T citotòxics CD8(plus) en immunoteràpia contra el càncer: una revisió", Journal of Cellular Physiology, vol. 234, núm. 6, pàgines 8509–8521, 2019.
[30] AM Newman, CL Liu, MR Green, et al., "Robust enumeration of cell subsets from tissue expression profiles", Nature Methods, vol. 12, núm. 5, pàgines 453–457, 2015.
[31] E. Becht, NA Giraldo, L. Lacroix, et al., "Estimating the population abundance of tissue-infiltrating cells immune and stromal cells using gene expression", Genome Biology, vol. 17, núm. 1, pàg. 218, 2016.
[32] DA Barbie, P. Tamayo, JS Boehm, et al., "La interferència sistemàtica de l'ARN revela que els càncers oncogènics impulsats per KRAS requereixen TBK1", Nature, vol. 462, núm. 7269, pàgs. 108–112, 2009.
[33] S. Hanzelmann, R. Castelo i J. Guinney, "GSVA: gene set variation analysis for microarray and RNA-seq data", BMC Bioinformatics, vol. 14, núm. 1, 2013.
[34] Q. Ou, N. Ma, Z. Yu et al., "Nudix hydrolase 1 is a prognostic biomarker in hepatocellular carcinoma", Aging, vol. 12, núm. 8, pàgines 7363–7379, 2020.
[35] G. Vitry, R. Paulin, Y. Grobs, et al., "La neteja de precursors d'ADN oxidat per NUDT1 contribueix a la remodelació vascular en la hipertensió arterial pulmonar", American Journal of Respiratory and Critical Care Medicine, vol. 203, núm. 5, pàgines 614–627, 2021.
[36] Y. Shen, L. Zhang, S. Piao, et al., "NUDT1: un potencial predictor independent per al pronòstic de pacients amb carcinoma de cèl·lules escamoses orals", Journal of Oral Pathology & Medicine, vol. 49, núm. 3, pàgines 210–218, 2020.
Junwei Xie,1,2,3,4,5 Lingang Cui,6 Shaokang Pan,1,2,3,4,5 Dongwei Liu,1,2,3,4,5 Fengxun Liu,1,2,3,4 ,5 i Zhangsuo Liu 1,2,3,4,5
1 Departament de Nefrologia, Primer Hospital Afiliat de la Universitat de Zhengzhou, Zhengzhou 450052, Xina
2 Institut de Recerca de Nefrologia, Universitat de Zhengzhou, Zhengzhou 450052, Xina
3 Centre de Recerca de Malalties Renals, Zhengzhou, 450052 Henan, Xina
4 Laboratori clau de diagnòstic i tractament de precisió per a la malaltia renal crònica a la província de Henan, Zhengzhou 450052, Xina
5 Unitat bàsica del Centre Nacional d'Investigació Mèdica Clínica de Malalties Renals, Zhengzhou 450052, Xina
6 Departament d'Urologia, Primer Hospital Afiliat de la Universitat de Zhengzhou, Zhengzhou 450052, Xina
