Funcions protectores renals de l'àcid lipoic en la malaltia renal
Aug 31, 2023
Resum:El ronyó és un òrgan crucial que elimina els residus metabòlics i reabsorbeix els elements nutritius. També participa en la regulació de la pressió arterial, el manteniment de l'equilibri electròlit i l'homeòstasi del pH sanguini, així com l'eritropoesi i la maduració de la vitamina D. A causa d'una càrrega de treball tan pesada, el ronyó és un òrgan que requereix energia i està constantment exposat a insults endògens i exògens, donant lloc al desenvolupament de qualsevollesió renal aguda(AKI) omalaltia renal crònica(ERC). No obstant això, no hi ha tractaments terapèutics per tractar l'IRA o l'ERC de manera eficaç. Per tant, calen amb urgència nous enfocaments terapèutics per combatre la lesió renal. Aquest article de revisió analitza el paper de l'àcid -lipoic (ALA) en la prevenció i el tractament de les malalties renals. Ens centrem en diversos models animals de lesió renal mitjançant els quals s'han desvelat els mecanismes renoprotectors subjacents de l'ALA. Els models animals coberts inclouen nefropatia diabètica, lesió renal induïda per sèpsia, lesió isquèmica renal, obstrucció ureteral unilateral i lesions renals induïdes per àcid fòlic i metalls com el cisplatí, el cadmi i el ferro. Destaquem els mecanismes comuns de les accions protectores renals de l'ALA que inclouen la disminució del dany oxidatiu, l'augment de les capacitats antioxidants, la contraresta de la inflamació, la mitigació de la fibrosi renal i l'atenuació de la mort de les cèl·lules nefrones. És per aquests mecanismes que l'ALA aconsegueix la seva funció biològica d'alleujar la lesió renal i millorar la funció renal. No obstant això, també assenyalem que es necessitaran estudis més exhaustius, preclínics i clínics per fer de l'ALA un millor agent terapèutic per dirigir els trastorns renals.
Paraules clau: àcid lipoic;lesió renal aguda; malaltia renal crònica; malaltia renal diabètica; nefropatia diabètica; nefroprotecció

FEU CLIC AQUÍ PER OBTENIR CISTANCHE PER A TRACTAMENTS DE L'ERC
1. Introducció
El ronyó és un òrgan vital que participa en el manteniment de l'equilibri electròlit, l'estabilitat del pH sanguini, l'eliminació de residus metabòlics i la reabsorció de nutrients i minerals [1,2]. El ronyó també està implicat en l'eritropoesi, la maduració de la vitamina D i la regulació de la pressió arterial [3]. En condicions fisiopatològiques com el dejuni, la fam a llarg termini i la resistència a la insulina, el ronyó també pot regenerar la glucosa mitjançant la gluconeogènesi utilitzant molècules precursores com ara glicerol, alanina, piruvat i lactat [4]. Com a tal, el ronyó sempre té una gran càrrega de treball i, per tant, està exposat a nombrosos factors de risc que poden causar malalties o lesions renals. Hi ha dos tipus de malalties renals: la malaltia renal crònica (ERC) [5] i la lesió renal aguda (IRA) [6]. La CKD es produeix quan hi ha una disminució gradual de la funció renal durant més de 3 mesos a causa del dany a la filtració glomerular i lesions tubulars [7]. S'ha previst que l'any 2040, la ERC es convertirà en la cinquena causa de mort a tot el món [8]. D'altra banda, l'IRA es produeix quan hi ha una disminució ràpida de la funció renal durant menys de 3 mesos, i això s'indica per acidosi, sobrecàrrega de líquids i anomalies amb electròlits i canvis hematologia [7]. També se sap que les persones amb ERC poden tenir un risc més elevat d'IRA [8]. Actualment, no hi ha productes farmacèutics per curar l'IRA o l'ERC. Si bé la diàlisi renal s'utilitza sovint per prevenir més danys als ronyons i mantenir la seva funció, la substitució renal pot ser l'últim recurs per a la supervivència del pacient. Per tant, si no es controlen, la IRA i la CKD poden provocar insuficiència renal, la qual cosa augmenta significativament la morbiditat i la mortalitat [7,9]. Per tant, hi ha una necessitat insatisfeta de lluitar contra la malaltia renal.
Per combatre les malalties renals, s'han explorat nombrosos enfocaments terapèutics [10–13]. Aquests inclouen compostos exògens i endògens, manipulacions dietètiques, modulació de vies metabòliques, enfocaments de cèl·lules mare i processos de senyalització cel·lular [10,11,14–21]. En aquest article de revisió, ens centrarem en el paper de l'àcid lipoic en la prevenció i la millora de les lesions renals. En particular, ens centrarem en estudis amb models animals per explorar els efectes protectors de l'àcid lipoic sobre les lesions renals. Aquests models animals de lesió renal inclouen la malaltia renal diabètica o nefropatia diabètica, lesió renal per isquèmia-reperfusió, lesió renal induïda per sèpsia, lesió renal induïda per obstrucció ureteral unilateral (UUO), cisplatina-lesió renal induïda, lesió renal induïda pel cadmi, fòliclesió renal induïda per àcid, ilesió renal aguda induïda pel ferro(Figura 1).

Figura 1. En aquest article es comenten models animals de lesió renal. Aquests models inclouen tant la lesió renal aguda com la malaltia renal crònica.
2. Àcid alfa-lipoic
L'ALA és un compost de ditiol d'origen natural [22]. És un cofactor per a -cetoglutarat deshidrogenasa, aminoàcid deshidrogenasa de cadena ramificada i piruvat deshidrogenasa [23–25] (figura 2). Per tant, ALA és un modulador d'energia [26, 27] (Figura 3). A més, a causa de la seva capacitat d'intercanviar grups tiol amb altres molècules que contenen tiol, com ara el glutatió i els residus de cisteïna de proteïnes, l'ALA també es coneix com a modulador redox [26–28] (Figura 3). L'ALA es coneix sovint com un antioxidant universal perquè pot actuar com a antioxidant tant en entorns lipòfils com hidròfils per reduir els subproductes del metabolisme oxidatiu, com les espècies reactives d'oxigen (ROS) i les espècies reactives de nitrogen (RNS) (Figura 4) [29] ]. L'ALA també pot quelar metalls com el zinc, el ferro i el coure i regenerar els antioxidants endògens, com el glutatió, i els antioxidants de vitamines exògens, com les vitamines C i E, amb efectes secundaris mínims [30] (Figura 4). Més important encara, l'ALA també pot inhibir la inflamació dirigint-se a NF-KB i disminuint l'alliberament de citocines inflamatòries (figura 4). Per tant, s'ha demostrat que eliminant els radicals lliures d'oxigen, l'ALA podria augmentar la funció glomerular i disminuir la inflamació renal [31]. Els estudis també han demostrat que el tractament amb ALA pot disminuir la lesió renal aguda reduint el nitrogen ureic en sang sèric,nivells de creatinina necrosi tumoralfactor-alfa (TNF-), interleucina-6 (IL-6) i interleucina-1 beta (IL{-1), per tantdisminució de l'endotelina-1vasoconstricció, difusió de neutròfils i inflamació als ronyons.

Figura 2. L'àcid lipoic és un cofactor del complex 2-cetoàcid deshidrogenasa mitocondrial, que inclou el complex de piruvat deshidrogenasa, el complex de -cetoglutarat deshidrogenasa i el complex d'aminoàcid deshidrogenasa de cadena ramificada. La subunitat E1 és 2-cetoàcid descarboxilasa utilitzant TPP com a cofactor; la subunitat E2 és una dihidrolipoamida aciltransferasa que utilitza àcid lipoic com a cofactor; la subunitat E3 és una dihidrolipoamida deshidrogenasa, que utilitza NAD+ com a acceptor d'electrons per a l'oxidació del grup lipoil unit a la subunitat E2. E3 catalitza la formació de la forma oxidada d'àcid lipoic i genera NADH mentrestant [32-34].
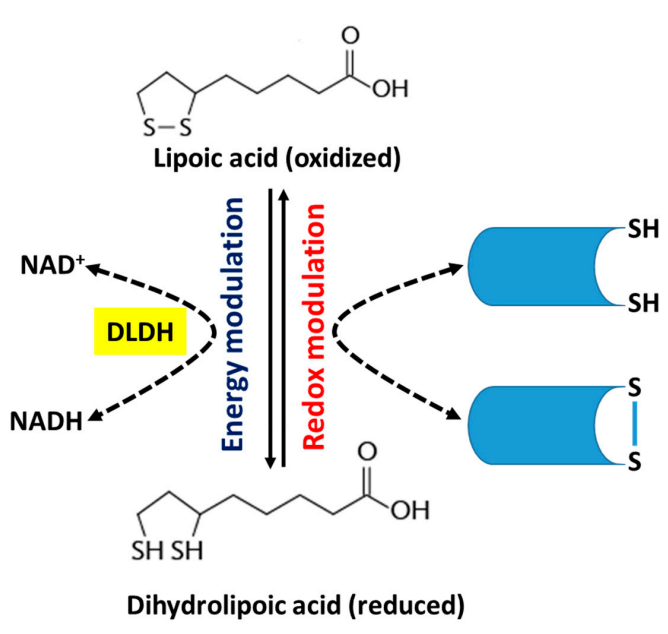
Figura 3. L'àcid lipoic està implicat en els intercanvis tiol-disulfur que modulen l'estat redox i energètic de la cèl·lula.

Figura 4. Accions biològiques de l'àcid lipoic i els seus mecanismes potencials, que inclouen la regeneració de glutatió, vitamines C i E, eliminació de ROS, ions metàl·lics quelants i poder antiinflamatori.

3. Funcions protectores de l'àcid lipoic (ALA) en la lesió renal
Els trastorns renals poden ser induïts per una sèrie d'insults, com ara diabetis, reperfusió isquèmica, toxicitat per fàrmacs, mitjans de contrast i medicaments [7]. Si no es controla, l'IRA pot provocar insuficiència renal amb una taxa de mortalitat del 20% [25]. L'AKI es caracteritza per un augment de la creatinina sèrica, oligúria i la presència de marcadors de dany renal com albuminúria, anomalies electròlits degudes a trastorns tubulars o danys estructurals observats en imatges o histologia [9]. S'ha demostrat que la profilaxi d'ALA disminueix les puntuacions de lesió tubular renal, els marcadors de dany urinari, el dany estructural de la creatinina sèrica i augmenta la filtració glomerular [35]. A les seccions següents, parlarem dels efectes nefroprotectors i dels mecanismes protectors subjacents de l'ALA en una varietat de models animals de lesió renal, tal com s'indica a la figura 1.
3.1. Nefropatia diabètica
La nefropatia diabètica (DN), també coneguda com a malaltia renal diabètica (DKD) [36–38], és una de les principals causes de CKD i insuficiència renal terminal en pacients diabètics [39–41]. Està ben establert que la disfunció mitocondrial contribueix a la DKD, i el mitocondri és un objectiu per combatre la DKD [42–44]. La DN es pot considerar una complicació microvascular de la diabetis mellitus tipus 1 o tipus 2 [7,41]. Aquesta malaltia renal diabètica es caracteritza per una disminució de la filtració glomerular, proteinúria i fibrosi renal [7]. La hiperglucèmia augmenta l'estrès oxidatiu, donant lloc a la sobreproducció primerenca d'espècies reactives d'oxigen (ROS) [45] i a la desregulació de les vies metabòliques del glutatió [7]. El malondialdehid (MDA) és el producte final de la peroxidació lipídica i s'ha utilitzat habitualment com a bon marcador de radicals lliures i estrès oxidatiu [46–49]. Els estudis han demostrat que el pretractament amb ALA va reduir el contingut de MDA i va millorar l'estrès oxidatiu renal [32,50]. S'ha demostrat que la lipoamida, un derivat de l'ALA, inhibeix la fibrosi renal en la diabetis millorant la funció mitocondrial i regulant l'expressió de l'activació del factor transcripcional del receptor X alfa de la retina [51]. En un model de diabetis de rata induïda per nicotinamida juntament amb estreptozotocina, un enfocament que requereix menys temps per crear models de diabetis de rosegadors [52], Dugbartey et al. també han demostrat que el mecanisme de protecció renal de l'ALA implica l'activació del sistema renal de cistationina-liasa/sulfur d'hidrogen [53]. També s'ha demostrat que l'ALA té un efecte sinèrgic en l'atenuació dels nivells sèrics de citocines inflamatòries i en la millora de la funció renal en animals diabètics quan es combina amb l'inhibidor del receptor d'angiotensina II valsartan [54]. La figura 5 mostra una evidència convincent de la tinció histològica que l'ALA presenta forts efectes protectors sobre els ronyons diabètics en un model animal de diabetis tipus 2 [55] El mecanisme de la nefroprotecció de l'ALA en la diabetis és la seva capacitat per activar la via de senyalització Nrf2, que condueix a la regulació de la segona. proteïnes citoprotectores de fase com l'hemoxigenasa-1 (HO-1) i la NAD(P)H quinona deshidrogenasa 1 (NQO1) [56–58]. Cal assenyalar que, tot i que l'ALA és nefroprotector en la malaltia renal diabètica, pot imposar efectes prooxidants o tòxics i podria no servir com a inductor de Nrf2 en determinades condicions fisiopatològiques [59-61]. A més, si bé s'ha pensat que l'ALA activa les vies de senyalització de la insulina per combatre la diabetis [28] i s'ha demostrat que prevé els trastorns cardiometabòlics induïts per alta fructosa i la disfunció renal [62], també s'ha informat que l'ALA només podria atenuar la proteinúria i l'oxidació. estrès sense frenar la progressió de la insuficiència renal diabètica [63].
3.2. Lesió renal induïda per sèpsia
La sèpsia és potencialment una condició patològica que amenaça la vida a causa d'una resposta inflamatòria excessiva a la infecció bacteriana [64–66]. La sèpsia severa pot causar fallades de diversos òrgans, sent el ronyó l'òrgan més afectat [67,68]. S'ha estimat que gairebé el 50% dels pacients sèptics desenvoluparien una lesió renal aguda i no hi ha tractaments efectius per a l'IRA sèptica [69]. En aquest sentit, nombrosos investigadors han avaluat de manera exhaustiva els valors protectors i terapèutics de l'ALA en l'AKI induïda per la sèpsia modelada per injecció de lipopolisacàrids, tot i que ocasionalment s'han utilitzat AKI sèptica induïda per punció i lligadura de cacal (CPL) [22,70]. S'ha demostrat que l'ALA pot protegir contra la lesió renal sèptica millorant l'autofàgia [71]. A més, l'ALA també pot millorar l'AKI induïda per la sèpsia contrarestant la inflamació mitjançant la inhibició de la via de senyalització NF-KB [72], atenuant l'estrès oxidatiu mitocondrial i preservant l'intercanviador de Na+/H+ tipus 3 i l'expressió d'aquaporina 2 al ronyó [73] . L'ALA també pot inhibir l'alliberament de factor de necrosi tumoral, interleucina (IL)-6 i IL{-1 al sèrum i suprimir l'expressió de l'òxid nítric sintasa inducible [22] en AKI sèptica. Per tant, l'ALA podria ser un producte natural prometedor per al tractament de l'IRA sèptica.

3.3. Reperfusió isquèmica renal
La isquèmia es produeix quan hi ha una disminució de la perfusió sanguínia i es redueix el flux sanguini als òrgans [74]; això es deu a moltes causes, com ara trombi, trauma i aterosclerosi [75]. Per prevenir el dany dels teixits i la necrosi, la isquèmia es resol per reperfusió [75]. Tot i que la reperfusió isquèmica és essencial per prevenir la necrosi dels teixits, també pot causar inflamació i un augment de les espècies reactives d'oxigen i les espècies reactives de nitrogen [75–77]. Els estudis han demostrat que el pretractament de l'ALA pot millorar els danys als ronyons, la retina, el sistema nerviós, el fetge, els intestins i més [75]. Els mecanismes protectors subjacents de l'ALA en la lesió per isquèmia-reperfusió renal poden ser multifactorials, inclosa la contraresta del dany oxidatiu [32, 75] i la regulació a la baixa de canals, enzims i transportadors, com ara aquaporines i transportadors de sodi, així com l'ATPasa de sodi i potassi i isoformes d'òxid nítric sintasa [78]. L'ALA també pot protegir la lesió per isquèmia-reperfusió renal mitigant la infiltració de neutròfils i inhibint l'alliberament de mediadors inflamatoris [79]. Els estudis també han demostrat que el dany de l'estructura cortical renal induït per la lesió per isquèmia-reperfusió de les extremitats es pot millorar amb ALA [80] i ALA, i quan es combina amb l'inhibidor de la xantina oxidasa febuxostat, mostra efectes protectors superiors sobre la lesió per isquèmia-reperfusió renal [81] . L'ALA també pot prevenir la disfunció renal i la lesió renal suprimint la sobreexpressió de l'endotelina -1 en la lesió per isquèmia-reperfusió renal [82].
3.4. Obstrucció ureteral unilateral (UUO)-Lesió renal induïda
El model animal d'obstrucció ureteral unilateral (UUO) de lesió renal s'ha utilitzat àmpliament per investigar els mecanismes de lesió renal i els valors terapèutics de nombrosos agents [83–87]. Aquest model té certs avantatges, ja que és un trastorn normotensiu no urèmic en absència de qualsevol agressió inflamatòria o tòxica aparent als ronyons [88]. A més, el model UUO de lesió renal també és un bon model per estudiar la fisiopatologia de la fibrosi renal [89–93]. Per tant, el model UUO de lesió renal pot imitar de prop la fisiopatologia subjacent de la lesió renal obstructiva humana [94,95]. S'ha demostrat que l'ALA és renoprotector contra la lesió renal induïda per UUO [88]. Wongmekiat et al. han trobat que quan es va administrar ALA (60/mg/kg de pes corporal) a rates mitjançant injecció ip dos dies abans de la inducció de l'UUO i va continuar durant una setmana després de l'UUO, la disfunció renal induïda per l'UUO, l'estrès oxidatiu i la producció d'òxid nítric i transformació. factor-1 es va atenuar molt pel tractament amb ALA [88]. A més, també s'ha demostrat que l'ALA millora la transició epitelial-mesenquimal en un model de ratolí de lesió renal UUO [96]. Així, aquests estudis demostren que l'ALA és nefroprotector contra la lesió renal induïda per UUO.
3.5. Nefrotoxicitat induïda per cisplatí
El cisplatí és un fàrmac de quimioteràpia que tracta el càncer entrant a les cèl·lules tumorals, alliberant ions de clorur i hidratant-se per reticular-se amb l'ADN i formar adductes d'ADN per inhibir la replicació de les cèl·lules tumorals [97,98]. Tanmateix, la medicació amb cisplatí té molts efectes secundaris, com ara ototoxicitat, neurotoxicitat, nefrotoxicitat, nàusees i vòmits [35,97–99]. La nefrotoxicitat es produeix perquè el cisplatí és absorbit per les cèl·lules tubulars proximals i es pot concentrar fins a cinc vegades més que el cisplatí en el sèrum [35,97]. La nefrotoxicitat del cisplatí condueix a una disminució de l'eliminació de la creatinina, augment dels nivells de creatinina sèrica, augment dels nivells d'urea, augment de la producció d'orina i disminució de la taxa de filtració glomerular 100,1011. El cisplatí també disminueix els antioxidants glutatió S-transferasa, glutatió peroxidasa i superòxid dismutasa, provocant una elevació de ROS i marcadors oxidatius com el MDA derivat de la peroxidació lipídica [35,100,102]. Els túbuls proximals dels ronyons contenen grans quantitats de mitocondris (35). El cisplatí hidrolitzat crea un metabòlit amb càrrega positiva, i aquest s'acumula dins dels mitocondris a causa de les molècules carregades negativament dels mitocondris, creant alts nivells d'estrès oxidatiu (35) Per gestionar-ho, els mitocondris utilitzar antioxidants endògens com l'àcid lipoic per reduir ROS (351. Els estudis han demostrat que l'ALA protegeix les cèl·lules renals contra la toxicitat del cisplatí (98], disminueix el dany tubular proximal estructural i augmenta la filtració glomerular als ronyons (99,103).) També s'ha demostrat que l'ALA reduir els nivells de creatinina plasmàtica i la producció d'orina, augmentar l'eliminació de creatinina i l'osmolalitat de l'orina i normalitzar l'excreció de sodi en la lesió renal de cisplatí [101].

3.6. Nefrotoxicitat induïda per àcid fòlic
Els alts nivells d'àcid fòlic poden causar danys tubulars pel despreniment i la dilatació de les cèl·lules tubulars [104], donant lloc a la mort cel·lular [105]. La ferroptosi és un tipus de mort cel·lular causada per la peroxidació de ferro i lípids que es produeix durant l'IRA induïda per l'àcid fòlic [106]. Quan hi ha grans quantitats de ferro al cos, es generen ROS, provocant la peroxidació lipídica, danyant les membranes lipídiques i causant la mort cel·lular [105]. S'ha establert que els efectes antioxidants de l'ALA van donar lloc a una renoprotecció contra el dany renal induït per l'àcid fòlic [105]. En l'estudi de Li et al., no hi va haver cap diferència significativa entre les dosis baixes i les dosis altes d'ALA, cosa que indica que els beneficis de l'ALA no depenen de la dosi [105]. A més, l'ALA pot funcionar bloquejant que p53 provoqui ferroptosi i regulant els exportadors de ferro de ferritina i ferroportina, evitant així l'AKI induïda per l'àcid fòlic [105]. La figura 6 mostra histològicament la visualització de la protecció de l'ALA contra la lesió renal induïda per l'àcid fòlic [105].
3.7. Nefrotoxicitat induïda pel cadmi
El cadmi és un metall pesat tòxic natural que causa nefrotoxicitat [104,107–109]. La nefrotoxicitat induïda pel cadmi augmenta els nivells de MDA, causant danys als mitocondris renals i a l'escorça renal [110]. També s'ha demostrat que el cadmi disminueix l'antioxidant de glutatió (GSH), la glutatió peroxidasa, la catalasa i la superòxid dismutasa (SOD) [110].
El tractament amb ALA va funcionar com a antioxidant per disminuir la MDA i l'apoptosi i quelat el cadmi per reduir el dany del cadmi als ronyons [111]. L'ALA també va reduir l'estrès oxidatiu, va promoure enzims endògens relacionats amb el glutatió i va prevenir l'apoptosi mitocondrial en lesions renals induïdes pel cadmi [110–112].
3.8. Lesió renal aguda induïda pel ferro
S'ha pensat que el ferro contribueix tant a l'IRA com a la CKD [113–118]. De fet, s'ha observat que els túbuls renals estan exposats a nivells elevats de ferro en pacients amb malaltia renal, que probablement es deu a l'augment de la filtració de ferro i proteïnes que contenen ferro a través de l'aparell glomerular [114,117,119]. El ferro també pot agreujar la malaltia renal diabètica augmentant l'estrès oxidatiu [120,121]. Per tant, els models animals de lesió renal induïts pel ferro han estat una eina valuosa per estudiar els mecanismes de lesions renals induïdes pel ferro i provar els efectes terapèutics de productes naturals o fàrmacs farmacèutics [122–125]. En aquest sentit, s'ha demostrat que l'ALA és nefroprotector en la lesió renal induïda per ions [126,127]. En un model de lesió renal de rata amb sobrecàrrega de ferro, es va trobar que l'ALA presentava efectes antioxidants atenuant el dany oxidatiu [128]. També es va trobar que l'ALA inhibeix la senyalització de p38 MAPK i l'expressió de NADPH oxidasa 4 en lesions renals induïdes pel ferro [127]. Cal tenir en compte que tots aquests efectes protectors de l'ALA en la lesió renal induïda pel ferro poden ser en part deguts a la seva propietat quelant el ferro [128–131], que redueix la disponibilitat de ferro lliure.
Servei de suport:
Correu electrònic:wallence.suen@wecistanche.com
Whatsapp/Tel:+86 15292862950
Botiga:
https://www.xjcistanche.com/cistanche-shop






