La diferència entre la lesió renal aguda de COVID-19 (AKl) i la sèpsia-AKI (S-AK)
Mar 20, 2022
ali.ma@wecistanche.com
PART Ⅱ: La lesió renal aguda en la COVID-19 greu-19 té similituds amb la lesió renal associada a la sèpsia: un estudi multiòmic
Mariam P. Alexander, MD; Kiran K. Mangalaparthi, PhD & et al.
RESUM
Objectiu: comparar la malaltia coronavirus 2019(COVID-19) lesió renal aguda (AKl)asèpsia-AKI(S-AKI). Es va analitzar la morfologia i les característiques transcriptòmiques i proteòmiques dels ronyons d'autòpsia. Pacients i mètodes: es van incloure persones de 18 anys o més que van morir per COVID-19 i que se'ls va fer una autòpsia a la Clínica Mayo entre l'abril de 2020 i l'octubre de 2020. Es va realitzar una avaluació morfològica dels ronyons de 17 persones amb COVID-19. En un subconjunt de set casos de COVID-19 amb intervals post mortem inferiors o iguals a 20 hores. Es van avaluar les característiques ultraestructurals i moleculars (anàlisis dirigides de transcriptoma i proteòmica del tubulointerstici). Es van comparar les característiques moleculars amb els casos arxivats de S-AKI(sèpsia-AKI)causes de l'IRA i no sèpsia (lesió renal aguda). Resultats: l'espectre de la patologia renal COVID-19 incloïa inflamació microvascular dominant en macròfags (glomerulitis i capil·laritis peritubular), disfunció vascular (congestió capil·lar peritubular i lesió endotelial) i lesió tubular amb evidència ultraestructural de dany mitocondrial. La investigació de l'arquitectura espacial mitjançant una nova citometria de massa d'imatge va revelar l'enriquiment de les cèl·lules T CD3fCD4 a prop de les cèl·lules presentadores d'antigen i infiltrats glomerulars i intersticials enriquits amb macròfags, cosa que suggereix una resposta de teixit immune innat i adaptatiu. Malaltia per coronavirus 2019 AKI(COVID-19 lesió renal aguda)i S-AKI(sèpsia-AKI), en comparació amb l'AKI no sèptica, tenia un enriquiment de les vies transcripcionals implicades en la inflamació (apoptosi, autofàgia, complex d'histocompatibilitat major classe I i ll i diferenciació de cèl·lules auxiliars de tipus IT). L'anàlisi de la via proteòmica va demostrar que COVID-19 AKI(COVID-19 lesió renal aguda)i en menor mesura S-AKI(sèpsia-AKI)es van enriquir en vies de necroptosi i de senyalització de sirtuïnes, ambdues implicades en la resposta reguladora a la inflamació. Regulació a l'alça de la via de senyalització de la ceramida i regulació a la baixa de la fosforilació oxidativa en COVID-19 AKI(COVID-19 lesió renal aguda)es van assenyalar.
Conclusió: aquestes dades posen de manifest les similituds entre S-AKI(sèpsia-AKI) i COVID-19 AKI(COVID-19 lesió renal aguda)i suggereix que la disfunció mitocondrial pot tenir un paper fonamental en la COVID-19 AKI(COVID-19 lesió renal aguda), Aquestes dades poden permetre el desenvolupament de noves dianes diagnòstiques i terapèutiques.

Feu clic a Cistanche UK malaltia renal
FEU CLIC AQUÍ PER PART Ⅰ
DISCUSSIÓ
El nostre estudi va examinar les característiques morfològiques i moleculars dels ronyons obtinguts durant les autòpsies de pacients que van morir de COVID{0}}. El perfil morfològic i molecular de la lesió renal greu de COVID-19 s'assembla a l'S-AKI(sèpsia-AKI). Això inclou una disfunció microvascular amb inflamació, és a dir, un fenotip cel·lular dominant en macròfags i una resposta destacada de cèl·lules T al tubulointerstici molt a prop de les cèl·lules presentadores d'antigen observades en l'anàlisi de l'arquitectura espacial. La disminució de la fosforilació oxidativa i la regulació a l'alça de les vies de senyalització de la ceramida amb evidència ultraestructural de lesió mitocondrial observada en COVID-19 AKI(COVID-19 lesió renal aguda)indica una reprogramació metabòlica de cèl·lules epitelials tubulars que s'han descrit a S-AKI(sèpsia-AKI).
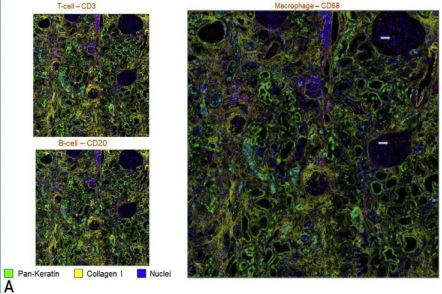
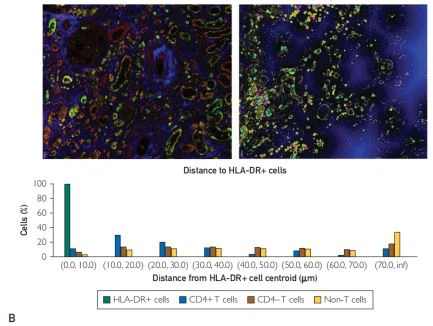
FIGURA 3. Citometria de massa d'imatge Hyperion que mostra la immunofenotipat simultània de cèl·lules inflamatòries i components estructurals renals amb l'exploració de la seva relació espacial.(A) Presència de cèl·lules T (esquerra, superior) i macròfags (dreta) al compartiment tubulointersticial amb una absència notòria de cèl·lules B (esquerra, inferior). La glomerulitis s'aprecia al panell dret amb la marginació dels macròfags (fletxes). Totes les cel·les d'interès s'han marcat en vermell. (B) L'anàlisi del barri d'imatges computacionals es va realitzar després d'etiquetar els túbuls (Pank i E-cadherina), l'estroma intertubular (col·lagen i actina del múscul llis alfa) i els glomèruls (vimentina) (esquerra). Després de classificar les cèl·lules mitjançant un enfocament supervisat (cèl·lules T CD4+, cèl·lules T CD4- i cèl·lules no T), es va generar un mapa de distància que mesurava la distància més propera des de les cèl·lules HLA-DRþ a cadascuna de les altres cèl·lules. (al mig, HLA-DR en groc, distància de HLA-DR mostrada en intensitat creixent de color blau). Es mostra el percentatge de cel·les dins de cada safata de distància definida (dreta).
COVID-19-Resposta inflamatòria associada
En general, els ronyons COVID-19 tenien una inflamació significativament més gran en comparació amb NS-AKI(sèpsia-AKI)controls. Els senyals moleculars d'inflamació i activació immune observats als ronyons de la COVID{0}} suggereixen una resposta antiviral global caracteritzada per una inflamació rica en macròfags i cèl·lules T i la producció d'interferó de tipus II, tal com suggereixen àmpliament els assajos basats en sang.20.21. La resposta de les cèl·lules T dominants CD4 plus, tal com vam observar als ronyons de la COVID-19, s'ha associat amb pitjors resultats clínics.22 Cèl·lules T CD4 plus específiques del coronavirus 2-síndrome respiratòria aguda severa dirigides a l'espiga s'han detectat glicoproteïnes superficials en pacients amb COVID-19 greu i poden explicar les cèl·lules T CD4 més que es troben al compartiment tubulointersticial dels ronyons. Les vies moleculars, investigades tant a nivell genòmic com proteòmic, van confirmar que la inflamació és el motor predominant de la lesió renal observada en COVID-19, similar a la S-AKI.(sèpsia-AKI).En ambdós grups, vam trobar una expressió més gran de conjunts de gens associats amb mecanismes contrareguladors que normalment es veuen en l'activació immune, inclosa la diferenciació de Treg i la senyalització de sirtuïnes. En casos greus de COVID-19, un augment de la freqüència de Treg circulant s'associa amb pitjors resultats, presumptes secundaris a la supressió de les respostes antivirals de les cèl·lules T.

COVID-19-Vies de senyalització associades als ronyons COVID-19, així com a S-AKI(sèpsia-AKI), vam trobar proves d'augment de l'apoptosi. Tot i que l'apoptosi està potencialment mediada pel virus a través de les vies extrínseques, la via de la ceramida regulada a l'alça que s'observa a la nostra AKI COVID-19(COVID-19 lesió renal aguda)La cohort juntament amb els senyals reduïts de fosforilació oxidativa suggereixen que l'apoptosi induïda per la ceramida mitjançant la interrupció mitocondrial podria tenir un paper en la mort de les cèl·lules tubulars. Els mitocondris de les cèl·lules epitelials tubulars proximals dels ronyons de la COVID-19 van mostrar una vacuolització i una distorsió marcades de les crestas, tal com s'ha descrit anteriorment.2 La via de la ceramida regulada a l'AKI de COVID-19 subratlla el paper de la desregulació dels lípids en COVID greu-19 tal com suggereixen altres. La necroptosi, una via de mort de cèl·lules immunogèniques que pot eliminar les cèl·lules infectades pel virus i mobilitzar respostes immunitàries tant innates com adaptatives per restringir la replicació del virus, també va ser més profunda als ronyons de COVID-19, en comparació amb NS-AKI.(sèpsia-AKI). La necroptosi té un paper important en la lesió pulmonar SARS-COV2 després de la infecció.26,30,31.

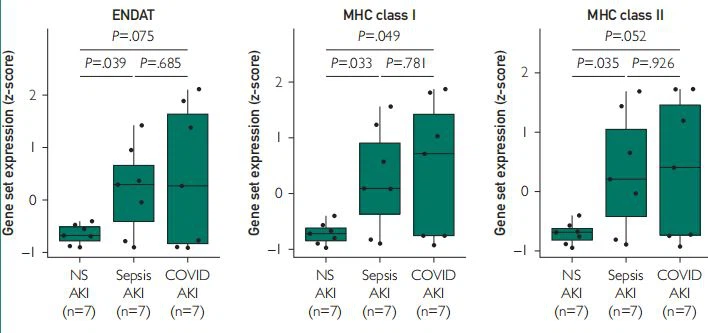
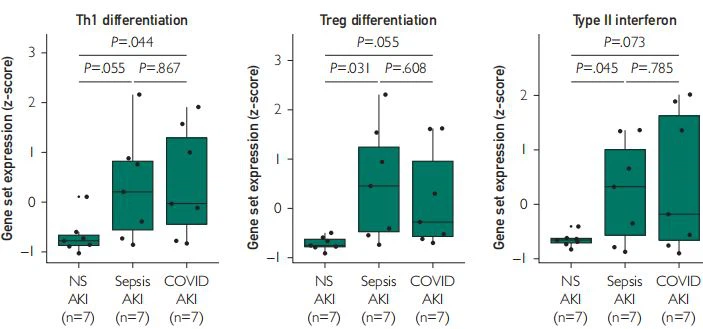
FIGURA 4. Anàlisi transcriptòmica.Els diagrames de caixa mostren l'expressió relativa de conjunts de gens d'anotació funcional seleccionats entre la lesió renal aguda (AKI) de la malaltia del coronavirus 2019 (COVID-19), la IRA relacionada amb la sèpsia (S-AKI) i la IRA no relacionada amb la sèpsia (NS-AKI) . ENDAT, transcripcions associades a cèl·lules endotelials; MHC, complex major d'histocompatibilitat; Th1, cèl·lula auxiliar T tipus 1; Treg, cèl·lula T reguladora.
COVID-19 AKI S'assembla a l'AKI associada a la sèpsia
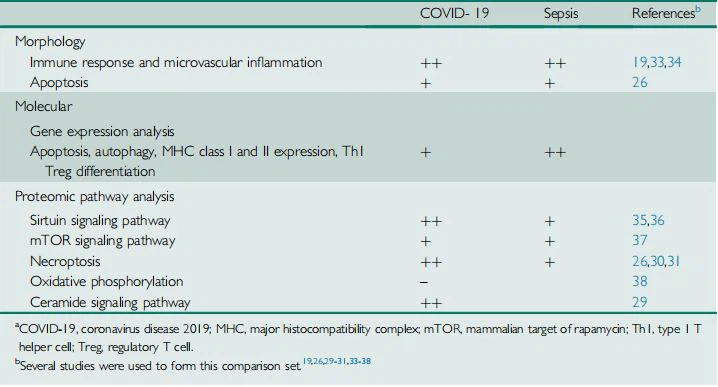
Kellum et al6 i altres han suggerit que la COVID-19 AKI és molt semblant a la S-AKI(sèpsia-AKI). Les nostres observacions de la disfunció microvascular, la inflamació i la reprogramació metabòlica (disminució de la fosforilació oxidativa i augment de la senyalització de la ceramida) en COVID-19 AKI(COVID-19 lesió renal aguda)són similars als mecanismes fisiopatològics fonamentals descrits a S-AKI(sèpsia-AKI).1933,3 Resumim les conclusions clau del nostre estudi i fem comparacions amb la literatura publicada sobre COVID-AKI(COVID-19 lesió renal aguda)i S-AKI(sèpsia-AKI)a la taula 4.19,26,29,31,3-38 Aquestes patologies mostren dianes terapèutiques potencials per a la COVID-19.
Limitacions de l'estudi
La principal limitació de l'estudi actual és que, tot i que teníem la capacitat de comparar les característiques moleculars de la patologia relacionada amb la COVID{0}}contra l'S-AKI(sèpsia-AKI)les autòpsies, no vam poder comparar-les amb les autòpsies de pacients que van morir per una altra IRA mediada per virus. Això requereix planificació i estudis prospectius per obtenir una preservació òptima del teixit d'autòpsia per als estudis òmics. Els artefactes de preservació observats en estudis ultraestructurals de teixits d'autòpsia no COVID-19 fixats amb formalina arxivats de pacients anteriors no van permetre la comparació. A més, l'anàlisi estadística no es va ajustar per a proves múltiples i una mida de mostra més gran podria haver proporcionat una anàlisi d'expressió gènica més robusta. La fortalesa del nostre estudi és que vam poder realitzar una anàlisi morfològica detallada i un enfocament de plataforma multiòmica per estudiar la lesió renal greu de COVID-19 i establir paral·lelismes amb les lesions associades a la sèpsia.

FIGURA 5. Anàlisi proteòmica.(A) El mapa de calor ofereix una visió global de l'expressió diferencial dels nivells de proteïnes per a cada gen individual a les tres cohorts de lesió renal aguda (AKI). Proteïnes que estaven significativament sobreexpressades (vermell) o subexpressades (blau) a P<.05 are="" shown.="" (b)="" the="" ingenuity="" pathway="" analysis="" of="" differential="" protein="" expression="" in="" coronavirus="" disease="" 2019="" (covid-19)="" aki,="" sepsis-associated="" aki,="" and="" other="" aki="" controls="" is="" shown.="" eif2,="" eukaryotic="" initiation="" factor="" 2;="" mtor,="" mammalian="" target="" of="" rapamycin;="" nrf2,="" nuclear="" factor="" erythroid="" 2erelated="" factor="">
CONCLUSIÓ
Aquesta sèrie està dedicada a les troballes histopatològiques, ultraestructurals i moleculars renals en pacients amb infecció per SARS-CoV-2, que proporciona evidència d'una resposta immune innata i destacada de cèl·lules T. Les característiques morfològiques i moleculars de la COVID-19 AKI(COVID-19 lesió renal aguda)s'assemblen als de S-AKI(sèpsia-AKI). La disfunció mitocondrial pot tenir un paper central en l'AKI COVID-19(COVID-19 lesió renal aguda).
TAULA 4. Comparació morfològica i molecular d'AKI COVID-19 i AKI de sèpsia
REFERÈNCIES
Hirsch JS, Ng JH, Ross DW, et al.Lesió renal agudaen pacients hospitalitzats amb COVID-19.Kidney Int 2020;98(I):209-218.
Pei G.Zhang Z, Peng et al Implicació renal i pronòstic precoç en pacients amb pneumònia COVID-19.JAm Soc Nephrol. 2020;3I(6):1 I57-1I65.
Cheng Y, Luo R, WangK et al. La malaltia renal s'associa amb la mort intrahospitalària de pacients amb COVID-19. Kidney Int 2020;97(5):829-838.
Felicitats S.Batal lSantoiello D, et al Kidney biopsy finding inpatients with COVD-19.JAm Soc Nephral.202031(9):1959-1968.
Su H Yang M, Wan C, et al Anàlisi histopatològica renal de 26 troballes postmortem de pacients amb COMD.19 a la Xina. Ronyó Int. 2020;98(I):219-227.
Santoriello D, Khairallah P, BombadkAS, et al. Trobades de patologia renal postmortem en pacients amb COVID.19.Sóc Soc Nephrol.20203I9)2158-2167.
