Determinació estructural de RMN inequívoca de (plus)-catequina-productes de reacció dimèrica de lacasa com a marcadors potencials d'oxidació del raïm i del vi
Mar 12, 2022
Per a més detalls, poseu-vos en contacte amb:tina.xiang@wecistanche.com
Resum:( més )-Catequina—laccaseoxidacióEls estàndards dimèrics es van sintetitzar hemisintetitzar mitjançant lacasa de Trametes Versicolor és una solució d'aigua-etanol a pH 3,6. Es van detectar vuit fraccions corresponents a vuit productes dimèrics d'oxidació potencials. Els perfils de fraccions es van comparar amb els perfils obtinguts amb altres dues oxidoreductases:polifenol oxidasaextret del raïm i lacasa de Botrytis cinerea. Els perfils eren molt similars, tot i que algunes diferències menors van suggerir possibles diferències en la reactivitat d'aquests enzims. Després es van aïllar cinc fraccions i es van analitzar mitjançant espectroscòpia RMN 1D i 2D. L'addició de traces de nitrat de cadmi a les mostres solubilitzades en acetona va conduir a senyals de RMN de protons fenòlics completament resolts, permetent la determinació estructural inequívoca de sis productes de reacció, una de les fraccions que conté dos enantiòmers. Aquests productes també es poden utilitzar com a marcadors d'oxidació per investigar la seva presència i evolució en el vi durant l'elaboració i la criança del vi.
Paraules clau: marcador d'oxidació;( més )-catequina; senyals de RMN fenòlics; lacasa; nitrat de cadmi; polifenol oxidasa

Feu clic per obtenir més informació
1. Introducció
Polifenolssón una família de compostos químics molt presents a la natura. Es troben en quantitats importants en te [1], cacau [2,3], nabius [4], raïm [5l i productes fermentats com el vi [6]. En ser objectius d'oxidació primaris J7,8], les estructures químiques dels polifenols evolucionen contínuament. Aquests canvis afecten les propietats organolèptiques de molts tipus d'aliments; són responsables de fenòmens com l'enrossament dels aliments [9] i les modificacions de les característiques sensorials del vi [10,11. En enologia, aquest fenomen d'oxidació té lloc al raïm o als vins. Pel que fa a l'oxidació enzimàtica, els principals enzims responsables del marronament són les oxidoreductases, més precisament,polifenol oxidasapresent en el raïm i la lacasa produïda per Botrytis cinerea [12].
Enzimàticoxidacióes produeix principalment en el most de raïm, però l'enrossament del vi pot ser degut a reaccions químiques d'oxidació |7,13]o a la lacasa de Botrytis cinerea que pot ser molt estable durant la criança del vi14. Es poden produir dues activitats enzimàtiques d'oxidació sobre substrats fenòlics: activitat monofenol oxidasa caracteritzada per la hidroxilació d'un grup hidroxil existent en posició adjacent i activitat difenol oxidasa corresponent a l'oxidació d'orto-dihidroxibenzens a orto-benzoquinones.
Segons el Comitè de Nomenclatura de la Unió Internacional de Bioquímica i Biologia Molecular (NC-IUBMB), aquestes activitats enzimàtiques estan catalitzades per enzims de classe EC1- corresponents a les oxidoreductases. Entre elles, les tres classes principals d'oxidoreductases que catalitzen l'oxidació de polifenols són EC1.14.18.1 (monofenol monooxigenasa), EC1.11.1 (peroxidasa/POD) i EC1.10.3 (oxidoreductases que actuen sobre difenols).
Aquesta darrera classe es divideix en diferents subclasses, i dues d'elles van semblar especialment interessants per a aquest estudi: EC1.10.3.1 (polifenol oxidasa/PPO) i EC1.10.3.2 (laccase) (vegeu la figura S1 de materials suplementaris).
La PPO, la lacasa i la peroxidasa són les oxidoreductases principalment responsables del daurament durant el processament del raïm [13]. El daurament causat per la POD és insignificant a les fruites, però pot augmentar la degradació dels fenols quan es combina amb PPO[15]. El PPO està present de manera natural al raïm i és capaç de catalitzar l'oxidació de monofenols a catecols i de catecols a pigments marrons [8,13,16]. Les lacass, que es troben en els raïms infectats per Botrytis, tenen un espectre d'acció més ampli|17|ja que poden catalitzar l'oxidació de molts substrats diferents. Els principals objectius d'oxidació de les lacases segueixen sent el 1-2 i el 1-4 dihidroxibenzè.
En el vi, la benzoquinona produïda per oxidació (PPO o lacases) pot experimentar fàcilment reaccions addicionals depenent de les seves propietats redox i afinitats electròniques [15]. Poden actuar com a electròfils i reaccionar amb derivats aminos [18] o actuar com a oxidants i reaccionar, entre d'altres, amb substrats fenòlics. Segons la seva conformació química (quinona o semiquinona), la benzoquinona pot donar lloc a diferents productes de reacció d'oxidació. A un pH neutre, la (+)-catequina s'oxidarà a quinona a la posició de l'anell A C5 o C7 i donarà lloc a la formació de sis possibles isòmers dimèrics que impliquen un enllaç entre la posició de l'anell B C2', C5' o C6' de la unitat de catequina superior i la posició de l'anell A C6 o C8 de la unitat inferior [19,20]. La dehidrodicatequina és un producte conegut d'aquest acoblament [21]. Les posicions d'etiquetatge de les estructures es mostren a la figura 1. En condicions àcides, les formes semi-quinona també poden estar presents a l'anell B (posició OH3'o OH4') i conduir a quatre possibles isòmers dimèrics [20,22] amb la unitat de catequina superior i l'anell A de la unitat inferior (posició C6 o C8). L'oxidació enzimàtica de la catequina es va investigar en estudis anteriors [22, 23], i els productes d'oxidació associats es van caracteritzar per HPLC [24], encara que més rarament aïllats i mai completament caracteritzats per RMN.

L'objectiu d'aquest treball va ser en primer lloc comparar mitjançant UHPLC-MS els perfils de productes d'oxidació de dimèric(plus)-catequina en presència de tres extractes d'oxidoreductasa, és a dir, PPO extret del raïm, lacasa del fong Botrytis cinerea present en vins dolços botrititzats. [14], i lacasa de Trametes Versicolor.
El segon objectiu va ser hemisintetitzar i caracteritzar les estructures d'alguns productes d'oxidació dimèrica mitjançant espectroscòpia RMN obtinguda amb lacasa de Trametes Versicolor.

2. Resultats i discussió
2.1. Comparació de perfils de productes de reacció dimèrica amb tres oxidoreductases diferents i (a més)-catequina
(a més)-La catequina es va oxidar per primera vegada en presència de lacasa de Trametes Versicolor a pH 3,6 a la solució de vi model. Després de la separació de la fracció dimèrica de la catequina residual (més) i altres fraccions polimèriques, es van recollir i analitzar vuit fraccions principals mitjançant UHPLC-UV-MS, anotades de N1 a N8 en ordre creixent de temps de retenció (taula 1). Els espectres de masses electrospray en mode positiu van mostrar els pics d'ions [M més H] més a m/z 579 per N1 a N6, hipotèticament corresponents a un dímer format per un únic enllaç entre dues unitats de catequina, i [M més H] més a m/577 per a N7 i N8, suggerint hipotèticament la formació d'un enllaç addicional.

Aquests vuitoxidacióLes fraccions es van observar potencialment després de la despolimerització química d'una fracció de taní en treballs anteriors [25, 26] i possiblement podrien ser les mateixes que les ja descrites per Guyot et al. [20], encara que les condicions experimentals fossin lleugerament diferents. De fet, en aquest estudi anterior, es va utilitzar un extracte de PPO brut a pH 3 i 6 per obtenir vuit fraccions. En el present estudi, es van comparar tres enzims diferents a pH 3,6 a la solució de vi model. L'anàlisi comparativa LC-MS de les principals fraccions d'oxidació obtingudes amb els tres enzims diferents (laccasa de Trametes Versicolor, lac-cas de Botrytis cinerea i polifenol oxidasa extreta del raïm) es presenten a la taula 2. Per a cadascuna de les vuit fraccions, els temps de retenció eren gairebé idèntics als diferents enzims, i es van determinar m/z similars amb l'anàlisi de MS. Aquests resultats donen suport a la hipòtesi que es van obtenir les mateixes fraccions per a cada enzim, que contenien productes amb estructures similars a les hipotetitzades per Guyot et al. [20]. Lopez-Serrano i Ros Barcel6 [27] també van realitzar un estudi comparatiu dels productes d'oxidació de (plus)-catequina amb dos enzims diferents: peroxidasa i polifenol oxidasa, tots dos extrets de maduixes. Van concloure que els productes obtinguts amb els dos enzims eren qualitativament els mateixos. Un compost addicional anomenat N4' amb m/z=578 Th i Rt=15,66 min es va observar en experiments amb lacasa de Botrytis cinerea i extreu PPO però no amb lacasa de Trametes Versicolor, cosa que suggereix possibles diferències. en reactivitat per a aquests enzims.
2.2. Estudi i optimització de paràmetres fisicoquímics en senyals OH fenòlics i alifàtics 1H-RMN
La caracterització estructural dels dímers de procianidines es pot obtenir mitjançant anàlisi de RMN. En particular, la posició precisa d'enllaç entre les unitats es pot determinar mitjançant espectres de correlació HMBC i/o ROESY [28, 29] (figures S2 i S3). En el cas d'un enllaç de tipus èter (COC), és necessària l'atribució dels protons senyal hidroxil. També pot ser crucial en el cas dels enllaços CC si alguns protons alifàtics o aromàtics es superposen o si falten algunes correlacions clau. Tanmateix, fins i tot en un dissolvent apròtic, els protons hidroxil dels polifenols apareixen sovint com a senyals amplis dels quals no es pot obtenir informació estructural [30]. Aquest problema es va solucionar provisionalment afegint rastres de
Cd(NO3)2 a les solucions mostra. De fet, els senyals amplis H dels grups OH es deuen a l'intercanvi intermolecular entre aquests protons OH i altres protons del dissolvent o solut. En reduir els enllaços intermoleculars, la presència de nitrat de cadmi a les mostres pot disminuir aquests intercanvis, millorant així la nitidesa dels senyals de protons OH.
2.2.1.Efecte de l'addició de cadmi
Després de la liofilització, les cinc fraccions N2, N3, N4, N6 i N8 es van solubilitzar en acetona-dg. Aleshores, es van adquirir espectres de RMN de protons 1D a 25 graus abans (figura 2A) i després d'afegir petites quantitats de cadmi (figura 2B). En acetona-d. pura, els protons OH fenòlics de totes les fraccions van aparèixer com a pics amplis. Després de l'addició de cadmi, aquests protons van mostrar senyals molt resoltes en el cas de les fraccions N6 i N8, mentre que per a les fraccions N2, N3 i N4 els senyals eren només una mica més nítids. També cal esmentar que l'augment del contingut de Cd no va tenir cap efecte sobre la resolució del senyal OH, ja que no es va observar nitidesa ni amplitud de l'amplada de línia màxima quan es van afegir petites quantitats successives de Cd a les mostres (dades no mostrades).

Els senyals OH fenòlics altament resolts dels productes N2, N3 i N4 es van aconseguir gràcies a un assecat i resolubilització addicionals (figura 2C, D).

La diferència de comportament després de l'addició de Cd entre les fraccions es pot explicar per la força de les interaccions moleculars: més forta en el cas de N2, N3 i N4 en comparació amb N6 i N8, sent necessari un pas més per trencar aquests enllaços.
Aquest pas addicional pot ser el pas clau quan s'utilitza Cd per obtenir senyals OH fenòlics d'alta resolució en qualsevol situació, sigui quin sigui l'origen de les mostres, la reacció de síntesi o els productes polifenòlics naturals.
Un treball previ tractant de la caracterització estructural inequívoca depolifenoldímers que utilitzen senyals de RMN fenòlics OH altament resolts gràcies a l'addició de nitrat de cadmi es van publicar el 1996[30]. Segons el nostre coneixement, des d'aleshores no s'ha publicat cap altre treball de recerca que utilitzi aquesta metodologia. Posteriorment es van dur a terme altres investigacions per assolir aquest objectiu, ja sigui mitjançant addicions dosificades d'àcid pícric [31] o utilitzant una temperatura d'adquisició baixa [32]. Això es pot explicar pel pas addicional necessari per obtenir un efecte decisiu sobre la nitidesa del pic d'OH amb l'addició de Cd, tal com es descriu anteriorment. Tanmateix, el cadmi sembla ser de gran valor, ja que es poden obtenir senyals altament resoltes sense necessitat d'afegir quantitats precises, en contrast amb l'adquisició d'àcid pícric o espectres de RMN a baixes temperatures.
2.2.2. Efecte de la temperatura
Una disminució de la temperatura de 25 graus C a 15 graus no va tenir cap impacte en la nitidesa dels senyals d'OH fenòlic o OH alifàtic. No obstant això, els desplaçaments cap avall dels pics de protons intercanviables ens van permetre separar alguns senyals OH fenòlics i alifàtics superposats, fent-ne més evident la identificació (figura 3). En disminuir la temperatura, es va reduir la taxa de canvi de protons i es podria esperar pics d'OH alifàtics més aguts [31]. La temperatura de 15 graus, òbviament, no és prou baixa per obtenir senyals OH alifàtics ben resolts. Tanmateix, ens va permetre identificar clarament la ressonància de dos protons OH alifàtics a les mostres N3 i N6 i d'un a la mostra N8. L'espectre de la mostra N2 també mostrava dos senyals de protons alifàtics OH, que eren més distingibles a 25 graus C que a 15 graus (figura 2E). En el cas de la mostra N4, els senyals derivats de l'OH alifàtic només eren parcialment visibles en el espectres, tant si la temperatura es va establir a 25 graus com a 15 graus C, a causa de la superposició persistent (figura 2E).

2.3.Caracterització estructural dels estàndards dimèrics—Anàlisi de l'espectre de RMN
Els espectres de RMN de les fraccions N2, N3, N4, N6 i N8 van mostrar que els productes d'oxidació eren d'alta puresa, ja que les intensitats del senyal d'altres compostos detectats eren inferiors al 10% en comparació amb les d'aquests productes.
En tots els espectres, es poden distingir quatre regions de desplaçament químic lH típiques de les unitats de catequina (figura 2C): els senyals dels protons alifàtics dels anells de pirans (anells C) es troben a la regió de 2,3 a 5. 0 ppm, i els dels protons senyal aromàtics dels anells de resorcinol (anells A) i dels anells de catecol (Brings) de 5,5 a 6,3 ppm i de 6,3 a 7,1 ppm, respectivament. Els senyals de fenol OH dels anells A i B van aparèixer de 7,1 a 10 ppm. Els espectres de RMN d'ambdues fraccions van mostrar la presència de diferents conjunts de senyals d'unitats de catequina en una relació d'intensitat constant: es van observar dos conjunts de senyals en els espectres de les fraccions N2, N3, N6 i N8 d'acord amb la presència de dímers, i quatre conjunts en l'espectre N4, que poden correspondre a un tetràmer, dos dímers o una barreja de diferents oligòmers, és a dir, un trímer més un monòmer. Per tal de determinar el grau d'oligomerització dels productes presents a la fracció N4, es va realitzar un experiment 'H DOSY amb una mescla que contenia alíquotes de les dues fraccions N4 i N2. Els coeficients de difusió de tots els senyals mostraven valors similars (figura 4), cosa que indica la presència de dos dímers de catequina a la fracció N4.

Gràcies als senyals de fenol OH totalment resolts que proporcionen resultats quantitatius fiables, el tipus d'enllaç entre les unitats de catequina es pot deduir directament de la integració de la superfície màxima. Així, per a ambdues fraccions, N3 i N6, la manca d'un OHfenol (que pertany al resorcinol o a un anell de catecol) i la manca d'un protó aromàtic de resorcinol van indicar un enllaç interflavànic (IFL) de tipus èter que implica una oposició en un A. o anell B i una posició C6 o C8 en un anell A. En el cas de la mostra N2, faltaven dos protons aromàtics, un d'anell B i un altre d'anell A, la qual cosa implica un CA-CB IFL. L'espectre 1D 'H de la fracció N4 va mostrar que faltaven dos protons de l'anell B, així com dos protons de l'anell A. Els enllaços entre les unitats dímeres de la fracció N4 són, per tant, els dos tipus CC. Els espectres de la fracció N8 eren força diferents dels altres quatre. Alguns senyals eren típics de les unitats de catequina, en què mancaven tres fenols OH, un anell A aromàtic i un protons de l'anell B, així com un OH alifàtic. D'altra banda, alguns altres senyals de RMN són atípics d'una unitat de catequina: metilè amb desplaçaments químics 13C dececs (~ 40 ppm) i un grup cetònic (~ 192 ppm).
Els sistemes de spin de protons dels anells C, A i B es van determinar mitjançant espectres TOCSY "H 1D i 1H 2D" (no mostrats). Es van observar dos sistemes de rotació ABMX C-ring (típic de catequina) als espectres de les fraccions N2, N3, N6 i N8, i quatre per a la fracció N4. En els espectres de les fraccions N2, N3, N6 i N8, es van assignar dos doblets meta-acoblats (J~2Hz) i un únic a la regió de l'anell aromàtic A, respectivament, als protons de l'anell A de la unitat de catequina no enllaçada. i al protó residual de l'anell A de la unitat de catequina lligada a C6-o C8-. En els espectres de N4, a causa de la presència de dos dímers, es van detectar i assignar quatre doblets meta-acoblats i dos singlets tal com s'ha descrit anteriorment. Els sistemes de protons de l'anell B també es van determinar fàcilment a partir d'aquests espectres i ens van permetre identificar dos sistemes de spin de protons ABM per als dímers de les fraccions N3 i N6, mentre que es van detectar un sistema de spin de protons ABM i un AB per al dímer N2, i un ABM i sistemes de spin d'un protó AM per al dímer N4. El dímer N8 només presentava un sistema de rotació de l'anell B ABM típic d'un monòmer de catequina.
2.3.1.Determinació de la posició de l'anell A de l'IFL dels dímers de les fraccions N2, N3, N4 i N6
L'establiment del pont situat a l'anell A dels dímers (és a dir, la posició C6A o C8A) requereix l'atribució del protó HA residual de la unitat de catequina lligada a CA. Gràcies als senyals OH fenòlics altament resolts, un punt de partida fàcil va ser la identificació dels dos protons OHfenols de les unitats enllaçades per anell A, és a dir, l'anell A que
had one isolated lHspin. This may be achieved using lH-13C long-range correlations, as illustrated in Figure5. The OH5A has readily been identified thanks to a correlation with the C4aC. This quaternary carbon is indeed characterized by both its chemical shift at~100 ppm and a long-range correlation observed with the H4Cprotons. OH5A also correlated with two other carbons∶ the most deshielded (δ>145 ppm) was obviously C5A, while the other (6>125 ppm) was C6A, which also showed a correlation with the other OHA phenol proton,i.e., OH7A. This latter correlated with two other carbons: a deshielded quaternary carbon(δ>145ppm) and a more shielded carbon(δ>125 ppm) que es van atribuir fàcilment a C7A i C8A, respectivament. Un cop assignats C6A i C8A, el protó HA residual es pot atribuir directament als espectres HSQC. Així, es va trobar que aquest protó HA residual era H6A per a totes les fraccions N2, N3, N4, N6. Així, l'IFL entre unitats de catequina implicava una posició C8A per a tots els dímers.
2.3.2. Determinació de la posició de l'anell B de l'IFL
Dímers de les fraccions N2 i N4. Els espectres de la fracció N2 van mostrar dos tipus diferents de sistemes d'espin de protons en anell B: un AMX corresponent a l'anell B de la unitat no enllaçada, i un AM amb una constant d'acoblament d'uns 8 Hz, característica de H6'B i H5'. B d'una unitat lligada a C2'B. Per tant, l'enllaç entre les unitats del dímer N2 és C2'B-C8A. Els espectres de RMN de la fracció N4 també van mostrar diferents sistemes d'espin B: dos AMX, corresponents a l'anell B no enllaçat, i dos sistemes AXspin, tots dos mostrant constants d'acoblament d'uns 2 Hz, que són característiques de H2'B i H6'. Protons B d'unitats lligades a C5'B. La presència de correlacions H/13C de llarg abast entre H6'Band C8A, que es van observar en els espectres HMBC dels dos dímers, estan d'acord amb un enllaç C5/'B-C8A (figura 5).
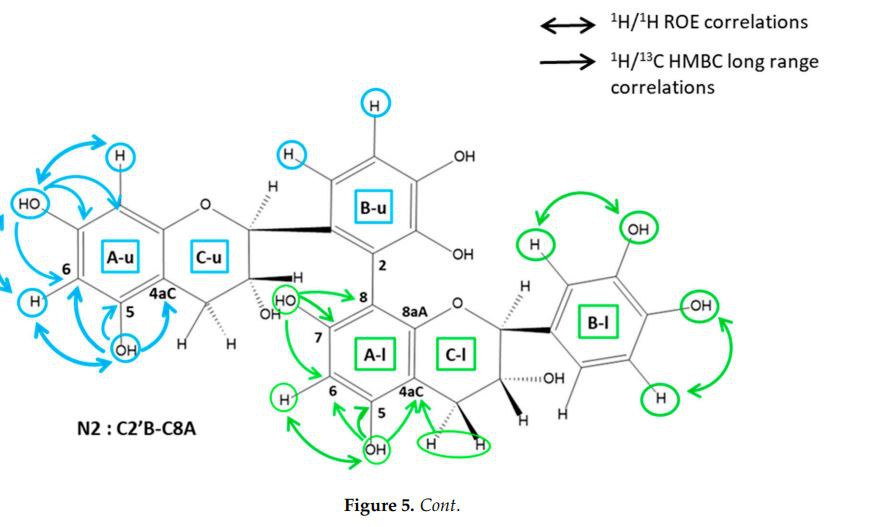

Dímers de les fraccions N3 i N6. Els espectres de les fraccions N3 i N6 van mostrar la presència de dos sistemes de protons d'anell B AMX i la manca d'un senyal de fenol OH. Com que es van identificar tots els protons fenòlics OHA de les unitats dímeres (tal com es descriu anteriorment), el senyal fenòlic OH que falta pot ser el de OH3'B o el de OH4'B.
La posició OH (3'B o 4'B) es pot determinar fàcilment mitjançant correlacions ROE amb H2'Bor H5'B, respectivament, o utilitzant correlacions HMBC de llarg abast tal com es mostra a la figura 5.
L'atribució de l'OH residual dels anells B es va realitzar fàcilment mitjançant correlacions HMBC o ROESY de llarg abast, tal com es mostra a la figura 5. En el cas del dímer N3, es va observar una correlació ROE entre l'H5'B i l'OH residual. 'B de la unitat de catequina enllaçada a través del seu anell B. Aquest OH es va identificar així com OH4'B. En el cas de la fracció N6, l'OH'B residual es va assignar a OH3'B, ja que es va observar una correlació ROE entre aquest OH i H2'B. Les correlacions HMBC de llarg abast estan d'acord amb aquestes atribucions. Les posicions d'enllaç d'aquests dos dímers es van determinar de la següent manera: CO3'B-C8A i CO4'B-C8A per a N3 i N6. respectivament.
Fracció N8. L'anàlisi d'espectre del dímer N8 va mostrar que una unitat d'aquest dímer és la catequina amb dues posicions d'enllaç una l'anell A, una a la posició C8A i l'altra a la posició C-O7A, ja que els protons H8A i OH7A són desaparegut. L'altra unitat d'aquest dímer presentava característiques espectrals singulars, que indicaven la pèrdua de l'aromaticitat de l'anell B i la presència de diverses posicions d'enllaç tant als anells B com als C.
Els senyals de RMN 'H sorgits de l'anell B eren dos doblets a 2,49 i 2,71 ppm, que presentaven un acoblament geminal de ~ 15 Hz (12,03 ppm) típic d'un grup metilè i un singlet a 6,38 ppm sorgit d'un protó etilènic. Com que aquests protons de metilè i etilè no estaven acoblats, és probable que estiguin a les posicions 2'B i 5'B. L'espectre HIMBC va mostrar totes les correlacions, permetent atribucions precises d'aquests carbonis de l'anell B, tal com s'il·lustra a la figura 5. L'H2C d'aquesta unitat va donar tres correlacions amb els carbonis de l'anell B: una és el carboni de metilè a ~ 45 ppm, que així es va atribuir a C2'B, i els dos restants, amb carbonis ressonant a ~ 90 ppm i ~ 162 ppm, que es poden assignar a C1'B i C6'B.H5'B només van donar fortes correlacions de 3J amb dos carbonis quaternaris d'aquest anell B. : un és el carboni assignat prèviament a C3'B (~95 ppm), i l'altre, que va ressonar a ~90 ppm, es podria atribuir així a C1'B. Aleshores es va deduir que el carboni a ~ 162 ppm era C6'B.
La presència d'un OH alifàtic (~ 5, 8 ppm) a la posició C3'B (~ 95 ppm) es va determinar mitjançant la seva correlació ROE amb els dos protons H2'B. A més, OH3/B va donar una correlació HMBC amb un carboni quaternari a ~ 192, 5 ppm, característica d'un grup cetònic a la posició C4'B.
El blindatge d'aquest C1'B d'unes 40 ppm està d'acord amb una pèrdua de l'aromaticitat de l'anell B. A més, la manca d'OH a la posició C7A de l'altra unitat està d'acord amb un enllaç d'èter C1'BO-C7A.
Les dades de RMN van mostrar que l'anell C d'aquesta unitat no té cap OH3C. La presència d'un enllaç C3C-O-C3'B està d'acord amb el blindatge de C3C d'aproximadament 1,5 ppm, així com el desplaçament químic de C3'B que és típic del carboni hemiketal (95 ppm).
En conjunt, les dades espectrals de RMN ens permeten concloure que aquest dímer correspon a la deshidrocatequina A descrita anteriorment per Winges et al.[33] i després per Guyot et al.[20].
Les estructures dels sis compostos dimèrics determinats per aquestes anàlisis de RMN es mostren a la figura 6, sent N2, N3, N6 i N8 productes purs, i N4 és una barreja de dos isòmers.


3. Materials i Mètodes
3.1.Químics
(més)-hidrat de catequina superior o igual al 98 per cent; lacasa de Trametes Versicolor(0,94 U·mg-1); fosfat de sodi dibàsic dihidrat Superior o igual al 98 per cent; àcid cítric (reactiu ACS, nitrat de cadmi tetrahidrat 99,997 per cent; àcid fòrmic i amberlita XAD7HP es van obtenir de Sigma-Aldrich) (Saint-Louis, MO, EUA). L'acetona-dgwa es va comprar a Euriso-top (Saarbrüicken, Alemanya) i trifluoroacètic àcid (TFA) de Roth Labo (Karlsruhe, Alemanya). L'aigua LC-MS, l'acetonitril LC-MS (ACN) i el metanol LC-MS (MeOH) eren tots de VWR (Radnor, PA, EUA).
3.2. Elaboració de la Solució Model de Vi
La solució de vi model era una solució d'etanol/aigua (12/88;o/o) amb àcid tartàric 0,033 M, ajustada a pH 3,6 amb NaOH 1 M [34].
3.3. Extractes de PPO de raïm cru
L'extracte de PPO es va preparar tal com es va descriure anteriorment per Singleton et al.[35]. El raïm congelat es va barrejar primer en un tampó d'acetat (1,5 M, pH 5; 10 gL-I d'àcid ascòrbic). A continuació, es va filtrar la mescla i es va centrifugar (3000 g; 10 min). Finalment, el residu es va rentar amb acetona (80 per cent) i es va assecar a l'aire.
3.4.Lacasa de Botrytis Cinerea
La lacasa de Botrytis cinerea es va obtenir tal com descriuen Quijada-Morin et al.[36]. Es va produir a partir de la soca VA612 (recollida en 2005 en una vinya d'Hautvillers, Champagne, França, a partir del conreu Pinot Noir). Breument, els cultius en medi sòlid de llevat de malta es van deixar durant una setmana a 24 graus sota llum blava. A continuació, es van raspar les espores i es van inocular en un matràs Erlenmeyer de 50{0 mL que contenia 125 mL de medi de cultiu (4{{30}} gL-1glucosa, 7 gL{{1{0}}glicerol, 0,5 g·L-1L-histidina, 0,1 g:L{-1 CuSO,1,8gL-1 NaNO3,0,5g:L -1 KCl,0,5gL-1 CaCl2·H2O,0,05g:L-1 FeSO4,7H2O,1,0g L{-1KH2PO4, i 0,7 gL{-1 MgSO 4-7H2O). Després de 3 dies d'incubació i 2 dies de creixement en el mateix medi anterior, es va afegir àcid gàlic (2 gL-1) als precultius. Després de 5 dies, el medi líquid es va filtrar i el sobrenedant es va sotmetre a filtració tangencial en un sistema de filtració Quixstand (GE Healthcare UK, Little Chalfont, Anglaterra) equipat amb un pes molecular de 30 kDa tallat a la membrana. Finalment es va sotmetre el concentrat a una diafiltració contra aigua destil·lada, i només es van mantenir les fraccions que presentaven activitat oxidant contra ABTS (-80 grau).
3.5.Procediment d'oxidació
Es va preparar prèviament una solució de lacasa (1 gL-1) en tampó fosfat-citrat i es va afegir a una solució de 6g.L{-1(més)-catequina (vi model) per obtenir una concentració final de lacasa de { {6}},3 gL-1. La solució obtinguda es va agitar lentament (180 rpm) a temperatura ambient durant 2 h. Les concentracions es van optimitzar prèviament i l'experimentació es va realitzar per triplicat.
3.6. Atura de reacció a la resina Amberlite XAD7HP
Es va condicionar una columna ambre lite amb etanol (absolut) i es va esbandir amb dos volums de columna d'aigua mili-O. El medi de reacció lacasa/(plus)-catequina anterior es va deixar caure a la columna i es va eluir primer amb dos volums de columna de milli-Qwater [37]. A continuació, es va eluir la columna amb etanol fins que la fracció recollida no va tenir color. Només es van mantenir, evaporar i liofilitzar les fraccions d'etanol. La pols es va emmagatzemar a -80 graus fins que s'ha utilitzat.
3.7.Procediment de purificació de la fracció dimèrica mitjançant cromatografia flash
La pols liofilitzada es va purificar primer mitjançant un sistema de cromatografia flash puriflash430 equipat amb un detector UV establert a 280 nm i una columna Puriflash diol 50 um f0025. La fase mòbil binària consistia en acetonitril (solvent A) i metanol (solvent B), tots dos acidificats amb un 0,1 per cent de TFA. Es va realitzar una sèrie d'injeccions a un cabal constant de 20 mL·min-1, utilitzant el següent gradient: 100 per cent A durant 4,4 min; 0-10 per cent de B en 10 min; 10 per cent de B durant 5 min; 10-90 per cent de B en 5 min; 90 per cent de B durant 3 min;90-10 per cent de B en 2 min; 10 per cent de B durant 10 min. El volum d'injecció era d'1 ml (300 mg de pols liofilitzada dissolta en 1 ml de dissolvent A). Es van recollir tres fraccions diferents cada vegada. El primer corresponia a la catequina residual (plus) i el tercer era una barreja de polifenols d'alt pes molecular. La segona fracció eluïda, que contenia una barreja de productes d'oxidació dimèrica, es va evaporar i liofilitzar abans del segon pas de purificació.
3.8. Procediment de purificació de productes d'oxidació de la fracció dimèrica mitjançant un sistema cromatogràfic de semipreparació
La fracció que contenia productes d'oxidació dimèrica es va purificar mitjançant un sistema de cromatografia a pressió mitjana Bio-Rad NGC 10 semipreparatiu equipat amb una columna Microsorb Varian Dynamax C18 de fase inversa (250 × 21,2 mm; 3 um). La fase mòbil binària constava d'aigua mili-O (solvent A) i 80 per cent d'acetonitril, 20 per cent d'aigua Milli-Q (dissolvent B), tots dos acidificats amb un 0,05 per cent de TFA. Es van realitzar una sèrie d'injeccions (300 μL) de la pols liofilitzada (20 mg dissolts en 200 uL de dissolvent A i 100 uL d'ACN) sota les següents condicions d'elució: 100 per cent A durant 4 min; 0-35 per cent de B en 46 min;35-100 per cent de B en 2 min; 100 per cent de B durant 5 min. Es van recollir vuit fraccions diferents cada vegada, corresponents a senyals UPLC purs a 280 nm. Cada fracció es va evaporar i liofilitzar abans de l'anàlisi de RMN.
3.9.Preparació de la mostra per a l'anàlisi de RMN
Al voltant d'1 mg de cada pols liofilitzada ponderada en tubs Eppendorf es va resoldre en 500 μL d'acetona-dg. A continuació, es van afegir ~ 10 uL d'una solució concentrada de nitrat de cadmi en acetona-d a les mostres i les solucions resultants es van transferir a tubs de RMN de 5 mm per a l'anàlisi de RMN. Es va realitzar un pas addicional per a algunes mostres: després de la solubilització de les pols liofilitzades en acetona-dg en presència de traces de cadmi, les mostres es van evaporar a sequedat i després es van tornar a solubilitzar en acetona-d sense afegir més Cd.
3.10.Especificacions de l'instrument
Anàlisi UPLC-MS. Les reaccions es van controlar mitjançant dos sistemes UPLC-MS. El primer es va utilitzar per identificar amb precisió els temps de retenció dels productes mitjançant un mètode de gradient llarg. és a dir, cromatografia líquida d'ultra-alt rendiment de Waters acoblada a espectrometria de masses (UHPLC-MS). El sistema de cromatografia líquida era un Acquity UPLC (Waters, Milford, MA, EUA) equipat amb un detector de matriu de fotodíodes. Hem utilitzat una columna Acquity UPLC HSS T3 (1,8 um, 2,1 × 150 mm). La temperatura de la columna era de 25 graus. La fase mòbil binària constava de 0,1 per cent d'àcid fòrmic en aigua (solvent A) i acetonitril (solvent B). La separació es va realitzar a un cabal constant de 0,25 mL·min-1, utilitzant el següent gradient: 8-11 per cent de B en 2 min; 11 per cent de B durant 8 min; 11-25 per cent B en 15 min;25-55 per cent Bin 5 min;55-99 per cent Bin 1 min; 99 per cent B durant 4 min;99-8 per cent Bin1 min; 8 per cent B durant 4 min. El volum d'injecció era de 5 μL. L'espectròmetre de masses era un quadrupol simple d'ionització electrospray (ESI) Waters Acquity QDa (Waters, Milford, MA, EUA). La tensió capil·lar es va establir en 0,8 kV. Els espectres de masses es van adquirir en un rang de massa de 200-900 el mode d'ions positius.
El segon sistema UHPLC-MS, utilitzat per a la verificació ràpida durant els passos de purificació, era el mateix que es descriu anteriorment, amb una columna Acquity UHPLC HSS T3 (1,8 μm, 2,1 × 100 mm) escalfada. a 38 graus. La separació es va realitzar a un cabal constant de 0,55 mL·min-1, utilitzant el següent gradient ràpid: 0,1-40 per cent de B en 5 min; 40-99 per cent de B en 2 min; 99 per cent de B durant 1 min; 99-0,1 per cent de B en 1 min. El volum d'injecció era de 2 μL. L'espectròmetre de masses era una trampa d'ions d'ionització electrospray (ESI) Bruker Amazon X (Bruker Daltonics, Bremen, Alemanya). La tensió capil·lar es va establir en -5,5 kV. Els espectres de masses es van adquirir en un rang de masses de 50-2000 el mode d'ions positius.
Totes les anàlisis UPLC-MS es van realitzar per triplicat.
Instrumentació de RMN. Tots els espectres de RMN es van registrar en un espectròmetre Agilent DD{{0}} MHz (Agilent Technologies, Santa Clara, CA, EUA), que funcionava a 500,05 i 125,74 MHz per a nuclis de protons i carboni-13, respectivament, mitjançant una sonda de detecció indirecta de 5 mm equipada amb una bobina de gradient. Programari .1 (Mestrelab Research, Espanya). Les mesures DOSY es van adquirir i processar tal com es va descriure anteriorment 38]. Els paràmetres d'adquisició de la seqüència de polsos DgcsteSL eren els següents: el temps de retard de difusió i l'amplada del pols del gradient es van establir en 50 ms i 2 ms, respectivament, la força del gradient (g) es va incrementar en 16 passos amb un espai g2 igual de 0,3 a 2 ms. 32G·cm-I. Després de la correcció de fase, es van construir espectres DOSY 2D a partir de la mesura de l'alçada màxima mitjançant el programari VNMRJ4.2.
Tots els espectres es van fer referència als senyals de solvent acetona-dg (senyal residual H a 2,05 ppm i senyal 13C a 29,92 ppm).

4. Conclusions
Es va investigar l'acció de tres oxidoreductases diferents (polifenol oxidasa extreta del raïm, lacasa de Botrytis cinerea i lacasa de Trametes Versicolor) sobre (plus)-catequina, i els perfils LC-UV-MS resultants eren molt similars, encara que algunes diferències menors. va suggerir possibles diferències en la reactivitat d'aquests enzims.
Les estructures de sis productes d'oxidació de catequina-laccasa (utilitzant lacasa de Trametes Versicolor) es van obtenir a partir de signatures RMN específiques (quatre productes purs, és a dir, N2, N3, N6 i N8, i N4, corresponents a una barreja de dos isòmers). L'atribució completa de senyals d'OH fenòlics va ser possible gràcies a l'addició de nitrat de cadmi amb un procediment de preparació de mostres que va permetre l'atribució inequívoca dels enllaços entre les unitats de catequina per a alguns dels compostos d'interès. Aquest procediment simplificarà molt l'anàlisi de RMN de mescles de polifenols, ja siguin sintetitzats o extrets de productes naturals.
Els estàndards obtinguts en aquest treball es podran utilitzar en el futur com a marcadors d'oxidació per investigar la seva presència i evolució durant la maduració del raïm i la criança del vi. A més de la catequina, altres compostos polifenolics, inclosos els flavonoides i els no flavonoides, també es poden utilitzar com a substrats de lacasa per obtenir nous estàndards addicionals.
Abreviatures
RMN: ressonància magnètica nuclear,
Cd: cadmi,
TOCSY: espectroscòpia de correlació total,
ROESY: espectroscòpia d'efecte Overhauser nuclear de marc giratori,
HSQC: experiment de correlació quàntica única heteronuclear,
HMBC: connectivitat multibanda heteronuclear,
DOSY: espectroscòpia ordenada per difusió.
Referències
1. Khan, N.; Mukhtar, H. Polifenols del te per a la promoció de la salut. Ciència de la vida. 2007, 81, 519–533. [Ref creuat]
2. Fayeulle, N.; Vallverdu-Queralt, A.; Meudec, E.; Hue, C.; Boulanger, R.; Cheynier, V.; Sommerer, N. Characterization of New Flavan-3-Ol Derivatives in Fermented Cocoa Beans. Química dels Aliments. 2018, 259, 207–212. [CrossRef] [PubMed]
3. Rimbach, G.; Melchin, M.; Moehring, J.; Wagner, AE Polifenols del cacau i la salut vascular: una revisió crítica. Int. J. Mol. Ciència. 2009, 10, 4290–4309. [Ref creuat]
4. Avram, AM; Morin, P.; Brownmiller, C.; Howard, LR; Sengupta, A.; Wickramasinghe, SR Concentracions de polifenols d'extracte d'orujo de nabius mitjançant nanofiltració. Bioprod alimentari. Procés. 2017, 106, 91–101. [Ref creuat]
5. Antoniolli, A.; Fontana, AR; Piccoli, P.; Bottini, R. Caracterització de polifenols i avaluació de la capacitat antioxidant en orujo de raïm del Cv. Malbec. Química dels Aliments. 2015, 178, 172–178. [Ref creuat]
6. Saucier, C. Com evolucionen els polifenols del vi durant l'envelliment del vi? Cerevisia 2010, 35, 11–15. [Ref creuat]
7. Oliveira, CM; Ferreira, ACS; De Freitas, V.; Silva, AMS Mecanismes d'oxidació que es produeixen als vins. Alimentació Res. Int. 2011, 44, 1115–1126. [Ref creuat]
8. Singleton, VL Oxigen amb fenols i reaccions relacionades en mostos, vins i sistemes model: observacions i implicacions pràctiques. Am. J. Enol. Vitic. 1987, 38, 69–77.
9. Mathew, AG; Parpia, HAB El bruniment dels aliments com a reacció de polifenols. En els avenços en la investigació alimentària; Chichester, CO, Mrak, EM, Stewart, GF, Eds.; Academic Press: Cambridge, MA, EUA, 1971; Volum 19, pàgs. 75–145. [Ref creuat]
10. Gambuti, A.; Rinaldi, A.; Ugliano, M.; Moio, L. Evolució dels compostos fenòlics i l'astringència durant l'envelliment del vi negre: efecte de l'exposició a l'oxigen abans i després de l'embotellat. J. Agric. Química dels Aliments. 2013, 61, 1618–1627. [CrossRef] [PubMed]






